BRDT thúc đẩy sự phát triển của tế bào ung thư buồng trứng
- Ling Chen ,
- Thượng Cai ,
- Jing-mei Wang ,
- Ying-ying Huai ,
- Pei-Hua Lu &
- Qian Chu
Tế bào chết & bệnh âm lượng 11 , Số bài viết : 1021 ( 2020 ) Trích dẫn bài viết này
- Số liệuchi tiết
trừu tượng
Yếu tố đặc hiệu cho tinh hoàn bromodomain (BRDT) là một thành viên của protein họ bromodomain và ngoài đầu cuối (BET). Biểu hiện và các chức năng tiềm ẩn của nó trong ung thư buồng trứng đã được kiểm tra. Chúng tôi cho thấy rằng BRDT được biểu hiện quá mức trong các mô ung thư buồng trứng ở người và trong các tế bào ung thư buồng trứng nguyên phát (CaOV3) / nguyên phát. Tuy nhiên, biểu hiện của nó ít ở các mô và tế bào biểu mô buồng trứng. Đáng kể, sự im lặng do shRNA gây ra hoặc loại bỏ BRDT qua trung gian CRISPR / Cas9 đã ức chế sự phát triển, khả năng tồn tại, tăng sinh và di chuyển của tế bào ung thư buồng trứng, đồng thời kích hoạt quá trình apoptosis đáng kể. Ngược lại, sự biểu hiện quá mức ngoại sinh của BRDT, bởi một cấu trúc ngoại vi, làm tăng sự di cư và tăng sinh tế bào CaOV3. Trong tế bào CaOV3, sự biểu hiện của hai gen đích BRDT chính, kinase 1 giống polo (PLK1) và aurora kinase C (AURKC), được điều chỉnh giảm bởi BRDT shRNA hoặc loại trực tiếp, nhưng được điều chỉnh bằng BRDT biểu hiện quá mức. In vivo, các khối u xenograft có nguồn gốc từ tế bào CaOV3 loại trực tiếp BRDT phát triển chậm hơn đáng kể so với các khối u kiểm soát ở chuột bị suy giảm miễn dịch kết hợp (SCID) nghiêm trọng. Hơn nữa, tiêm virut BRDT shRNA lentivirus vào khoang miệng đã ức chế mạnh mẽ sự phát triển của các tế bào ung thư buồng trứng nguyên phát ở chuột SCID. Điều hòa giảm PLK1 và AURKC được phát hiện trong các mô khối u loại bỏ BRDT và BRDT im lặng. Nói chung, sự biểu hiện quá mức của BRDT thúc đẩy sự tiến triển của tế bào ung thư buồng trứng. Nhắm mục tiêu BRDT có thể là một chiến lược mới để điều trị ung thư buồng trứng. tiêm vào trong khoang miệng của BRDT shRNA lentivirus ức chế mạnh sự phát triển của các tế bào ung thư buồng trứng nguyên phát ở chuột SCID. Điều hòa giảm PLK1 và AURKC được phát hiện trong các mô khối u loại bỏ BRDT và BRDT im lặng. Nói chung, sự biểu hiện quá mức của BRDT thúc đẩy sự tiến triển của tế bào ung thư buồng trứng. Nhắm mục tiêu BRDT có thể là một chiến lược mới để điều trị ung thư buồng trứng. tiêm vào trong khoang miệng của BRDT shRNA lentivirus ức chế mạnh sự phát triển của các tế bào ung thư buồng trứng nguyên phát ở chuột SCID. Điều hòa giảm PLK1 và AURKC đã được phát hiện trong các mô khối u loại bỏ BRDT và BRDT im lặng. Nói chung, sự biểu hiện quá mức của BRDT thúc đẩy sự tiến triển của tế bào ung thư buồng trứng. Nhắm mục tiêu BRDT có thể là một chiến lược mới để điều trị ung thư buồng trứng.
Giới thiệu
Mặc dù đã đạt được những tiến bộ đáng kể để cải thiện tỷ lệ sống chung của bệnh ung thư buồng trứng trong những thập kỷ qua, nó vẫn là một trong những nguyên nhân chính gây tử vong ở nữ giới 1 . Chỉ riêng tại Hoa Kỳ, Hiệp hội Ung thư Hoa Kỳ ước tính có 22.440 trường hợp ung thư buồng trứng mới và 14.080 trường hợp tử vong liên quan mỗi năm 2 . Ung thư buồng trứng thường được chẩn đoán ở giai đoạn muộn do thiếu chiến lược tầm soát 3 , 4 , 5 hiệu quả . Phương pháp điều trị tiêu chuẩn cho ung thư buồng trứng mới được chẩn đoán bao gồm phẫu thuật và hóa trị liệu dựa trên bạch kim 3 , 4 , 5. Tuy nhiên, do khả năng kháng thuốc và khả năng tái phát đáng kể, các nhà nghiên cứu đang tập trung vào các tế bào sinh ung thư mới và các con đường tín hiệu tế bào cần thiết cho sự tiến triển của ung thư 3 , 4 , 5 .
Yếu tố đặc hiệu cho tinh hoàn bromodomain (BRDT) là một thành viên của protein họ bromodomain và ngoài đầu cuối (BET) 6 . BRDT, giống như các protein gia đình BET khác (BRD1–4), điều chỉnh biểu sinh sự biểu hiện của gen mục tiêu thông qua tương tác với acetylated lysine 7 , 8 , rất quan trọng đối với sự phát triển bình thường và tiến triển của bệnh (ung thư) 6 . Các nghiên cứu gần đây đã ngụ ý rằng các protein họ BET là các protein gây ung thư quan trọng, được biểu hiện quá mức trong một số bệnh ung thư khác nhau 7 , 8 . Các chất ức chế protein BET đã cho thấy hiệu quả đầy hứa hẹn chống lại các tế bào ung thư ở người trong ống nghiệm và in vivo 9 , 10 .
BRDT được biểu hiện trong tinh hoàn, điều chỉnh sự biểu hiện của gen meiotic và gen sau meiotic để thúc đẩy quá trình sinh tinh 11 . Tế bào ung thư có khả năng kích hoạt lại các gen hạn chế tinh hoàn im lặng bình thường, rất quan trọng đối với sự tiến triển của ung thư 6 . Các nghiên cứu gần đây đã chỉ ra rằng BRDT được kích hoạt ngoại bào và biểu hiện trong bệnh ung thư ở người 6 . Người ta đã đề xuất rằng BRDT có thể là một dấu ấn sinh học mới và có thể là một mục tiêu điều trị cho bệnh ung thư ở người 6 . Một số gen điều chỉnh BRDT, bao gồm polo-like kinase 1 (PLK1) 12 và aurora kinase C (AURKC) 13 , là các protein gây ung thư quan trọng 6 , 11. Cho đến nay, biểu hiện BRDT và các chức năng tiềm ẩn trong ung thư buồng trứng vẫn chưa được nghiên cứu.
Nguyên liệu và phương pháp
Hóa chất và thuốc thử
Thuốc thử nuôi cấy tế bào được cung cấp bởi Gibco Co. (Grand Island, NY). Puromycin, polybrene và các thuốc thử khác được lấy từ Sigma-Aldrich (St. Louis, Mo). Tất cả các đoạn mồi, trình tự và cấu trúc virus đều được cung cấp bởi Shanghai Genechem Co (Thượng Hải, Trung Quốc). Kháng thể chống BRDT được mua từ Sigma-Aldrich (SAB2106423). Các kháng thể cho polymerase phân cắt-caspase-3 (# 9664), polymerase phân cắt-poly (ADP-ribose) (PARP) (# 5625), phân cắt-caspase-9 (# 20750), Tubulin (# 2125) và PLK1 (# 4513) được lấy từ Cell Signaling Tech China (Thượng Hải, Trung Quốc). Kháng thể kháng AURKC được lấy từ Abcam (ab46783). Thuốc thử cho xét nghiệm RNA được cung cấp bởi Thermo-Fisher Invitrogen (Tô Châu, Trung Quốc).
Mô người
Từ tổng số sáu (6) bệnh nhân ung thư buồng trứng nguyên phát, các mô ung thư buồng trứng ở người tươi (“Ca”) và mô biểu mô buồng trứng cận ung thư (“S”) đã được thu nhận. Các mô được rửa sạch, băm nhỏ và đồng nhất trong đệm ly giải mô (Công nghệ sinh học Beyotime, Thượng Hải, Trung Quốc), được bảo quản trong nitơ lỏng. Sự biểu hiện của BRDT được kiểm tra bằng PCR định lượng men sao chép ngược (“qPCR”) và xét nghiệm thấm phương tây. Mỗi người tham gia đều nhận được sự đồng ý bằng văn bản. Các bệnh nhân tham gia không được hóa trị trước khi phẫu thuật. Mô tinh hoàn bình thường đã được phẫu thuật cắt bỏ được cung cấp bởi một bệnh nhân ung thư tinh hoàn được thông báo bằng văn bản được quản lý tại Bệnh viện Côn Sơn trực thuộc Đại học Giang Tô.
Nuôi cấy tế bào
Dòng tế bào ung thư buồng trứng CaOV3 được mua từ Ngân hàng Tế bào của Viện Khoa học Sinh học Thượng Hải, CAS (Thượng Hải, Trung Quốc). Tế bào được nuôi cấy trong môi trường được mô tả trước đây 14 . Tế bào biểu mô buồng trứng bình thường (“OE”) được cung cấp bởi Tiến sĩ Bi 14 , được nuôi cấy trong môi trường MCDB109 / M199 với 20% huyết thanh bò thai (FBS). Các mô ung thư buồng trứng đạt được được rửa trong nước muối có đệm photphat trong năm lần và băm thành các mảnh nhỏ (1 mm 3), được tiêu hóa bởi Collagenase I (Sigma-Aldrich) và DNase (Sigma-Aldrich). Huyền phù đơn bào được tạo thành viên và rửa sạch trong môi trường Eagle cải tiến (DMEM) của Dulbecco. Nguyên bào sợi, tế bào mạch máu và tế bào miễn dịch bị loại bỏ thông qua phương pháp cơ học và ly tâm. Các tế bào ung thư buồng trứng nguyên phát ở người đã tinh khiết được nuôi cấy trong môi trường được mô tả trước đây 15 . Bốn tế bào ung thư buồng trứng khác nhau được thành lập, được đặt tên là “pOC-1/4”. Tất cả các tế bào đều được kiểm tra thường xuyên để loại trừ khả năng nhiễm mycoplasma và vi sinh vật. Xác thực bằng cách lập hồ sơ STR, thời gian nhân đôi dân số và hình thái tế bào cũng được kiểm tra thường xuyên để xác minh các kiểu gen 3–4 tháng một lần.
qPCR
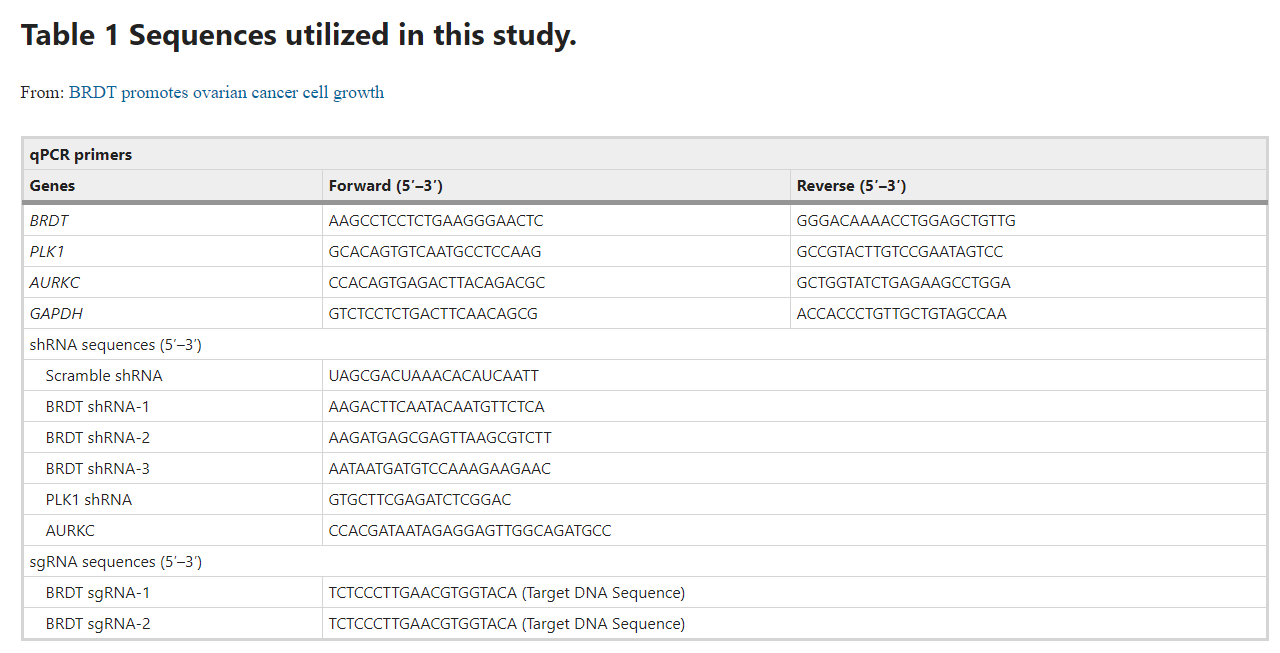
Thuốc thử trizol (Promega, Madison, WI) được thêm vào để tách chiết RNA. Một bộ kit SYBR Green PCR (Hệ thống Sinh học Ứng dụng, Thành phố Foster, CA) đã được sử dụng để phiên mã ngược trong hệ thống PCR Thời gian thực Nhanh ABI Prism7500. Một phân tích đường cong nóng chảy được thực hiện để tính toán nhiệt độ nóng chảy của sản phẩm. Để định lượng biểu hiện gen mục tiêu, phương pháp 2 -∆∆Ct đã được áp dụng, với GAPDH được kiểm tra như là kiểm soát nội bộ. Các chất mồi được liệt kê trong Bảng 1 .
Thấm Tây
Tế bào hoặc mô được ủ với đệm ly giải được mô tả 14 . Phần lớn 40 µg protein của mỗi điều kiện được phân tách bằng gel điện di trên gel natri dodecyl sulphat-polyacrylamide 10% và sau đó được chuyển sang các khối PVDF (Millipore, Bedford, MA). Sau khi ngăn chặn, các đốm màu được ủ với các kháng thể sơ cấp cụ thể (qua đêm ở 4 ° C) và các kháng thể thứ cấp tương ứng (2 giờ ở nhiệt độ phòng) 14 . Liên kết kháng thể-kháng nguyên đã được kiểm tra bằng hệ thống phát quang hóa học (ECL) nâng cao (Amersham Biosciences, Piscataway, NJ). Phần mềm Image J (NIH) đã được sử dụng để định lượng dữ liệu.
Thử nghiệm MTT
Các tế bào, với các thao tác di truyền khác nhau, ban đầu được gieo vào các đĩa 96 giếng với mật độ 2,5 × 10 3 tế bào trên mỗi giếng. Sau khi ủ trong 72 giờ, khả năng sống của tế bào được kiểm tra bằng xét nghiệm MTT. Mật độ quang MTT (OD) được đo ở bước sóng 550 nm.
Thử nghiệm BrdU
Tế bào ung thư buồng trứng được cấy vào đĩa 96 giếng với mật độ 2,5 × 10 3 tế bào mỗi giếng. Sau khi ủ với BrdU (10 μM, Cell Signaling Tech, Thượng Hải, Trung Quốc) trong 48 giờ, các tế bào được rửa sạch và việc kết hợp BrdU được kiểm tra bằng bộ ELISA (Cell Signaling Tech), với độ hấp thụ ELISA được kiểm tra ở bước sóng 405 nm.
Thử nghiệm “Transwell”
Tế bào CaOV3 biến đổi gen (1,5 × 10 5 tế bào trong môi trường không chứa huyết thanh 250 μL) được cấy vào các khoang trên “Transwell” (kích thước lỗ chân lông 16 μm, BD Biosciences, Thượng Hải, Trung Quốc). Các ngăn dưới chứa đầy 10% môi trường FBS. Sau 24 giờ, các tế bào không di chuyển ở bề mặt trên được loại bỏ. Các tế bào di cư, ở bề mặt dưới, được cố định, nhuộm màu và đếm.
Thử nghiệm hoạt động Caspase-3
Dịch ly giải tế bào ung thư buồng trứng (20 μg mỗi nghiệm thức) được trộn với chất đệm xét nghiệm được mô tả 16 , cùng với chất nền caspase-3 (Ac-DEVD-AFC). Sau khi rửa nhiều lần, hoạt tính AFC của enzym caspase-3 được đo ở bước sóng kích thích 380 nm và bước sóng phát xạ 440 nm.
Nhuộm EdU
Tế bào ung thư buồng trứng với các chỉnh sửa di truyền được áp dụng được cấy vào đĩa 24 giếng (3 × 10 4 tế bào trên mỗi giếng) và nuôi cấy trong 48 giờ. Tiếp theo, xét nghiệm nhuộm EdU (5-ethynyl-20-deoxyuridine) được thực hiện bằng cách sử dụng quy trình được mô tả ở nơi khác 17 , 18 . Tỷ lệ phần trăm EdU (EdU so với DAPI,%) của 800 ô trong năm chế độ xem ngẫu nhiên (mỗi lần điều trị, độ phóng đại 1 × 100) đã được ghi lại.
Khử cực ti thể
Thuốc nhuộm huỳnh quang JC-1 có thể tạo thành các monome màu xanh lá cây bằng cách tập hợp trong ty thể trong tế bào apoptotic với sự khử cực của ty thể 19 . Tế bào ung thư buồng trứng với các chỉnh sửa di truyền được áp dụng được cấy vào đĩa 24 giếng (3 × 10 4 tế bào trên mỗi giếng) và nuôi cấy trong 48 giờ. Các tế bào sau đó được nhuộm bằng JC-1 (10 μg / mL, Sigma). Hình ảnh huỳnh quang JC-1, tích hợp bước sóng màu xanh lá cây (ở 488 nm) và màu đỏ (ở 625 nm) đã được trình bày. Cường độ huỳnh quang xanh JC-1 (ở 488 nm) cũng được ghi lại.
Gien điều khiển bằng RNA kẹp tóc ngắn (shRNA) im lặng
Có các shRNA khác nhau, nhắm mục tiêu các trình tự không chồng chéo (“−1 / −2 / −3”, được liệt kê trong Bảng 1 ) của BRDT , được nhân bản riêng lẻ thành GV248 (hU6-MCS-Ubiquitin-EGFP-IRES-puromycin) xây dựng. Cấu trúc shRNA, cùng với plasmid của gói lentivirus, đã được đồng chuyển sang các tế bào HEK-293 để tạo ra BRDT shRNA lentivirus. Sau quá trình lọc và làm giàu, vi rút được thêm vào tế bào ung thư buồng trứng (được nuôi cấy trong môi trường polybrene, giống nhau đối với tất cả các quy trình vi rút). Các tế bào bị nhiễm bệnh sau đó được chọn lọc bằng puromycin (2,0 μg / mL) trong 4–5 đoạn khác. Sự tiêu diệt BRDT trong các tế bào ổn định đã được xác minh bằng qPCR và thử nghiệm thấm phương Tây. Sự im lặng của PLK1 và AURKC được thực hiện theo cùng một quy trình, với trình tự shRNA của chúng được liệt kê trong Bảng 1.
Loại trực tiếp BRDT
RNA hướng dẫn đơn (sgRNA) nhắm mục tiêu BRDT (hai trình tự khác nhau, “sgRNA-1 / -2”, được liệt kê trong Bảng 1 , do Shanghai Genechem Co. cung cấp) được nhân bản phụ thành cấu trúc lenti-CRISPR-GFP-puro , được truyền sang các tế bào HEK-293 cùng với các plasmid của gói vi-rút lentivirus để tạo ra vi-rút BRDT-KO. Vi rút được lọc, làm giàu và thêm vào các tế bào ung thư buồng trứng trong 24 giờ. Các tế bào được chọn lọc với puromycin (2,0 μg / mL) trong 4–5 đoạn. Trong kết quả các tế bào ổn định BRDT KO đã được xác minh bằng phương pháp thấm phương tây và xét nghiệm qPCR.
Biểu hiện quá mức của BRDT và những người khác
BRDT cDNA có chiều dài đầy đủ được tổng hợp và xác minh trình tự bởi Shanghai Genechem Co, được nhân bản phụ thành vectơ GV248. Cấu trúc này sau đó được chuyển sang các tế bào HEK-293 với plasmid đóng gói ngoại vi 20 , tạo ra lentivirus biểu hiện BRDT (“LV-BRDT”). Sau quá trình lọc và làm giàu, LV-BRDT được thêm vào các tế bào ung thư buồng trứng. Sau đó, puromycin (2,0 μg / mL) được đưa vào để chọn các tế bào ổn định, trong đó sự biểu hiện quá mức của BRDT đã được xác minh bằng các xét nghiệm Western blotting và qPCR. Các ô kiểm soát đã bị nhiễm vi-rút lentivirus có vectơ trống (“LV-C”). Sự biểu hiện quá mức của PLK1 và AURKC ngoài tử cung thông qua cùng một quy trình.
Xét nghiệm Xenograft
Chuột thiếu miễn dịch kết hợp (SCID) nghiêm trọng (17,5–18,5 g, 4–5 tuần tuổi) được lấy từ Trung tâm Động vật của Học viện Khoa học Trung Quốc (Thượng Hải, Trung Quốc). Tế bào chính CaOV3 hoặc pOC-1 (đối với mỗi con chuột, 5 × 10 6 tế bào trong 100 μL DMEM cộng với 100 μL Matrigel, không có huyết thanh) được tiêm dưới da (sc) vào hai bên sườn phải của chuột SCID. Sau 3 tuần, các vết xước dưới da được thiết lập (khoảng 100 mm 3 ) và các bản ghi được bắt đầu (Ngày-0, hoặc “D0”). Trọng lượng cơ thể chuột và các phép đo khối u hai chiều được ghi lại bảy ngày một lần trong tổng số 35 ngày. Các giao thức động vật đã được phê duyệt bởi Ban Đạo đức và IACUC của Bệnh viện Côn Sơn trực thuộc Đại học Giang Tô.
Phân tích thống kê
Các thí nghiệm in vitro được lặp lại ít nhất ba lần và thu được kết quả tương tự. Các giá trị được chuẩn hóa khi cần thiết và được biểu thị dưới dạng trung bình ± độ lệch chuẩn (SD, phân phối chuẩn). Đối với phân tích thống kê, phần mềm SPSS (phiên bản 21.0, sử dụng ANOVA một chiều) đã được sử dụng. Để kiểm tra ý nghĩa giữa hai nhóm điều trị, thử nghiệm t- không ghép đôi hai phía (Excel 2007) đã được sử dụng. Tất cả các khác biệt được coi là có ý nghĩa ở P <0,05.
Các kết quả
BRDT biểu hiện quá mức trong ung thư buồng trứng
Đầu tiên, cơ sở dữ liệu proteomicsdb ( www.proteomicsdb.org ) đã được tham khảo để xác minh sự biểu hiện BRDT trong mô người. Như đã chỉ ra, protein BRDT chủ yếu được biểu hiện trong các mô tinh hoàn, phổi và buồng trứng (Hình 1A ), rất ít được phát hiện trong các mô khác của con người. Để xác minh dữ liệu, tổng cộng sáu mô ung thư buồng trứng (“Ca”) và các mô biểu mô buồng trứng bình thường được ghép nối xung quanh (“S”) đã được thử nghiệm. Các mô này được lấy từ sáu bệnh nhân ung thư buồng trứng nguyên phát khác nhau: Pat-1 đến Pat-6. Kết quả qPCR, Hình 1B , đã chứng minh rằng biểu hiện mRNA BRDT tương đối thấp trong các mô biểu mô buồng trứng bình thường (Hình 1B ), nhưng được điều chỉnh đáng kể ở 5 trong số 6 mô ung thư (Pat-1 đến Pat-5, Hình.1B ). Sự điều hòa protein BRDT cũng được phát hiện trong năm mô ung thư buồng trứng (Hình 1C ). Một lần nữa, biểu hiện protein BRDT thấp đã được phát hiện trong các mô biểu mô buồng trứng (Hình 1C ). Biểu hiện BRDT trong mô tinh hoàn của người được chứng minh là đối chứng dương tính (Hình 1B, C ).
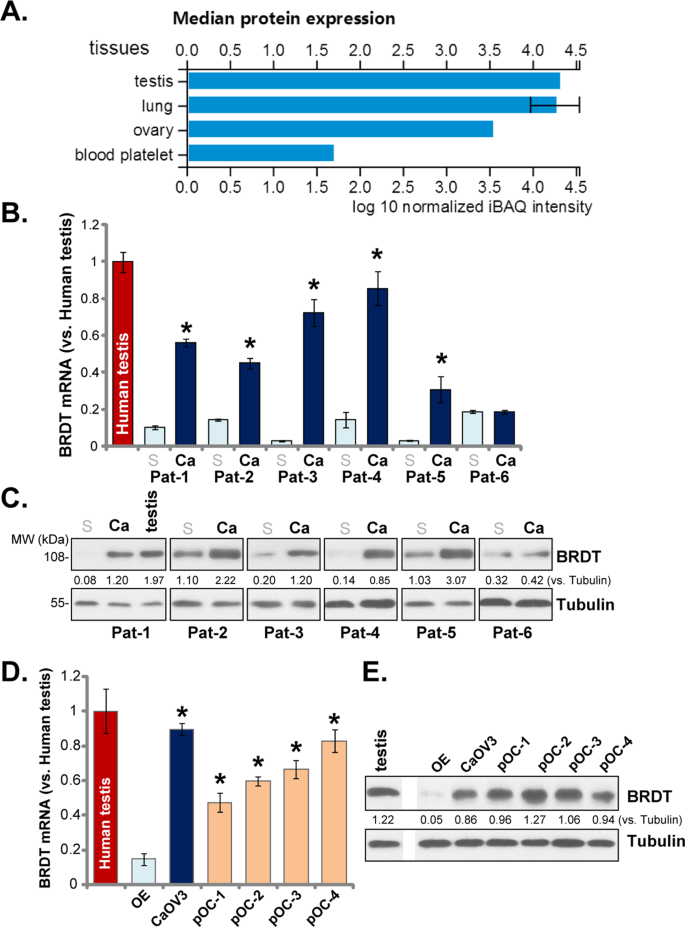
Hồ sơ biểu hiện protein BRDT từ cơ sở dữ liệu proteomicsdb ( A ). BRDT mRNA và biểu hiện protein trong các mô ung thư buồng trứng ở người được liệt kê (“Ca”) và mô biểu mô buồng trứng bình thường bị ung thư (“S”), cũng như trong các tế bào ung thư buồng trứng được liệt kê và tế bào biểu mô buồng trứng (“OE”) là được kiểm tra bằng các xét nghiệm qPCR ( B và D ) và Western blotting ( C và E ). Mỗi mô được cắt ngẫu nhiên thành năm mảnh khác nhau ( B ). Biểu hiện BRDT trong các mô tinh hoàn của người được thử nghiệm là đối chứng dương tính ( B – E ). Biểu hiện protein BRDT được định lượng và chuẩn hóa thành Tubulin ( C và E). Đối với mỗi thử nghiệm, n = 5 ( D ). * P <0,05 so với mô “S” ( B ) hoặc tế bào “OE” ( D ). Các thí nghiệm trong hình này được lặp lại ba lần, với các kết quả tương tự.
Trong tế bào ung thư buồng trứng nguyên phát (dòng tế bào CaOV3) và tế bào ung thư buồng trứng người nguyên phát, biểu hiện mRNA BRDT (Hình 1D ) và protein (Hình 1E ) cao hơn đáng kể so với tế bào biểu mô buồng trứng (“OE”). Các tế bào ung thư chính có nguồn gốc từ bốn mô ung thư buồng trứng có sự điều chỉnh BRDT đáng kể (“Pat-1 / -2 / -3 / -4”, xem Hình 1B, C ). Các kết quả này cùng nhau cho thấy BRDT được biểu hiện quá mức trong các mô và tế bào ung thư buồng trứng ở người.
BRDT shRNA ức chế sự tồn tại, phát triển, tăng sinh và di cư của tế bào ung thư buồng trứng
Chúng tôi đã kiểm tra xem BRDT có đóng một vai trò nào đó trong các hành vi gây ung thư của tế bào ung thư buồng trứng hay không. Ba shRNA BRDT khác nhau, với trình tự không chồng chéo (cụ thể là “shBRDT-1 / -2 / -3”, được liệt kê trong Bảng 1 ), được chuyển riêng lẻ sang các tế bào CaOV3. Sau khi chọn lọc bằng puromycin, các tế bào ổn định được thiết lập. Phân tích sự biểu hiện BRDT mRNA, bằng qPCR, đã chứng minh rằng mức độ BRDT mRNA đã giảm đáng kể trong các tế bào ổn định với BRDT shRNA (Hình 2A ). Mức protein BRDT cũng được điều chỉnh thấp hơn (Hình 2A ). Kết quả xét nghiệm đếm tế bào, trong Hình 2B, đã chứng minh rằng các tế bào CaOV3 ổn định với BRDT shRNA tăng trưởng chậm hơn đáng kể so với các tế bào đối chứng (với shRNA kiểm soát xáo trộn / “shSCR”). Sự hạ gục BRDT trong tế bào CaOV3 đã ức chế khả năng tồn tại của tế bào (MTT OD, Hình 2C ) và tăng sinh (kết hợp BrdU, Hình 2D ). Hơn nữa, BRDT im lặng làm giảm tỷ lệ nhân EdU dương tính trong tế bào CaOV3, khẳng định thêm sự ức chế tăng sinh (Hình 2E ). Kết quả xét nghiệm “Transwell”, Hình 2F , chứng minh rằng các shRNA BRDT được áp dụng đã ức chế sự di chuyển của tế bào CaOV3 trong ống nghiệm (Hình 2F ).
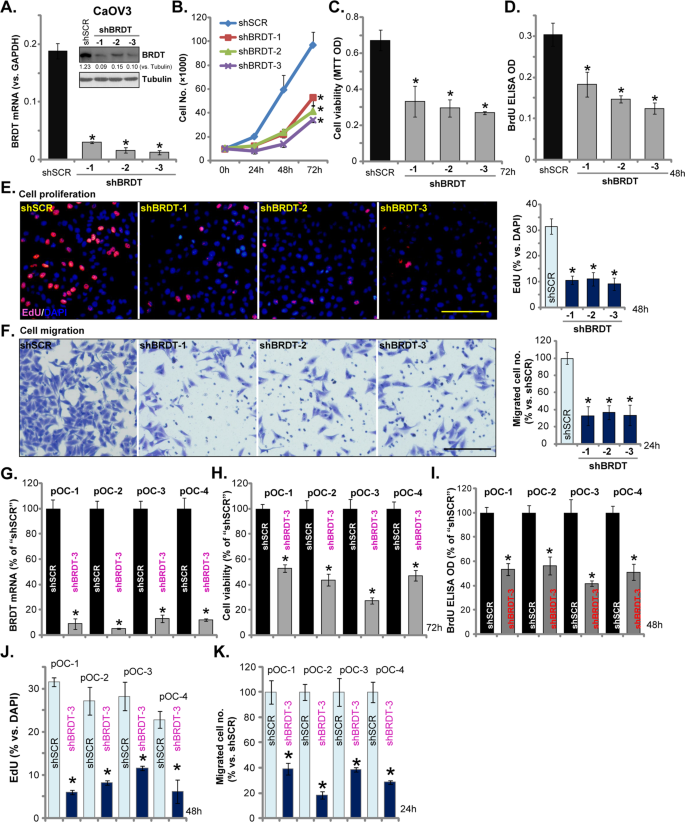
Tế bào CaOV3 ( A – F ) hoặc tế bào ung thư buồng trứng nguyên phát ở người (“pOC-1 / -2 / -3 / -4”) ( G – K ) đã được truyền nhiễm virut shRNA lentivirus kiểm soát xáo trộn (“shSCR”) hoặc BRDT shRNA lentivirus (“shBRDT-1 / -2 / -3”, với trình tự shRNA khác nhau) trong 24 giờ, các tế bào ổn định được chọn bằng puromycin. BRDT mRNA hoặc biểu hiện protein đã được hiển thị ( A và G ); Tăng trưởng tế bào ( B ), khả năng tồn tại (xét nghiệm MTT, C và H ), cũng như tăng sinh (xét nghiệm nhuộm BrdU ELISA và EdU, D , E , I và J), và sự di chuyển của tế bào (xét nghiệm “Transwell”, F và K ) được kiểm tra bằng các xét nghiệm thích hợp, kết quả được định lượng. Đối với các thử nghiệm chức năng, cùng một lượng tế bào sống sót với các biến đổi gen khác nhau ban đầu (ở 0 giờ) được gieo vào mỗi giếng / đĩa và được nuôi cấy trong các khoảng thời gian áp dụng (giống nhau cho tất cả các Hình). Biểu hiện protein BRDT được định lượng và chuẩn hóa thành Tubulin ( A ). Đối với mỗi thử nghiệm, n = 5 (năm đĩa hoặc giếng). * P <0,05 so với ô “shSCR”. Các thí nghiệm trong hình này được lặp lại năm lần, với các kết quả tương tự. Thang đo = 100 μm ( E và F ).
Để kiểm tra chức năng của BRDT trong các tế bào nguyên phát, các tế bào ung thư buồng trứng nguyên phát ở người (“pOC-1 / -2 / -3 / -4”, có nguồn gốc từ các bệnh nhân khác nhau, xem Hình 1 ) đã được truyền gen BRDT shRNA (“shBRDT- 3 ”). Các tế bào ổn định đạt được bằng cách chọn lọc puromycin, cho thấy biểu hiện mRNA BRDT giảm đáng kể (Hình 2G ). BRDT shRNA ức chế mạnh khả năng tồn tại của tế bào (MTT OD, Hình 2H ) và sự tăng sinh (BrdU ELISA OD, Hình 2I ) trong các tế bào ung thư nguyên phát. Ngoài ra, tỷ lệ hạt nhân dương tính với EdU đã giảm đáng kể sau khi BRDT im lặng (Hình 2J ). Hơn nữa, BRDT im lặng ức chế sự di chuyển trong ống nghiệm của các tế bào ung thư nguyên phát (xét nghiệm “Transwell”, Hình. 2K). Nhìn chung, những kết quả này cho thấy BRDT im lặng có tác dụng chống tế bào ung thư buồng trứng đáng kể.
BRDT im lặng kích thích kích hoạt quá trình apoptosis ở các tế bào ung thư buồng trứng
Ở tế bào ung thư buồng trứng, sự ức chế và ngừng tăng trưởng khả năng sống của tế bào có thể gây ra kích hoạt quá trình apoptosis 21 , 22 . Tiếp theo, chúng tôi kiểm tra xem liệu BRDT im lặng có thể tạo ra quá trình chết rụng ở tế bào ung thư buồng trứng hay không. Chúng tôi cho thấy rằng BRDT im lặng, bằng shBRDT-1 / -2 / -3 (xem Hình 2 ), làm tăng đáng kể hoạt động của caspase-3 trong các tế bào CaOV3 (Hình 3A ). Sự phân cắt của caspase-3, caspase-9 và PARP được phát hiện trong các tế bào CaOV3 được BRDT im lặng (Hình 3B ). Hơn nữa, các đứt gãy DNA do BRDT shRNA gây ra, được chứng minh bằng sự tích tụ DNA sợi đơn (ssDNA) (Hình 3C ). Các kết quả thí nghiệm bổ sung cho thấy rằng các monome màu xanh lá cây JC-1 được tích lũy trong các tế bào CaOV3 được BRDT im lặng, cho thấy sự khử cực của ty thể.19 (Hình 3D ). Những kết quả này cho thấy sự kích hoạt của con đường chết rụng của ty thể trong các tế bào CaOV3 được giữ kín BRDT3 23 , 24 , 25 , 26 . Trong các tế bào CaOV3 biểu hiện shRNA BRDT, sự hoạt hóa apoptosis được khẳng định thêm bằng cách tăng số lượng nhân apoptotic, cho thấy nhuộm Hoechst 33342 hạt nhân cô đặc hoặc phân mảnh (Hình 3E ). Các nhân apoptosis đặc trưng được đánh dấu sao vàng (Hình 3E ) chỉ một phần trong số chúng dương tính với TUNEL (huỳnh quang màu tím, Hình 3E , giống nhau cho tất cả các hình).
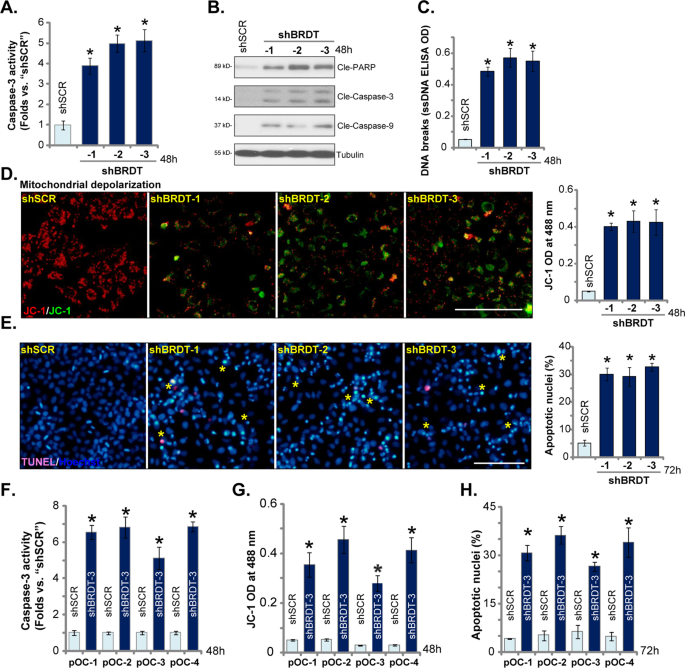
Tế bào CaOV3 ( A – E ) hoặc tế bào ung thư buồng trứng nguyên phát ở người (“pOC-1 / -2 / -3 / -4”) ( F – H ) đã được truyền nhiễm virut shRNA lentivirus kiểm soát xáo trộn (“shSCR”) hoặc BRDT shRNA lentivirus (“shBRDT-1 / -2 / -3”, với trình tự shRNA khác nhau) trong 24 giờ, các tế bào ổn định được chọn bằng puromycin; Các tế bào được nuôi cấy thêm trong các khoảng thời gian áp dụng, kích hoạt caspase ( A , B và F ), hàm lượng DNA sợi đơn (ssDNA) ( C ), khử cực ty thể (xét nghiệm JC-1, D và G ) đã được kiểm tra. Quá trình chết rụng tế bào đã được kiểm tra bằng xét nghiệm nhuộm màu hạt nhân Hoechst 33342 ( E vàH ). Đối với mỗi thử nghiệm, n = 5 (năm đĩa hoặc giếng). * P <0,05 so với ô “shSCR”. Các thí nghiệm trong hình này được lặp lại năm lần, với các kết quả tương tự. Thang đo = 100 μm ( D và E ).
Trong các tế bào ung thư buồng trứng nguyên phát ở người (“pOC-1 / -2 / -3 / -4”), sự im lặng BRDT do shBRDT-3 gây ra (xem Hình 2 ) dẫn đến tăng hoạt tính caspase-3 (Hình 3F ), khử cực ti thể (tích tụ đơn phân màu xanh lá cây JC-1, Hình 3G ) và tăng nhân apoptotic (Hình 3H ), xác nhận kích hoạt quá trình apoptosis. Nói chung, những kết quả này cho thấy rằng sự kích hoạt quá trình chết chết im lặng gây ra BRDT trong các tế bào ung thư buồng trứng.
Loại bỏ BRDT do CRISPR / Cas9 gây ra ức chế mạnh sự tiến triển của tế bào ung thư buồng trứng
Để khẳng định thêm vai trò của BRDT trong tế bào ung thư buồng trứng, chúng tôi đã sử dụng chiến lược CRISPR / Cas9. Như đã mô tả, hai cấu trúc CRISPR / Cas9-BRDT-KO ngoại vi, với các sgRNA khác nhau (“sgRNA-1 / -2”), được chuyển nạp riêng lẻ sang các tế bào CaOV3. Sau khi chọn lọc các tế bào ổn định puromycin được thiết lập. Phân tích BRDT mRNA và biểu hiện protein trong các tế bào ổn định xác nhận rằng BRDT đã bị cạn kiệt hoàn toàn bởi cấu trúc CRISPR / Cas9 (Hình 4A ). Đáng kể, trong tế bào CaOV3, BRDT KO ức chế mạnh khả năng sống của tế bào (MTT OD, Hình 4B ). Sự kết hợp BrdU (Hình 4C ) và tỷ lệ hạt nhân dương EdU (Hình 4D) đã giảm trong tế bào BRDT-KO CaOV3, cho thấy sự ức chế tăng sinh. Kết quả xét nghiệm “Transwell”, Hình 4E , chứng minh rằng sự di chuyển của tế bào CaOV3 phần lớn bị ức chế với BRDT KO.
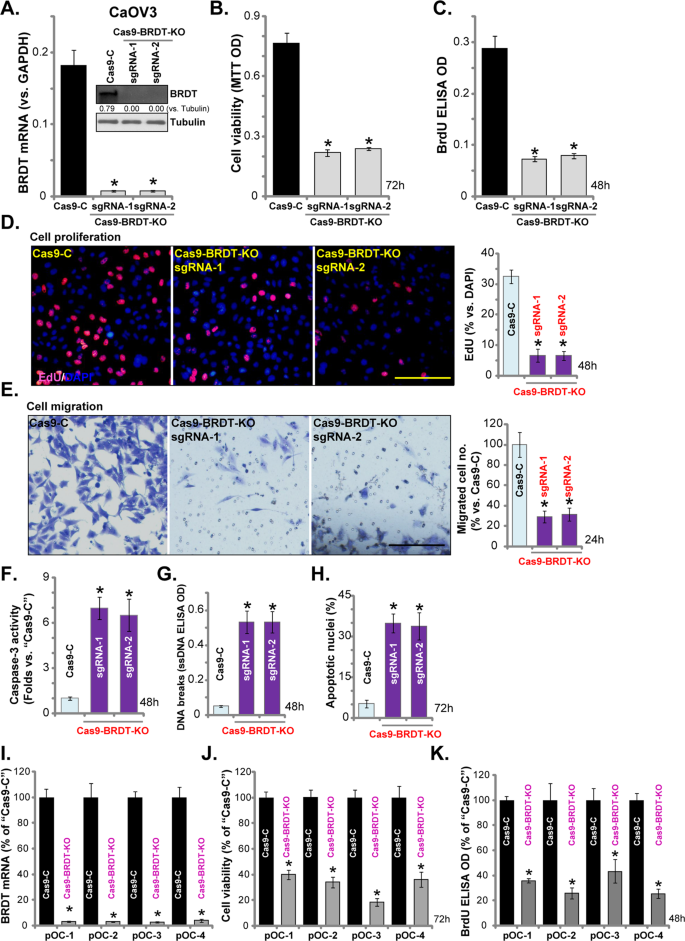
Tế bào CaOV3 ( A – H ) hoặc tế bào ung thư buồng trứng nguyên phát ở người (“pOC-1 / -2 / -3 / -4”) ( I – K ) được truyền với cấu trúc CRISPR / Cas9-BRDT-KO (với “ sgRNA-1 / -2 ”) hoặc cấu trúc kiểm soát CRISPR / Cas9 (“ Cas9-C ”), với sự chọn lọc bởi các tế bào ổn định puromycin đã được thiết lập. BRDT mRNA hoặc biểu hiện protein đã được hiển thị ( A và I ); Khả năng tồn tại của tế bào (MTT OD, B và J ) và sự tăng sinh (kết hợp BrdU và xét nghiệm nhuộm EdU, C , D và K ), cũng như sự di chuyển của tế bào (xét nghiệm “Transwell”, E) đã được kiểm chứng. Quá trình kích hoạt Caspase ( F ), hàm lượng DNA sợi đơn (ssDNA) ( G ) cũng như quá trình chết rụng tế bào (nhuộm Hoechst 333342, H ) đã được kiểm tra. Đối với mỗi thử nghiệm, n = 5 (năm đĩa hoặc giếng). * P <0,05 so với ô “Cas9-C”. Các thí nghiệm trong hình này được lặp lại ba lần, với các kết quả tương tự. Thang đo = 100 μm ( D và E ).
Các nghiên cứu bổ sung đã chứng minh rằng BRDT KO do CRISPR / Cas9 gây ra làm tăng hoạt động của caspase-3 (Hình 4F ) và gây ra đứt gãy DNA (tích tụ ssDNA, Hình 4G ). Hơn nữa, sự hoạt hóa apoptosis đáng kể đã được phát hiện trong các tế bào BRDT KO CaOV3, bằng chứng là tỷ lệ nhân apoptosis tăng lên (Hình 4H ).
Trong các tế bào ung thư buồng trứng nguyên phát ở người (“pOC-1 / -2 / -3 / -4”), sự chuyển nạp cấu trúc vi rút CRISPR / Cas9-BRDT-KO (với “sgRNA-1”) đã làm cạn kiệt mRNA BRDT (Hình 4I ) , do đó dẫn đến giảm khả năng sống (Hình 4J ) và ức chế tăng sinh (Hình. 4K ). Do đó, tương tự như kết quả shRNA, BRDT KO ức chế mạnh sự tiến triển của tế bào ung thư buồng trứng trong ống nghiệm.
BRDT biểu hiện quá mức thúc đẩy sự gia tăng và di cư của ung thư buồng trứng
Dựa trên những kết quả này, chúng tôi đưa ra giả thuyết rằng BRDT bộc lộ quá mức có thể thúc đẩy sự phát triển của tế bào ung thư buồng trứng. Để kiểm tra giả thuyết này, một cấu trúc biểu hiện BRDT siêu vi khuẩn (“LV-BRDT”) đã được chuyển sang các tế bào CaOV3. Puromycin được áp dụng một lần nữa để chọn hai dòng tế bào ổn định (“sL-1 / sL-2”). Thử nghiệm biểu hiện mRNA BRDT bằng qPCR, xác nhận rằng trong các tế bào ổn định LV-BRDT, mức BRDT mRNA tăng hơn 10 lần (so với các tế bào kiểm soát có vector trống / “LV-C”) (Hình 5A ). Mức protein BRDT cũng tăng lên (Hình 5A ). Như đã trình bày, sự biểu hiện quá mức của BRDT ngoại sinh làm tăng khả năng tồn tại của tế bào CaOV3 (Hình 5B ) và sự tăng sinh (bằng cách ghi lại tỷ lệ hạt nhân dương tính với EdU, Hình 5C). BRDT biểu hiện quá mức cũng thúc đẩy sự di chuyển của tế bào CaOV3, được kiểm tra bằng các xét nghiệm “Transwell” (Hình. 5D ) Những kết quả này khẳng định thêm rằng BRDT đóng một vai trò thiết yếu trong sự tiến triển của tế bào ung thư buồng trứng.
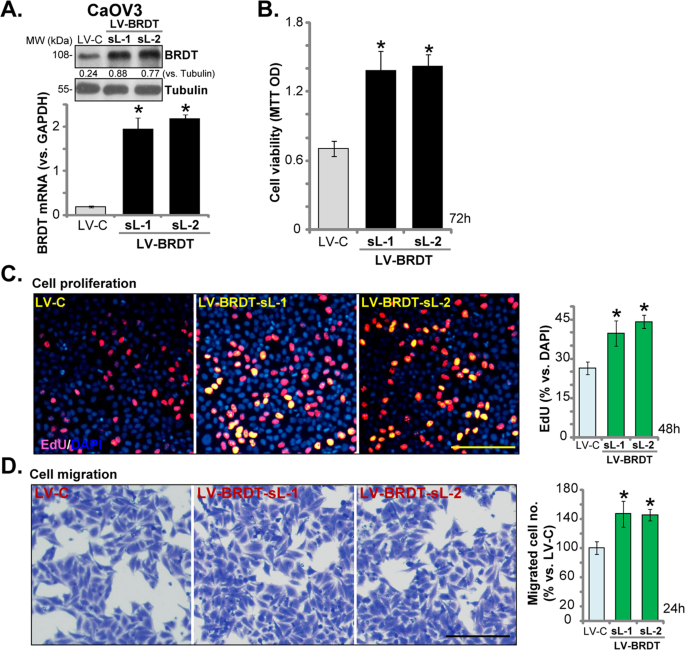
Các tế bào CaOV3 được truyền với cấu trúc biểu hiện BRDT của virut (“LV-BRDT”) hoặc vectơ trống (“LV-C”), các tế bào ổn định được chọn bởi puromycin. BRDT mRNA và biểu hiện protein ( A ), khả năng tồn tại của tế bào (MTT OD, B ), sự tăng sinh (bằng cách ghi lại tỷ lệ hạt nhân dương tính với EdU, C ) và sự di cư (xét nghiệm “Transwell”, D ) được thử nghiệm tương tự. Biểu hiện protein BRDT được định lượng và chuẩn hóa thành Tubulin ( A ). Đối với mỗi thử nghiệm, n = 5 (năm đĩa hoặc giếng). * P <0,05 so với ô “LV-C”. Các thí nghiệm trong hình này được lặp lại ba lần, với các kết quả tương tự. Thanh thang đo = 100 μm ( C và D).
Hoạt động của tế bào chống ung thư buồng trứng do suy giảm BRDT có liên quan đến sự điều hòa giảm PLK1-AURKC
Người ta đã chỉ ra rằng BRDT cần thiết cho quá trình phiên mã và biểu hiện của PLK1 và AURKC 11 , cả hai đều là các gen gây ung thư hoặc tiền ung thư quan trọng 13 , 21 , 27 . Trong các tế bào CaOV3 ổn định có BRDT-shRNA (“shBRDT-1 / -2”, xem Hình 2 ) hoặc cấu trúc CRISPR / Cas9-BRDT-KO (“sgRNA-1”, xem Hình 4 ), mRNA và biểu hiện protein của PLK1 và AURKC được điều chỉnh giảm đáng kể (Hình 6A, B ). Ngược lại, BRDT bộc lộ quá mức trong tế bào CaOV3 (xem Hình 5 ) làm tăng đáng kể sự biểu hiện PLK1 và AURKC (cả mRNA và protein) (Hình 6C, D). Những kết quả này cho thấy BRDT thực sự quan trọng đối với sự biểu hiện PLK1 và AURKC trong tế bào ung thư buồng trứng.
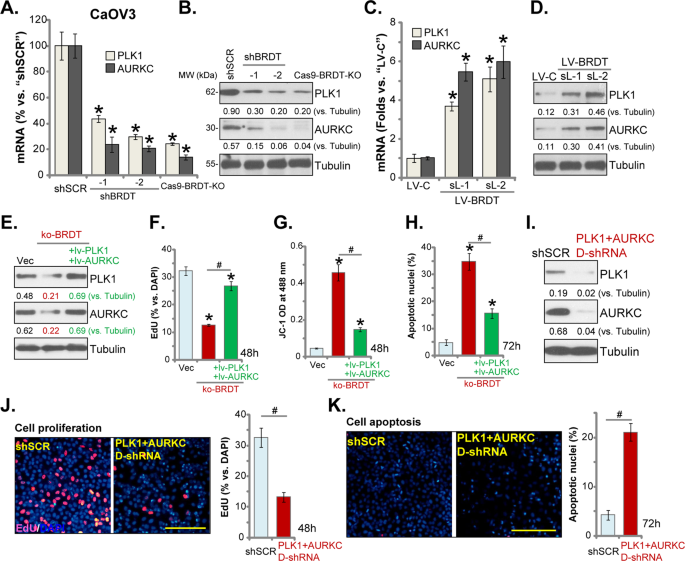
Các biểu hiện mRNA và protein của các gen được liệt kê trong các tế bào CaOV3 ổn định, với shRNA BRDT siêu vi khuẩn (“shBRDT-1 / -2”), cấu trúc CRISPR / Cas9-BRDT-KO ngoại vi (“sgRNA-1”), hoặc cấu trúc Cấu trúc biểu hiện BRDT của lentiviral (“LV-BRDT”), đã được kiểm tra bằng các xét nghiệm qPCR ( A và C ) và Western blotting ( B và D ). Các ô CaOV3 ổn định thể hiện cấu trúc CRISPR / Cas9-BRDT-KO (với các ô “sgRNA-1”, “ko-BRDT”) được truyền thêm có hoặc không có mã hóa lentivirus PLK1 và AURKC (“+ lv-PLK1 + lv-AURKC” ), các tế bào kiểm soát có vectơ trống (“Vec”), biểu hiện của các protein được liệt kê đã được hiển thị ( E ); Các tế bào được nuôi cấy thêm trong các khoảng thời gian được áp dụng, tăng sinh tế bào (ghi lại tỷ lệ hạt nhân dương tính với EdU,F ), khử cực ti thể (cường độ đơn phân màu xanh lá cây JC-1, G ) và quá trình chết rụng (ghi lại tỷ lệ hạt nhân chết, H ) đã được kiểm tra bằng các xét nghiệm thích hợp. Các tế bào CaOV3 đã được lây nhiễm bằng virut shRNA kiểm soát tranh giành (“shSCR”) hoặc PLK1 shRNA lentivirus cộng với virut AURKC shRNA (“PLK1 + AURKC D-shRNA”) trong 24 giờ, các tế bào ổn định được chọn bằng puromycin. Biểu hiện của các protein được liệt kê đã được hiển thị ( I ). Các tế bào được nuôi cấy thêm trong các khoảng thời gian được áp dụng, sự tăng sinh tế bào ( J ) và quá trình tự chết ( K ) được kiểm tra bằng phương pháp nhuộm EdU và các xét nghiệm nhuộm nhân apoptotic, tương ứng. Đối với mỗi thử nghiệm, n = 5 (năm đĩa hoặc giếng). * P <0,05 so với ô “shSCR” / “Vec”. # P <0,05. Sự biểu hiện của các protein được liệt kê đã được định lượng và chuẩn hóa thành Tubulin. Các thí nghiệm trong hình này được lặp lại ba lần, với các kết quả tương tự. Thang đo = 100 μm ( J và K ).
Để kiểm tra mối liên hệ giữa hoạt động tế bào chống ung thư buồng trứng do suy giảm BRDT và quá trình điều hòa PLK1-AURKC, các tế bào BRDT-KO CaOV3 được tiếp tục lây nhiễm với mã hóa lentivirus PLK1 và AURKC (“+ lv-PLK1 + lv-AURKC”). Tế bào ổn định được thiết lập với sự chọn lọc puromycin. Như đã trình bày, biểu hiện protein PLK1 và AURKC đã được khôi phục bởi hai cấu trúc trong tế bào BRDT-KO CaOV3 (Hình 6E ). Các nghiên cứu chức năng đã chứng minh rằng ức chế tăng sinh do BRDT-KO gây ra (tỷ lệ EdU giảm, Hình 6F ), khử cực ty thể (tăng cường độ xanh JC-1, Hình 6G ) và quá trình chết rụng tế bào (tăng tỷ lệ nhân apoptotic, Hình 6H ) là chủ yếu. giảm dần với biểu hiện lại PLK1 và AURKC (Hình 6F – H). Do đó, điều hòa PLK1-AURKC phải là cơ chế chính của hoạt động chống tế bào ung thư buồng trứng do suy giảm BRDT. Tuy nhiên, biểu hiện quá mức duy nhất của PLK1 hoặc AURKC chỉ hơi suy yếu ức chế sự tăng sinh BRDT-KO gây ra (Hình. S1A ) và apoptosis kích hoạt (Hình. S1B ) trong các tế bào CaOV3. Tác dụng giải cứu do biểu hiện quá mức đơn trong các tế bào ko-BRDT yếu hơn đáng kể so với biểu hiện quá mức kép (Hình 6F – H ).
Để hỗ trợ thêm cho giả thuyết của chúng tôi, các tế bào CaOV3 đã được đồng truyền nhiễm với mã hóa lentivirus PLK1 shRNA và AURKC shRNA. Các tế bào ổn định lại đạt được: cụ thể là các tế bào “PLK1 + AURKC D-shRNA”. Như đã thể hiện, sự biểu hiện của protein PLK1 và AURKC được điều chỉnh giảm đáng kể trong các tế bào CaOV3 với “PLK1 + AURKC D-shRNA” (Hình 6I ), nơi ức chế tăng sinh đáng kể (giảm tỷ lệ EdU hạt nhân, Hình 6J ) và quá trình chết (Hình 6K ) được phát hiện.
Đáng chú ý, sự hạ gục đơn lẻ của PLK1 hoặc AURKC do shRNA gây ra chỉ gây ra sự ức chế tăng sinh nhẹ (bằng cách ghi lại tỷ lệ hạt nhân dương tính EdU, Hình S1C ) và kích hoạt apoptosis (Hình S1D ). Quan trọng là, PLK1 cộng với AURKC đánh bật kép (“D-shRNA”) – hoạt động của tế bào kháng CaOV3 gây ra mạnh hơn so với đánh gục đơn (Hình S1C, D ), nhưng yếu hơn BRDT KO (Hình. S1C, D ). Những kết quả này ngụ ý rằng các mục tiêu protein khác, ngoài PLK1 hoặc AURKC, cũng nên tham gia vào sự tiến triển của tế bào ung thư buồng trứng qua trung gian BRDT. Kết quả xét nghiệm qPCR, Hình S1E , đã chứng minh sự biểu hiện của mRNA mục tiêu trong tế bào CaOV3 với các chỉnh sửa gen được áp dụng.
BRDT im lặng ức chế sự phát triển xenograft ung thư buồng trứng ở chuột SCID
Để nghiên cứu tác động tiềm tàng của BRDT trong sự phát triển của tế bào ung thư buồng trứng in vivo, kiểm soát tế bào CaOV3 (“Cas9-C”) và BRDT-KO (với “sgRNA-1”) tế bào CaOV3 đã được cấy vào chuột SCID để tạo thành các mô tế bào dưới da . Kết quả đường cong phát triển khối u, Hình 7A , chứng minh rằng xenografts có nguồn gốc từ tế bào BRDT-KO CaOV3 phát triển chậm hơn đáng kể so với khối u đối chứng (được hình thành bởi tế bào Cas9-C). Bằng cách tính toán sự phát triển khối u ước tính hàng ngày, sử dụng công thức [khối lượng khối u ở Ngày-35 (D35) trừ khối lượng khối u ở Ngày-0 (D0)] / 35, chúng tôi cho thấy rằng sự phát triển khối u BRDT-KO CaOV3 bị ức chế đáng kể (Hình. 7B ). Tại D35 khối u của hai nhóm được phân lập và cân bằng. Như đã chứng minh, khối u BRDT-KO CaOV3 nhẹ hơn đáng kể so với khối u đối chứng (Hình 7C). Mặt khác, trọng lượng cơ thể chuột không khác biệt đáng kể giữa hai nhóm (Hình 7D ). Không có dấu hiệu đáng chú ý về độc tính rõ ràng. Những kết quả này cho thấy BRDT-KO ức chế đáng kể sự phát triển của tế bào CaOV3 in vivo.
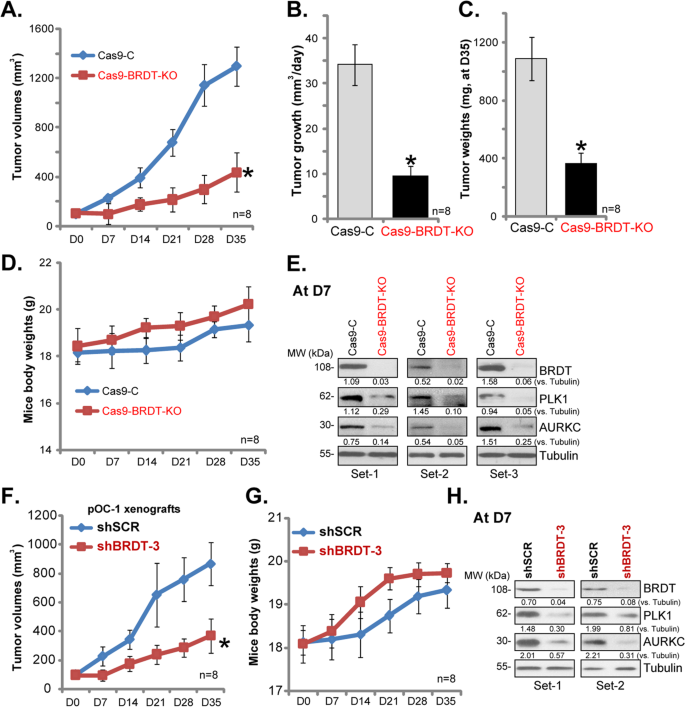
Những con chuột SCID đã được tiêm sc với các tế bào đối chứng và BRDT-KO CaOV3 (5 × 10 6 tế bào trong 100 μL DMEM cộng với 100 μL Matrigel, không có huyết thanh) ở hai bên sườn bên phải, trong vòng 3 tuần các xenografts được thiết lập (Ngày-0, “ D0 ”). Thể tích khối u ( A ) và trọng lượng cơ thể chuột ( B ) được ghi lại sau mỗi bảy ngày trong tổng số 35 ngày; Sự phát triển khối u ước tính hàng ngày đã được tính toán ( C ); Tại D35, tất cả các khối u đều được phân lập và có trọng số ( D ). Tại D7, ba khối u của mỗi nhóm được phân lập và các mô ly giải được thực hiện các xét nghiệm thấm phương Tây đối với các protein được liệt kê ( E ). Những con chuột SCID được tiêm tế bào ung thư buồng trứng nguyên phát pOC-1 (5 × 10 6tế bào trong 100 μL DMEM cộng với 100 μL Matrigel, không có huyết thanh) ở hai bên sườn bên phải. Trong vòng 3 tuần, các chương trình bài ngoại đã được thiết lập (Ngày-0, “D0”). Những con chuột sau đó được tiêm vào trong khoang miệng của virut BRDT shRNA (“shBRDT-3”) hoặc virut shRNA kiểm soát (shSCR). Sau đó, thể tích khối u ( F ) và trọng lượng cơ thể chuột ( G ) được ghi lại sau mỗi 7 ngày; Ở Ngày-7 / D7, hai khối u của mỗi nhóm được phân lập và các mô ly giải được thực hiện các xét nghiệm thấm phương Tây ( H ). Biểu hiện protein được liệt kê đã được định lượng và chuẩn hóa thành Tubulin ( E và H ). n = 8 con chuột mỗi nhóm * P <0,05 so với khối u “Cas9-C” / “shSCR”.
Để kiểm tra sự thay đổi tín hiệu, tại D7, ba khối u của mỗi nhóm được phân lập và các mô ly giải được phân tích để tìm các protein truyền tín hiệu. Như đã trình bày, BRDT đã cạn kiệt trong bản sao BRDT-KO CaOV3 (Hình 7E ), trong đó sự biểu hiện PLK1 và AURKC đã giảm đáng kể (Hình 7E ). Những kết quả báo hiệu in vivo này phù hợp với những phát hiện in vitro.
Để hỗ trợ thêm vai trò của BRDT trong sự phát triển của tế bào ung thư buồng trứng in vivo, các tế bào ung thư buồng trứng nguyên phát, pOC-1, đã được tiêm vào hai bên sườn của chuột SCID, tạo thành các bản sao pOC-1 trong vòng 3 tuần. Sau đó, những con chuột được phân ngẫu nhiên thành hai nhóm, được tiêm vào trong khoang miệng của BRDT shRNA lentivirus (“shBRDT-3”) hoặc shRNA lentivirus kiểm soát (shSCR). Khi ghi lại sự phát triển của khối u, chúng tôi nhận thấy rằng tiêm shBRDT-3 ức chế mạnh sự phát triển xenograft pOC-1 ở chuột (Hình 7F ), nhưng không ảnh hưởng đến trọng lượng cơ thể chuột (Hình 7G ). Ở Ngày-7 (D7), hai khối u của mỗi nhóm được phân lập và các mô ly giải được thực hiện các xét nghiệm thấm phương Tây. Kết quả xác nhận BRDT im lặng trong các khối u được tiêm shBRDT-3 (Hình 7H), với điều chỉnh giảm PLK1 và AURKC được quan sát (Hình 7H ). Những kết quả này chỉ ra rằng BRDT rất quan trọng đối với sự phát triển của tế bào ung thư buồng trứng in vivo.
Thảo luận
BRDT là động cơ thúc đẩy biểu hiện gen meiotic và hậu meiotic 6 , 28 . BRDT liên kết với các lysine đã acetyl hóa để điều chỉnh các quá trình biểu sinh, cần thiết cho sự hình thành cấu trúc nhiễm sắc trong quá trình nguyên phân 6 . Hơn nữa, BRDT thu nhận yếu tố kéo dài phiên mã dương tính b (p-TEFb), điều chỉnh sự kéo dài phiên mã và biểu hiện của một số protein quan trọng 6 , bao gồm PLK1 và AURKC 11 . Biểu hiện BRDT cao gấp ba lần được phát hiện ở tinh hoàn trưởng thành so với biểu hiện ở tinh hoàn phôi 29 , 30 . Biểu hiện BRDT có tương quan với sự tăng hydro hóa histone H4 trong quá trình hình thành tinh trùng 29 , 30. Ở những bệnh nhân có quá trình sinh tinh bất thường, ít hoặc không có biểu hiện BRDT được phát hiện trong tinh hoàn 29 , 30 . Các nghiên cứu gần đây đã chỉ ra rằng BRDT được kích hoạt trở lại và biểu hiện trong các bệnh ung thư khác nhau ở người, bao gồm ung thư phổi không phải tế bào nhỏ (NSCLC), ung thư biểu mô tế bào vảy ở đầu và cổ (HNSCC) và ung thư biểu mô tế bào vảy thực quản, nhưng không phải trong khối u ác tính hoặc ung thư ruột kết, vú, thận và bàng quang 6 , 28 , 30 . Cơ sở dữ liệu proteomicsdb và kết quả của chúng tôi trong các mô người đã xác nhận rằng BRDT được biểu hiện trong các mô buồng trứng.
Kết quả của chúng tôi ở đây cho thấy BRDT có thể là một gen gây ung thư quan trọng và là mục tiêu điều trị của ung thư buồng trứng. Biểu hiện của nó được điều chỉnh đáng kể trong các mô ung thư buồng trứng và trong các tế bào ung thư buồng trứng nguyên phát ở người (CaOV3) / nguyên phát. Tuy nhiên, biểu hiện BRDT thấp được phát hiện trong các mô và tế bào biểu mô buồng trứng. Trong các tế bào ung thư buồng trứng, loại trực tiếp BRDT shRNA hoặc CRISPR-Cas9 ức chế mạnh sự phát triển, tồn tại, tăng sinh và di cư của tế bào, trong khi kích hoạt quá trình apoptosis. Ngược lại, sự bộc lộ quá mức của BRDT bắt buộc làm tăng sinh và di cư tế bào CaOV3. Điều quan trọng là, khối u xenograft BRDT-KO CaOV3 phát triển chậm hơn đáng kể so với khối u đối chứng. Hơn nữa, tiêm virut BRDT shRNA lentivirus vào trong cơ ức chế mạnh mẽ sự phát triển của xenograft pOS-1 ở chuột SCID.
PLK1 đóng một vai trò thiết yếu trong việc điều chỉnh sự tiến triển của chu kỳ tế bào 12 . Nó được yêu cầu đối với một số quá trình của chu kỳ tế bào, bao gồm cả quá trình nhập phân bào và điểm kiểm tra G2 / M, sự phối hợp tâm thể, sự lắp ráp trục quay và sự phân ly của nhiễm sắc thể 12 . PLK1 cũng thực hiện các chức năng chính tại vùng giữa của trục chính trong quá trình abscission, tạo điều kiện thuận lợi cho việc sao chép DNA và tạo tế bào 12 . Do đó, nó rất quan trọng đối với sự tiến triển chu kỳ tế bào và tăng sinh tế bào 12 . Các nghiên cứu đã chỉ ra hoạt động gây ung thư của PLK1 biểu hiện quá mức trong ung thư buồng trứng 21 , 27 , điều này quan trọng đối với sự tiến triển của tế bào ung thư và độ bền hóa học 21 , 27. Ngoài ra, AURKC, một gen khác được điều chỉnh bởi BRDT, được kích hoạt lại và biểu hiện quá mức trong nhiều tế bào ung thư khác nhau ở người 13 , rất cần thiết cho các hành vi ung thư, bao gồm tăng sinh và di chuyển tế bào 13 . AURKC có thể thúc đẩy sự phát triển của khối u xenograft 13 . AURKC chết Kinase ức chế sự tăng sinh tế bào HeLa, trong khi AURKC hoạt động tích cực thúc đẩy sự tiến triển của tế bào ung thư 31 , 32 , 33 .
Kết quả của nghiên cứu hiện tại cho thấy PLK1 và AURKC được biểu hiện trong các tế bào ung thư buồng trứng. Đáng chú ý là cả hai đều bị BRDT shRNA hoặc KO điều chỉnh giảm, nhưng được điều chỉnh tăng lên với biểu hiện quá mức BRDT ngoài tử cung. Điều hòa giảm PLK1 và AURKC cũng được phát hiện trong các mô khối u BRDT-KO CaOV3 và trong xenografts pOS-1 có tiêm BRDT shRNA. Điều quan trọng là, hoạt động chống lại tế bào ung thư buồng trứng do BRDT-KO gây ra phần lớn bị suy giảm khi tái biểu hiện PLK1 và AURKC. PLK1 cộng với AURKC ức chế tăng sinh gây im lặng kép và kích hoạt apoptosis trong tế bào CaOV3, bắt chước các hành động gây im lặng BRDT. Do đó, sự tiến triển của tế bào ung thư buồng trứng qua trung gian BRDT có liên quan đến việc điều chỉnh biểu hiện PLK1 và AURKC. Các cơ chế chi tiết có thể đảm bảo các đặc điểm khác.
Phần kết luận
Các phương pháp điều trị ung thư buồng trứng hiện nay, với sự kết hợp của hóa trị liệu dựa trên bạch kim và phẫu thuật, chỉ có thể mang lại tỷ lệ sống sót tổng thể trong 5 năm là gần 45%. Tỷ lệ này giảm xuống 25% đối với các bệnh ung thư tiến triển 34 . Tỷ lệ sống sót kém nêu bật những hạn chế trong hiểu biết sinh học về căn bệnh quái ác này 35 , 36 , 37 , 38 . Do đó, việc xác định các chiến lược điều trị mới / các mục tiêu phân tử 35 , 36 , 37 , 38 là cấp thiết . Các nghiên cứu bộ gen gần đây đã chứng minh sự thay đổi rộng rãi của các chất điều hòa biểu sinh trong ung thư buồng trứng, có thể được sử dụng làm cơ sở để phát triển các loại thuốc biểu sinh mới35 , 36 , 37 , 38 . Kết quả của chúng tôi chỉ ra rằng sự biểu hiện quá mức của BRDT thúc đẩy sự tiến triển của tế bào ung thư buồng trứng in vitro và in vivo. Nhắm mục tiêu BRDT có thể là một chiến lược mới để điều trị ung thư buồng trứng.
-
Người giới thiệu
- 1.Smith, RA, Cokkinides, V. & Brawley, OW Tầm soát ung thư ở Hoa Kỳ, 2009: đánh giá về các hướng dẫn hiện tại của Hiệp hội Ung thư Hoa Kỳ và các vấn đề trong tầm soát ung thư. Ung thư CA J. Clin. 59 , 27–41 (2009).
Bài báo Google Scholar
- 2.Siegel, RL, Miller, KD & Jemal, A. Thống kê Ung thư, 2017. CA Cancer J. Clin. 67 , 7–30 (2017).
Bài báo Google Scholar
- 3.Matulonis, UA và cộng sự. Ung thư buồng trứng. Nat. Rev. Dis. Nghiêm trang. 2 , 16061 (2016).
Bài báo Google Scholar
- 4.Nielsen, FC, van Overeem Hansen, T. & Sorensen, CS Ung thư vú và buồng trứng di truyền: các gen mới trong các con đường hạn chế. Nat. Rev. Cancer 16 , 599–612 (2016).
CAS Bài báo Google Scholar
- 5.Groen, RS, Gershenson, DM & Fader, AN Cập nhật và các liệu pháp mới cho các bệnh ung thư buồng trứng biểu mô hiếm gặp: một kích thước không còn phù hợp với tất cả. Gynecol. Oncol. 136 , 373–383 (2015).
Bài báo Google Scholar
- 6.Bourova-Flin, E., Chuffart, F., Rousseaux, S. & Khochbin, S. Vai trò của yếu tố đặc hiệu bromodomain testis, BRDT, trong ung thư: một dấu ấn sinh học và một mục tiêu điều trị khả dĩ. Ô J. 19 , 1–8 (2017).
PubMed PubMed Central Google Scholar
- 7.Fensterle, J., Aicher, B., Seipelt, I., Teifel, M. & Engel, J. Quan điểm hiện tại về cơ chế hoạt động của perifosine trong ung thư. Đại lý chống ung thư Med. Chèm. 14 , 629–635 (2014).
CAS Bài báo Google Scholar
- số 8.Radin, NS Tiêu diệt tế bào ung thư bằng cách làm tăng nồng độ ceramide của nhiều loại thuốc: một giả thuyết đã đến lúc? Eur. J. Hóa sinh. 268 , 193–204 (2001).
CAS Bài báo Google Scholar
- 9.Fu, LL và cộng sự. Ức chế BET bromodomains như một chiến lược điều trị để khám phá thuốc điều trị ung thư. Oncotarget 6 , 5501–5516 (2015).
Bài báo Google Scholar
- 10.Shi, J. & Vakoc, CR Các cơ chế đằng sau hoạt động điều trị của sự ức chế BET bromodomain. Mol Ô. 54 , 728–736 (2014).
CAS Bài báo Google Scholar
- 11.Matzuk, MM và cộng sự. Sự ức chế phân tử nhỏ của BRDT để tránh thai cho nam giới. Tế bào 150 , 673-684 (2012).
CAS Bài báo Google Scholar
- 12.Liu, Z., Sun, Q. & Wang, X. PLK1, một mục tiêu tiềm năng cho liệu pháp điều trị ung thư. Bản dịch. Oncol. 10 , 22–32 (2017).
Bài báo Google Scholar
- 13.Quartuccio, SM & Schindler, K. Chức năng của aurora kinase C trong bệnh meiosis và ung thư. Trước mặt. Nhà phát triển tế bào. Biol. 3 , 50 (2015).
Bài báo Google Scholar
- 14.Yang, YL và cộng sự. Sự ức chế sphingosine kinase-1 làm nhạy cảm sự ức chế tăng trưởng và quá trình chết rụng do curcumin gây ra ở các tế bào ung thư buồng trứng. Khoa học ung thư. 103 , 1538–1545 (2012).
CAS Bài báo Google Scholar
- 15.Minjie, S., Defei, H., Zhimin, H., Weiding, W. & Yuhua, Z. Nhắm mục tiêu tế bào ung thư tuyến tụy bằng chất ức chế histone deacetylase (HDAC) dựa trên hydroxamate ST-3595. Biol khối u. 36 , 9015–9022 (2015).
Bài báo Google Scholar
- 16.Lv, H. và cộng sự. Đánh giá tiền lâm sàng của ceramide liposomal C8 như một chất chống ung thư biểu mô tế bào gan mạnh. PLoS ONE 11 , e0145195 (2016).
Bài báo Google Scholar
- 17.Wang, SS và cộng sự. Triptonide ức chế sự phát triển của tế bào ung thư biểu mô vòm họng ở người thông qua việc phá vỡ tín hiệu Lnc-RNA THOR-IGF2BP1. Chữ cái ung thư. 443 , 13–24 (2019).
CAS Bài báo Google Scholar
- 18.Yang, L. và cộng sự. Ceramide C6 giúp tăng cường đáng kể sự ức chế phát triển docetaxel gây ra và quá trình chết rụng ở các tế bào ung thư vú được nuôi cấy: một nghiên cứu về cơ chế. Hết hạn. Tế bào Res. 332 , 47–59 (2015).
CAS Bài báo Google Scholar
- 19.Brooks, MM, Neelam, S., Fudala, R., Gryczynski, I. & Cammarata, PR Bảo vệ ty thể dạng thấu kính. Phần A: theo dõi sự khử cực của ty thể với JC-1 và huỳnh quang tạo tác bằng chất ức chế glycogen synthase kinase-3beta, SB216763. Mol Lượt xem 19 , 1406–1412 (2013).
CAS PubMed PubMed Central Google Scholar
- 20.Zhang, X. và cộng sự. microRNA-9 nhắm mục tiêu chọn lọc LMX1A để thúc đẩy sự tiến triển của tế bào ung thư dạ dày. Hóa sinh. Lý sinh. Res. Commun. 505 , 405–412 (2018).
CAS Bài báo Google Scholar
- 21.Guo, P., Xiong, X., Zhang, S. & Peng, D. miR-100 tái kích ứng ung thư buồng trứng biểu mô kháng với cisplatin. Oncol. Đại diện. 36 , 3552-3558 (2016).
CAS Bài báo Google Scholar
- 22.Zhang, D., Xia, H., Zhang, W. & Fang, B. Hoạt động chống ung thư buồng trứng của WYE-132, một chất ức chế kép mTORC1 / 2. Biol khối u. 37 , 1327–1336 (2016).
CAS Bài báo Google Scholar
- 23.Fu, M., Shi, W., Li, Z. & Liu, H. Kích hoạt con đường apoptosis ty thể phụ thuộc mPTP bằng một chất resminostat ức chế HDAC chảo mới trong tế bào ung thư biểu mô tế bào gan. Hóa sinh. Lý sinh. Res. Commun. 477 , 527–533 (2016).
CAS Bài báo Google Scholar
- 24.Fu, M., Wan, F., Li, Z. & Zhang, F. 4SC-202 kích hoạt con đường apoptosis ty thể phụ thuộc ASK1 để ức chế các tế bào ung thư biểu mô tế bào gan. Hóa sinh. Lý sinh. Res. Commun. 471 , 267–273 (2016).
CAS Bài báo Google Scholar
- 25.Porter, AG & Janicke, RU Vai trò mới nổi của caspase-3 trong quá trình apoptosis. Cell Death Differ. 6 , 99–104 (1999).
CAS Bài báo Google Scholar
- 26.Riedl, SJ & Shi, Y. Cơ chế phân tử điều hòa caspase trong quá trình apoptosis. Nat. Linh mục Mol. Biol tế bào. 5 , 897–907 (2004).
CAS Bài báo Google Scholar
- 27.Chan, KK và cộng sự. Tác động của iASPP đối với tính kháng hóa học thông qua PLK1 và quá trình tự động trong ung thư biểu mô tế bào rõ buồng trứng. Int. J. Cancer 143 , 1456–1469 (2018).
CAS Bài báo Google Scholar
- 28.Scanlan, MJ và cộng sự. Biểu hiện của kháng nguyên ung thư-tinh hoàn trong ung thư phổi: định nghĩa của gen đặc hiệu bromodomain testis (BRDT) là một gen CT mới, CT9. Chữ cái ung thư. 150 , 155–164 (2000).
CAS Bài báo Google Scholar
- 29.Jones, MH, Numata, M. & Shimane, M. Nhận dạng và đặc điểm của BRDT: Một gen đặc hiệu cho tinh hoàn liên quan đến các gen bromodomain RING3 và Drosophila fsh. Genomics 45 , 529–534 (1997).
CAS Bài báo Google Scholar
- 30.Zheng, Y., Yuan, W., Zhou, Z., Xu, M. & Sha, JH Nhân bản phân tử và biểu hiện của một biến thể mối nối thay thế mới của gen BRDT. Int. J. Mol. Med. 15 , 315–321 (2005).
CAS PubMed Google Scholar
- 31.Khan, J. và cộng sự. Sự biểu hiện quá mức của Aurora-C kinase hoạt động dẫn đến biến đổi tế bào và hình thành khối u. PLoS ONE 6 , e26512 (2011).
CAS Bài báo Google Scholar
- 32.Tsou, JH và cộng sự. AURKC được biểu hiện một cách khác thường giúp tăng cường sự biến đổi và tính khối u của các tế bào biểu mô. J. Pathol. 225 , 243–254 (2011).
CAS Bài báo Google Scholar
- 33.Spengler, D. Aurora-C-T191D là một đột biến aurora-C hiếu động. Chu kỳ ô 6 , 1803–1804 (2007).
CAS Bài báo Google Scholar
- 34.Siegel, RL, Miller, KD & Jemal, A. Số liệu thống kê về ung thư, 2018. CA Cancer J. Clin. 68 , 7–30 (2018).
Bài báo Google Scholar
- 35.Nick, AM, Coleman, RL, Ramirez, PT & Sood, AK Một khuôn khổ cho phương pháp phẫu thuật được cá nhân hóa đối với bệnh ung thư buồng trứng. Nat. Linh mục Clin. Oncol. 12 , 239–245 (2015).
CAS Bài báo Google Scholar
- 36.Markman, M. Hóa trị: Hạn chế sử dụng đường trong phúc mạc đối với ung thư buồng trứng-tại sao? Nat. Linh mục Clin. Oncol. 12 , 628–630 (2015).
CAS Bài báo Google Scholar
- 37.Coleman, RL, Monk, BJ, Sood, AK & Herzog, TJ Nghiên cứu mới nhất và điều trị ung thư buồng trứng biểu mô giai đoạn tiến triển. Nat. Linh mục Clin. Oncol. 10 , 211–224 (2013).
CAS Bài báo Google Scholar
- 38Vaughan, S. và cộng sự. Suy nghĩ lại về ung thư buồng trứng: các khuyến nghị để cải thiện kết quả. Nat. Rev. Cancer 11 , 719–725 (2011).
CAS Bài báo Google Scholar
Tải xuống tài liệu tham khảo
Sự nhìn nhận
Công việc này đã được hỗ trợ một cách hào phóng bởi các khoản tài trợ từ Quỹ Khoa học Tự nhiên Trung Quốc (81902715), Quỹ Khoa học Tự nhiên tỉnh Giang Tô (BK20180195) và Chương trình Nghiên cứu Khoa học cho Tài năng Trẻ của Tổng công ty Hạt nhân Quốc gia Trung Quốc (Shang Cai, 51003) bởi Các Tài năng Y tế Trẻ Giang Tô ( Số tài trợ QNRC2016180), và Dự án Sáu đỉnh cao nhân tài của tỉnh Giang Tô (WSN-173). Các nhà tài trợ không có vai trò gì trong việc thiết kế nghiên cứu, thu thập và phân tích dữ liệu, quyết định xuất bản hoặc chuẩn bị bản thảo.
Thông tin tác giả
Ghi chú của tác giả- Các tác giả này đóng góp ngang nhau: Ling Chen, Shang Cai
Chi nhánh
- Khoa bệnh lý, Bệnh viện Tháp Trống Nam Kinh, Bệnh viện trực thuộc Trường Y Đại học Nam Kinh, Nam Kinh, Trung Quốc
Ling Chen & Jing-mei Wang
- Khoa Xạ trị và Ung thư, Bệnh viện trực thuộc thứ hai của Đại học Soochow, Tô Châu, Trung Quốc
Thương Cai
- Khoa Sản và Phụ khoa, Bệnh viện Côn Sơn trực thuộc Đại học Giang Tô, 215300, Côn Sơn, Giang Tô, Trung Quốc
Ying-ying Huai & Qian Chu
- Khoa Ung thư Y tế, Bệnh viện Nhân dân Vô Tích thuộc Đại học Y Nam Kinh, Vô Tích, Trung Quốc
Pei-Hua Lu
Các tác giả tương ứng
Thư từ Pei-Hua Lu hoặc Qian Chu .
- 1.Smith, RA, Cokkinides, V. & Brawley, OW Tầm soát ung thư ở Hoa Kỳ, 2009: đánh giá về các hướng dẫn hiện tại của Hiệp hội Ung thư Hoa Kỳ và các vấn đề trong tầm soát ung thư. Ung thư CA J. Clin. 59 , 27–41 (2009).