Một loại thuốc ung thư mới thu nhỏ khối u khó điều trị
Các loại thuốc mới được gọi là liên hợp thuốc kháng thể giúp bệnh nhân ung thư từng không điều trị được
TÁC GIẢ JYOTI MADHUSOODANAN

TôiTrong cuộc tìm kiếm lâu dài và thường nản lòng để chữa bệnh ung thư, sự chấp thuận năm 1998 của thuốc Herceptin là một khoảnh khắc vô cùng hy vọng. Thuốc điều trị ung thư vú này là loại thuốc đầu tiên sử dụng protein đặc hiệu khối u làm đèn hiệu dẫn đường để tìm và tiêu diệt tế bào ung thư. Và nó đã hoạt động. Herceptin đã mang lại lợi ích cho gần ba triệu người kể từ thời điểm đó, làm tăng đáng kể tỷ lệ sống sót sau 10 năm và tỷ lệ không bị ung thư đối với những gì đã từng là một trong những chẩn đoán y tế tồi tệ nhất. “Thành thật mà nói, nó đã gây chấn động trái đất”, bác sĩ ung thư Sara M. Tolaney thuộc Viện Ung thư Dana-Farber ở Boston nói.
Nhưng thuốc có một hạn chế lớn. Đèn hiệu của Herceptin là một protein gọi là HER2 và nó hoạt động tốt nhất cho những người có khối u được thúc đẩy phát triển bởi tín hiệu HER2 – nhưng đó chỉ là khoảng một phần năm bệnh nhân ung thư vú. Đối với 80% còn lại trong số khoảng 250.000 người được chẩn đoán mắc bệnh mỗi năm ở Mỹ, Herceptin không mang lại lợi ích gì.
Việc săn lùng các phương pháp điều trị tốt hơn đã khiến các nhà nghiên cứu hình dung lại các liệu pháp nhắm mục tiêu. Đến năm 2022, họ đã phát triển một loại thuốc liên kết Herceptin với một loại thuốc tiêu diệt ung thư khác. Liệu pháp này, lần đầu tiên, có thể làm hỏng các khối u có nồng độ HER2 thấp. Loại thuốc này, được đặt tên là Enhertu, kéo dài cuộc sống của những người bị ung thư vú thêm vài tháng, đôi khi lâu hơn. Và nó đã làm như vậy với ít tác dụng phụ nghiêm trọng hơn so với hóa trị liệu tiêu chuẩn. Cục Quản lý Thực phẩm và Dược phẩm Hoa Kỳ đã phê duyệt việc sử dụng nó trong năm đó.
Tin tức thậm chí còn tốt hơn vào năm 2023. Các nhà nghiên cứu báo cáo rằng Enhertu dường như hoạt động ngay cả trên các khối u dường như không có HER2 nào cả. (Có thể các bệnh ung thư đã có protein nhưng ở mức rất thấp thoát khỏi các phương pháp phát hiện tiêu chuẩn.) “Thật thú vị!”, bác sĩ ung thư Shanu Modi thuộc Trung tâm Ung thư Memorial Sloan Kettering (MSK) ở thành phố New York, người đã giúp thực hiện nghiên cứu dẫn đến sự chấp thuận của Enhertu, nói. “Họ đã thực hiện thử nghiệm khiêu khích này và thấy tỷ lệ đáp ứng gần 30% này” trong các khối u dường như thiếu protein ung thư, cô lưu ý.
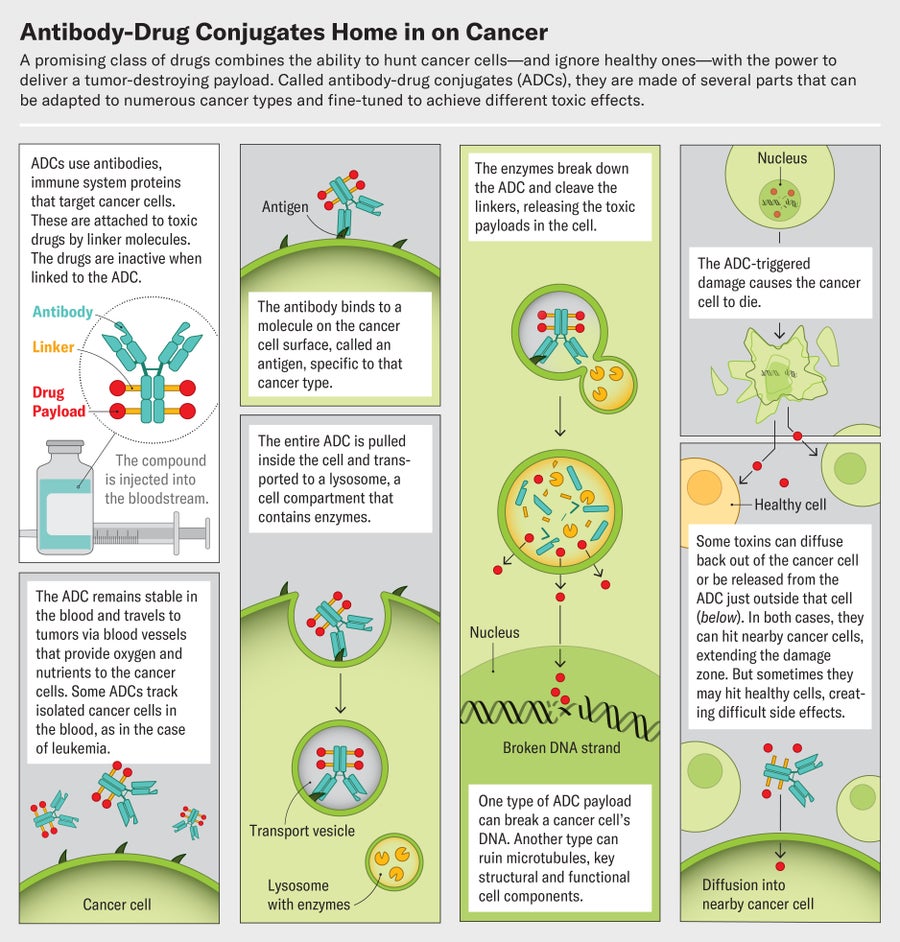
Enhertu thuộc về một nhóm thuốc ung thư nhắm mục tiêu khéo léo và đang phát triển được gọi là liên hợp thuốc kháng thể, hoặc ADC. Các hợp chất được xây dựng xung quanh một kháng thể đặc biệt, một protein hệ thống miễn dịch tập trung vào các phân tử có nhiều trên các tế bào ung thư. Kháng thể được liên kết với một trọng tải độc hại, một loại thuốc giết chết các tế bào đó. Ái lực của ADC đối với ung thư có nghĩa là nó tránh được các tế bào khỏe mạnh, tránh được nhiều tác dụng phụ của hóa trị liệu truyền thống. Và mỗi kháng thể có thể được kết hợp với một số loại thuốc khác nhau. Việc lắp ráp giống như Lego này mở ra một thế giới của các khả năng trộn và kết hợp. Các nhà nghiên cứu có thể sử dụng cùng một loại thuốc để điều trị nhiều bệnh ung thư bằng cách chuyển đổi kháng thể, hoặc họ có thể tấn công một loại khối u với nhiều ADC khác nhau nhắm vào một số dấu ấn sinh học ung thư trên các tế bào. Khả năng này “thay đổi cách chúng ta nghĩ về phát triển thuốc”, Tolaney nói.
Ý tưởng về ADC không hoàn toàn mới – ý tưởng đầu tiên được phép sử dụng cho bệnh nhân vào năm 2000 – nhưng gần đây các nhà khoa học đã học được các kỹ thuật xây dựng hóa học phức tạp làm cho các hợp chất hiệu quả hơn nhiều và họ đã xác định được các mục tiêu mới dành riêng cho bệnh ung thư. Những tiến bộ này đã thúc đẩy một làn sóng phát triển mới. Mười bốn ADC đã được phê duyệt cho các bệnh ung thư vú, bàng quang, buồng trứng, máu và các bệnh ung thư khác. Khoảng 100 người khác đang trong đường ống tiền lâm sàng. Một ADC cho ung thư vú, được gọi là T-DM1, đã chứng minh hiệu quả hơn nhiều so với Herceptin và hiện đã trở thành tiêu chuẩn chăm sóc cho giai đoạn đầu của bệnh. “Thật tuyệt khi thấy mọi thứ đã thay đổi nhanh chóng như thế nào,” Tolaney nói. Phấn khởi trước những thành công, các nhà nghiên cứu và các công ty dược phẩm đang đổ nguồn lực vào việc phát triển các ADC mạnh hơn – thậm chí có thể hoạt động trên nhiều loại ung thư. Những gã khổng lồ dược phẩm như Gilead, Roche và BioNTech đã đầu tư rất nhiều vào các chương trình ADC của họ; Chẳng hạn, vào tháng 10/2023, Merck đã đầu tư 4 tỷ USD vào quan hệ đối tác với Daiichi Sankyo, công ty công nghệ sinh học hợp tác với AstraZeneca để sản xuất Enhertu.
Nhưng các loại thuốc mới vẫn bị bao vây bởi một số vấn đề bí ẩn. Một số ADC có tác dụng phụ tương tự như các liệu pháp hóa trị truyền thống – điều này không nên xảy ra, bởi vì các loại thuốc được cho là chỉ nhắm vào các tế bào ung thư. Trên các diễn đàn bệnh nhân, mọi người mô tả cần phải giảm liều vì buồn nôn hoặc mệt mỏi không thể chịu đựng được. Những hạn chế này hạn chế việc sử dụng ADC, vì vậy các nhà khoa học và công ty dược phẩm đang khẩn trương cố gắng tìm ra nguyên nhân gây ra chúng.
Trong thử nghiệm lâm sàng dẫn đến sự chấp thuận của Enhertu, bệnh nhân thường đã nhận được các loại thuốc hóa trị khác nhau, chẳng hạn như thuốc ngăn chặn tế bào nhân lên. Nhưng những loại thuốc này và các hình thức hóa trị khác không phân biệt giữa tế bào ung thư và tế bào khỏe mạnh. Bất kỳ tế bào nào cố gắng tạo ra DNA hoặc nhân lên đều dễ bị tổn thương, và mô bình thường cũng như khối u có thể bị tấn công. 64% những người dùng hóa trị tiêu chuẩn trải qua buồn nôn, tiêu chảy, mệt mỏi và các tác dụng phụ tiêu cực khác. Đối với nhiều người, những điều này có thể gây suy nhược như chính bệnh ung thư. Những tác dụng như vậy hạn chế liều lượng mọi người có thể dùng và thời gian điều trị, để lại cơ hội cho các khối u phát triển kháng thuốc và phục hồi.
Trong nhiều năm, các nhà nghiên cứu đã tìm kiếm các lựa chọn thay thế ít độc hại hơn, hình dung các loại thuốc chính xác nhắm vào ung thư và dự phòng các tế bào khỏe mạnh. Ý tưởng về ADC xuất phát từ tính đặc hiệu tinh tế của kháng thể. Nếu các hình thức hóa trị có độc tính cao có thể được gắn vào kháng thể, độc tố sẽ chỉ đến được các tế bào ung thư và không có các tế bào khác. Mặc dù khái niệm này rất đơn giản, nhưng những nỗ lực chế tạo ADC đã chững lại trong nhiều thập kỷ.
Một số nỗ lực sớm nhất đã sử dụng ma túy không đủ mạnh. Ví dụ, vào những năm 1950, các nhà nghiên cứu đã liên kết một loại thuốc có tên methotrexate với một kháng thể nhắm vào kháng nguyên carcinoembryonic, một dấu hiệu khối u phổ biến và kiểm tra xem cấu trúc này có thể điều trị ung thư đại trực tràng và buồng trứng tiến triển ở người hay không. Thuốc liên kết với mục tiêu của nó nhưng có ít hiệu quả điều trị. Các nhà nghiên cứu sau đó đã đi quá xa đến đầu kia của quang phổ và thay vào đó cố gắng sử dụng các loại thuốc độc hại hơn nhiều. Nhưng những loại thuốc này đã gây ra tác dụng phụ nghiêm trọng.
Greg Thurber, một kỹ sư hóa học tại Đại học Michigan, đã xem xét câu hỏi hóc búa này. Ông bắt đầu nghiên cứu ADC khi nghiên cứu cách các kháng thể lây lan qua cơ thể để liên kết với mục tiêu của chúng. Sau khi ADC xâm nhập vào một khối u thông qua mạng lưới các mạch máu của nó, các hợp chất trượt ra khỏi các mạch này và vào các tế bào ung thư để tiêu diệt chúng, Thurber nói. Nhưng các ADC tồn tại vào thời điểm đó không bao giờ vượt qua các tế bào ngay bên ngoài các mạch máu. Họ trói quá chặt. Chìa khóa để cải thiện hiệu quả, hóa ra, là điều chỉnh các bộ phận kháng thể để chúng tập trung vào các tế bào ung thư nhưng có độ bám đủ lỏng để một số trượt vào bên trong khối u. “Rất nhiều người trong lĩnh vực này có một khái niệm rất đơn giản – chúng tôi đưa một loại thuốc hóa trị vào một kháng thể, nó nhắm mục tiêu nó vào tế bào ung thư và nó sẽ tránh các mô khỏe mạnh”, Thurber nói. “Đó hoàn toàn không phải là cách chúng hoạt động trong thực tế.”
Mày mò với thành phần thuốc của ADC, cũng như kháng thể, cuối cùng đã dẫn đến một điểm ngọt ngào giết chết ung thư. Năm 2013, FDA bật đèn xanh T-DM1 cho bệnh ung thư vú. Kháng thể của nó là trastuzumab (“T” trong T-DM1), cùng một kháng thể được sử dụng trong Herceptin. Thuốc gắn liền với kháng thể này rất đáng chú ý vì nó quá nguy hiểm để tự sử dụng. Được gọi là emtansine, ban đầu nó được phát hiện vào những năm 1970 nhưng bị gác lại vì nó quá độc đối với quá nhiều tế bào. Tuy nhiên, được kết hợp với nhau dưới dạng T-DM1, thuốc và kháng thể thường tránh xa các tế bào khỏe mạnh và được chứng minh là một sự kết hợp mạnh mẽ và chính xác.
Vào đầu những năm 2000, Modi đã giúp tiến hành thử nghiệm T-DM1 – mang nhãn hiệu Kadcyla của nhà sản xuất Genentech – ở những người mắc một căn bệnh đặc biệt khó khăn: ung thư vú dương tính với HER2 tiến triển đã di căn khắp cơ thể. Chỉ những người đã hết các lựa chọn điều trị khác mới được ghi danh. Modi nói: “Chúng tôi đang tiếp nhận những người trong một số trường hợp thực sự muốn đến nhà tế bần. Tuy nhiên, “hầu hết mọi bệnh nhân đăng ký dùng loại thuốc đó đều nhận được lợi ích. Nó thực sự rất thỏa mãn.”
Trong một thử nghiệm khác với khoảng 1.500 người mắc bệnh ung thư vú giai đoạn đầu, một phân tích dữ liệu tạm thời được công bố vào năm 2019, ước tính rằng 88% những người nhận được T-DM1 sẽ không bị ung thư ba năm sau đó, so với chỉ 77% những người nhận được T-DM1. riêng Herceptin. Modi cho biết loại thuốc này đã được chứng minh là “có tác dụng mạnh hơn hầu hết các liệu pháp mà chúng tôi đang áp dụng cho bệnh nhân và nó có liên quan đến mức độ an toàn tốt hơn”.
Thành công của Kadcyla trong việc chống lại những căn bệnh ung thư khó điều trị không chỉ thay đổi cuộc sống của một số bệnh nhân. Nó thúc đẩy sự nhiệt tình – và có lẽ quan trọng hơn là cả đô la của ngành dược phẩm – vào ý tưởng về ADC. Giờ đây, các nhà nghiên cứu biết rằng khi được ghép lại với nhau một cách chính xác, có thể nạp vào kháng thể những loại thuốc quá độc để có thể sử dụng theo cách khác mà vẫn tạo ra một loại thuốc có tác dụng tốt hơn hóa trị liệu truyền thống.
Một số ADC được thiết kế tương tự đã được phê duyệt cho một loạt các loại ung thư khác nhau. Nhiều người trong số này mang các loại thuốc ức chế enzyme topoisomerase 1, rất cần thiết cho sự sao chép DNA. Giống như emtansine, loại thuốc được sử dụng trong Kadcyla, các chất ức chế topoisomerase mới hơn quá độc để được sử dụng làm thuốc độc lập nhưng ít gây hại hơn khi chúng bị hạn chế phần lớn ở các tế bào khối u. Và bản thân Kadcyla, sau khi được chứng minh là làm chậm hoặc ngăn chặn ung thư vú giai đoạn cuối, đang được thử nghiệm trên những bệnh nhân mắc bệnh giai đoạn rất sớm để xem liệu điều trị tại thời điểm đó có thể không chỉ làm chậm ung thư mà còn thực sự chữa khỏi nó hay không. Thành công của nó “là chất xúc tác để tiếp tục thăm dò”, Modi nói. “Chúng ta có thể xây dựng dựa trên điều này không? Chúng ta có thể làm tốt hơn nữa không?”
Kiểm tra các bản tin khác của chúng tôi
DOing tốt hơn, hóa ra, liên quan đến việc thiết kế các phân tử liên kết tốt liên kết kháng thể với thuốc. Những cấu trúc nhỏ bé này hoạt động như các tác nhân hóa học. Chúng phải duy trì hoàn toàn ổn định cho đến khi đạt được mục tiêu, sau đó tách khỏi kháng thể để xả tải trọng của chúng vào khối u. Một số nỗ lực sớm nhất trong việc tạo ra ADC đã thất bại không phải vì kháng thể hoặc thuốc của chúng mà là kết quả của các liên kết không ổn định.
ADC hiện đại dựa trên hai loại liên kết. Một loại vẫn không bị phá vỡ ngay cả khi ADC đạt được mục tiêu của nó. Loại khác, được gọi là liên kết có thể phân tách, là các hóa chất phá vỡ để đáp ứng với các tín hiệu rất cụ thể, chẳng hạn như các enzyme có nhiều trong khối u, trong không gian giữa các tế bào ung thư riêng lẻ. Khi ADC nằm trong ranh giới của khối u, các enzyme này sẽ tách liên kết và giải phóng tải trọng thuốc.
Các liên kết có thể phân tách đang cho thấy những lợi thế ấn tượng và hơn 80% các ADC hiện được phê duyệt hiện đang sử dụng chúng. Một ADC với một liên kết không thể phân tách sẽ chỉ giết chết tế bào mà nó gắn vào, nhưng một ADC tách ra có thể đặt các phân tử thuốc gần các tế bào khối u lân cận và tiêu diệt chúng. Cái gọi là hiệu ứng người ngoài cuộc này có thể làm cho các loại thuốc hiệu quả hơn nhiều, Thurber nói.
Enhertu, ví dụ, sử dụng cùng một kháng thể như Kadcyla nhưng với một liên kết có thể phân tách (Kadcyla sử dụng một phiên bản không thể phân tách) và một loại thuốc khác. Mỗi kháng thể Enhertu mang khoảng tám phân tử thuốc, so với khoảng ba phân tử trên mỗi kháng thể ở Kadcyla. Trong một nghiên cứu gần đây, các nhà nghiên cứu đã so sánh tác dụng của hai loại thuốc này ở những người bị ung thư vú dương tính với HER2. Enhertu là người chiến thắng rõ ràng. Nó đã ngăn chặn sự phát triển của khối u trong hơn hai năm trung bình, trong khi Kadcyla đã làm như vậy chỉ trong sáu tháng. “Đó là một trận lở đất về mặt nó tốt hơn bao nhiêu,” Tolaney nói. “Đó là một ví dụ thực sự tốt đẹp về cách công nghệ ADC dẫn đến sự khác biệt đáng kể về kết quả.”
Hiệu ứng người ngoài cuộc cũng giải thích, một phần, tại sao Enhertu có hiệu quả chống lại các khối u hầu như không có HER2: một khi ADC xâm nhập vào khối u và các phân tử thuốc tách ra, chúng có thể tiêu diệt các tế bào khối u lân cận ngay cả khi những người ngoài cuộc đó không mang nhiều HER2 trên bề mặt của chúng. Hành động này, cùng với việc sử dụng xét nghiệm chẩn đoán có thể bỏ lỡ mức HER2 cực thấp, có thể giải thích kết quả từ thử nghiệm trong đó thuốc dường như hoạt động trên các khối u không có HER2. Thử nghiệm đó sử dụng một xét nghiệm được gọi là xét nghiệm IHC. Nó thường được sử dụng để phân loại ung thư là HER2 dương tính hoặc âm tính, không phải để đo lượng protein có mặt. Kết quả âm tính thường có nghĩa là 10% hoặc ít hơn các tế bào của khối u có HER2 trên bề mặt của chúng. Tuy nhiên, 10% có thể đủ để thu hút một vài hạt Enhertu, và hiệu ứng người ngoài cuộc có thể đủ để tiêu diệt các tế bào khối u, Modi nói.
Enhertu không phải là ADC duy nhất hoạt động theo cách này. Trong một nghiên cứu năm 2022, các nhà nghiên cứu phát hiện ra rằng Trodelvy, một ADC nhắm vào một protein bề mặt được gọi là TROP2, dường như hiệu quả hơn hóa trị liệu tiêu chuẩn đối với những người bị ung thư vú ba âm tính di căn, một căn bệnh đặc biệt khó điều trị. Trodelvy tốt hơn bất kể TROP2 được phát hiện nhiều hay ít trên các khối u. “Điều đó, đối với tôi, thật hoang dã,” Tolaney nói. “Chúng tôi rất vui mừng về điều đó bởi vì những bệnh ung thư này đang có những lợi ích [rõ ràng] mà không có mục tiêu.”
Thế hệ ADC mới này đang tạo ra sự khác biệt trong các loại ung thư khác trước đây được cho là khó chữa, chẳng hạn như ung thư bàng quang di căn. Vào năm 2021, FDA đã phê duyệt Trodelvy và một ADC khác có tên Padcev để điều trị căn bệnh này. Trong 30 năm, tiêu chuẩn chăm sóc cho loại ung thư bàng quang này chỉ là hóa trị, bác sĩ ung thư David J. Benjamin, người điều trị ung thư sinh dục tiết niệu tại Viện Ung thư Gia đình Hoag ở miền nam California cho biết. “Bây giờ chúng tôi có nhiều phương pháp điều trị mới, và hai trong số đó là liên hợp kháng thể-thuốc”, Benjamin nói. Trong các thử nghiệm lâm sàng cho bệnh nhân ung thư bàng quang tiến triển, Padcev kết hợp với một loại thuốc kích thích hệ thống miễn dịch thu nhỏ khối u hoặc ngăn chặn sự phát triển của chúng ở hơn 60% số người. Trong một con số khổng lồ 30 phần trăm những người nhận được sự kết hợp hai loại thuốc, ung thư của họ hoàn toàn biến mất – một thành công chưa từng có.
Nhưng ngay cả những ADC mới hơn cũng không phải là không có vấn đề. Hiệu ứng người ngoài cuộc, làm cho chúng rất hiệu quả, có thể lây lan đủ xa từ khối u để ảnh hưởng đến các tế bào khỏe mạnh, gây rụng tóc, buồn nôn, tiêu chảy, mệt mỏi và các tác dụng phụ khác tương tự như bụi phóng xạ của hóa trị trường học cũ. ADC cũng có liên quan đến một loạt các vấn đề về mắt, từ viêm kết mạc đến mất thị lực nghiêm trọng.
Một lời giải thích khác cho những tác động khó chịu này là không có mục tiêu protein nào dành riêng cho các tế bào ung thư. Những protein này, còn được gọi là kháng nguyên, có nhiều hơn trong các bệnh ung thư nhưng có thể xuất hiện trong các tế bào bình thường. Điều đó làm cho một số liên kết của ADC với các tế bào khỏe mạnh là không thể tránh khỏi. “Tôi không thể nghĩ ra bất kỳ ví dụ nào về kháng nguyên đặc hiệu khối u thực sự”, Matthew Vander Heiden, một nhà sinh học phân tử tại Viện Koch thuộc Viện Công nghệ Massachusetts cho biết. Hơn nữa, ADC, giống như bất kỳ loại thuốc hoặc kháng thể nào khác, cuối cùng được ăn và chuyển hóa bởi các tế bào không ung thư. Quá trình này phân mảnh chúng thành những mảnh nhỏ hơn, giải phóng thuốc tải trọng từ các liên kết của chúng và kích hoạt các phản ứng.
Tuy nhiên, khả năng tách ADC ra và tinh chỉnh các thành phần của chúng – điều không thể thực hiện được với các phương pháp điều trị truyền thống – mang đến cho các nhà nghiên cứu cơ hội tìm ra các phiên bản có ít tác dụng phụ hơn và nhiều lợi thế hơn. Hiện tại, hầu hết các ADC được sử dụng ở liều tối đa mà một người có thể dung nạp. Điều đó có thể không đúng với các phiên bản trong tương lai. Khi phát triển một loại thuốc, cho dù đó là thuốc giảm đau đơn giản, hóa trị hay ADC, các nhà nghiên cứu bắt đầu bằng cách tìm ra liều thấp nhất mà thuốc có hiệu quả. Sau đó, họ tìm ra liều cao nhất mà mọi người có thể nhận được một cách an toàn. Khoảng cách giữa hai liều đó, được gọi là cửa sổ trị liệu, thường nhỏ. Nhưng khả năng hoán đổi các thành phần cung cấp cho các nhà nghiên cứu ADC nhiều con đường để mở rộng nó. Cuối cùng, các nhà sản xuất thuốc có thể tạo ra ADC hiệu quả đến mức bệnh nhân không bao giờ cần dùng liều cao nhất có thể chấp nhận được – liều thấp hơn nhiều sẽ loại bỏ khối u mà không tạo ra hậu quả không lường trước như buồn nôn hoặc rụng tóc.
Chuyển từ các loại thuốc dựa trên hóa trị liệu độc hại như tải trọng cũng có thể làm giảm tác dụng phụ. Ví dụ, một số ADC được phê duyệt gần đây liên kết các kháng thể với các loại thuốc có thể kích hoạt hệ thống miễn dịch của chính cơ thể để tấn công các tế bào ung thư thay vì dựa vào các hóa chất đầu độc tế bào. Ngoài ra, các nhà khoa học đang khám phá các cách để đưa xạ trị trực tiếp đến các khối u bằng cách buộc các kháng thể với đồng vị phóng xạ. Joshua Z. Drago, một bác sĩ ung thư tại Trung tâm Ung thư MSK, nói rằng với loại liên kết phù hợp, ADC “về mặt lý thuyết có thể cung cấp bất kỳ loại thuốc phân tử nhỏ nào”.
Cuối cùng, các thành phần được kết hợp lại và cải tiến có thể dẫn đến loại hoán đổi mà bệnh nhân ung thư thực sự quan tâm: trao đổi bệnh của họ để chữa bệnh.