Sử dụng APP model chưa bệnh Alzheimer bằng Zinc Nuclear

Bài viết gốc: https://journals.plos.org/plosone/article?id=10.1371%2Fjournal.pone.0075493&fbclid=IwAR2UsxScTN_WyfhNbsFL8sw42oUkfMrh90gPaszs9fIjtuTQgsKJS4MYNk8
Trừu tượng
Hạt nhân ngón tay kẽm (ZFN), nổi tiếng với khả năng sửa đổi chính xác và hiệu quả các locus gen cụ thể, đã được sử dụng trong nhiều sinh vật mô hình chuyển gen và cấu trúc tế bào. Ở đây, chúng tôi sử dụng công nghệ ZFN, với sự tái tổ hợp tương đồng (HR), để xây dựng các tế bào gõ protein Amyloid tiền chất (APP) đặc hiệu theo trình tự. Với việc sử dụng ZFN, chúng tôi đã thiết lập APP gõ vào các dòng tế bào với hiệu suất chỉnh sửa gen khoảng 7%. Chúng tôi đã điện hóa đoạn DNA có chứa chất khởi động và vùng mã hóa protein của các hạt nhân ngón tay kẽm vào tế bào, thay vì các plasmid, để tránh các vấn đề liên quan đến tái tổ hợp tương đồng mục tiêu và áp dụng một cặp miền phân tách FokI bị đột biến để làm giảm tác dụng độc hại của FokI. các ZFN về tăng trưởng tế bào. Vì biểu hiện quá mức của APP hoặc tên miền phụ của nó, có thể dẫn đến một hiệu ứng gây chết người ngay lập tức, chúng tôi đã sử dụng Hệ thống Cre-LoxP để điều chỉnh biểu thức APP. Các dòng tế bào biến đổi gen của chúng tôi, w5c1 và s12c8, cho thấy sản xuất APP và Amyloid β (Aβ) có thể phát hiện được. Đột biến kép của Thụy Điển trong chuỗi mã hóa APP đã tăng cường sự phong phú của APP và Aβ. Hơn nữa, hoạt động của ba giai đoạn quan trọng trong sự hình thành Aβ có thể được điều chỉnh, chỉ ra rằng các tế bào chuyển gen này có khả năng sàng lọc thuốc để sửa đổi chuyển hóa amyloid trong tế bào. Các tế bào biến đổi của chúng ta có thể dễ dàng được nhân giống trong nuôi cấy và sẽ cung cấp một môi trường thử nghiệm tuyệt vời để làm sáng tỏ các khía cạnh của sinh bệnh học phân tử của bệnh Alzheimer, đặc biệt là các liên quan đến con đường amyloidogen liên quan đến đột biến trong trình tự mã hóa APP.
Số liệu
Trích dẫn: Zhang X, Li H, Mao Y, Li Z, Wang R, Guo T, et al. (2013) Mô hình ứng dụng biểu hiện quá mức cho sàng lọc thuốc chống bệnh Alzheimer được tạo ra bởi công nghệ N ngón tay kẽm. PLoS MỘT 8 (11): e75493. https://doi.org/10.1371/journal.pone.0075493
Biên tập: Christian Holscher, Đại học Lancaster, Vương quốc Anh
Nhận được: ngày 23 tháng 6 năm 2013; Được chấp nhận: ngày 17 tháng 7 năm 2013; Xuất bản: ngày 6 tháng 11 năm 2013
Bản quyền: © 2013 Zhang và cộng sự. Đây là một bài viết truy cập mở được phân phối theo các điều khoản của Giấy phép ghi nhận tác giả Creative Commons, cho phép sử dụng, phân phối và tái sản xuất không hạn chế trong bất kỳ phương tiện nào, miễn là tác giả và nguồn gốc được ghi có.
Tài trợ: Nghiên cứu này được hỗ trợ bởi các khoản tài trợ từ Quỹ tài trợ khoa học tự nhiên quốc gia Trung Quốc (NSFC) 30772603, Chương trình nghiên cứu và phát triển công nghệ quan trọng quốc gia (Cấp số 2006BAF07B01, 2009BAK61B01, 2009BAK61B04? 2012BAK25B01) và tài trợ từ Quỹ khoa học quốc gia Trung Quốc – Viện nghiên cứu sức khỏe Canada (NSFC-CIHR) Sáng kiến nghiên cứu sức khỏe chung Trung Quốc-Canada (Số cấp 81061120525 và CCI-109605). Các nhà tài trợ không có vai trò trong thiết kế nghiên cứu, thu thập và phân tích dữ liệu, quyết định xuất bản hoặc chuẩn bị bản thảo.
Lợi ích cạnh tranh: Tôi đã đọc chính sách của tạp chí và có những xung đột sau đây. Gang Nui là chủ tịch và CEO của Bắc Kinh N & N Genetech Co. Điều này không làm thay đổi sự tuân thủ của các tác giả đối với tất cả các chính sách của PLOS ONE về chia sẻ dữ liệu và tài liệu.
Giới thiệu
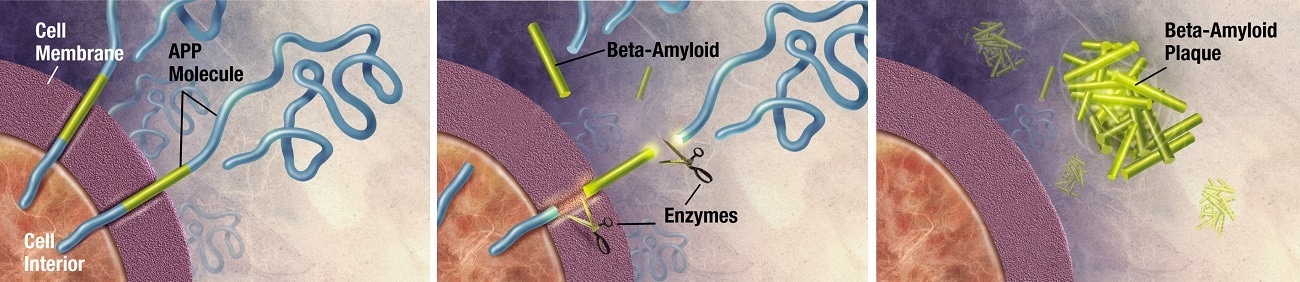
Bệnh Alzheimer (AD) là một rối loạn thoái hóa thần kinh gây ra trí nhớ tiến bộ và suy giảm nhận thức trong giai đoạn giữa đến cuối tuổi trưởng thành. Não AD được đặc trưng bởi sự lắng đọng của amyloid peptide (Aβ), được sản xuất từ protein tiền chất amyloid (APP) bởi sự phân tách liên tiếp theo chuỗi-và-secretase (phức hợp presenilin) [ 1 ]. Giả thuyết cơ bản để mô tả nguồn gốc của AD là Aβ khởi tạo một tầng độc hại gây ra AD [ 2]. Tuân thủ giả thuyết amyloid, người ta có thể dễ dàng tìm thấy một số mục tiêu tiềm năng để điều trị bệnh. Kết quả là, sự chú ý đáng kể đang được tập trung vào việc phát triển các liệu pháp điều trị cho AD hướng vào con đường trao đổi chất liên quan đến Aβ. Các can thiệp trị liệu cho AD đã được phát triển trong 20 năm qua, tuy nhiên, kết quả điều trị vẫn không đạt yêu cầu, và đã có một vài tiến bộ trong điều trị bằng thuốc mới hoặc hướng đi mới trong điều trị AD. Lý do cho sự thiếu tiến bộ một phần là do thiếu một mô hình nghiên cứu tiền lâm sàng đáng tin cậy.
Các tế bào chuyển gen là công cụ mong muốn để phát triển thuốc mới vì chúng cung cấp một hệ thống truy cập trực tiếp vào các cơ chế tế bào có thể gợi ý các mục tiêu thuốc tiềm năng mới. Với sự phát triển của các phương pháp sàng lọc thông lượng cao (HTS), việc xây dựng các mô hình tế bào chuyển gen phù hợp sẽ cho phép các nhà nghiên cứu nhanh chóng tiến hành hàng triệu xét nghiệm hóa học, di truyền hoặc dược lý [ 3 ] và các xét nghiệm này sẽ nhanh chóng xác định các hợp chất, kháng thể hoặc gen hoạt động điều đó sẽ điều chỉnh một con đường phân tử sinh học cụ thể trong sinh bệnh học AD. Các dòng tế bào có nguồn gốc từ thận hoặc não của con người, các tế bào thần kinh chính có nguồn gốc từ chuột và chuột, hoặc các tế bào biểu hiện quá mức APP hoặc presenilin nhân tạo có hoặc không có đột biến AD gia đình đã được sử dụng cho các nghiên cứu in vitro [ 4 ,5 ]. Những mô hình dòng tế bào này đã được chứng minh là công cụ tuyệt vời để sàng lọc thuốc và cho phép điều tra các cơ chế tế bào của bệnh lý AD. Tuy nhiên, trong các mô hình hiện có này, Aβ không được biểu thị ổn định hoặc được thể hiện ở mức thấp và thường khó xác định các thay đổi ngoài mục tiêu [ 4 – 6 ]. Hơn nữa, do tỷ lệ tái hợp tương đồng thấp và độ phức tạp của quá trình, có thể mất vài tháng để thiết lập các dòng tế bào này [ 7 ]. Gần đây, việc sử dụng tế bào thần kinh có nguồn gốc tế bào gốc đa năng (iPS) do con người gây ra để sàng lọc thuốc AD đã được báo cáo [ 8]. Các tế bào iPS cung cấp một công cụ mới mạnh mẽ để phát triển các phương pháp điều trị AD vì chúng có sản lượng A cao và phản ứng với các chất ức chế và điều biến điển hình của con đường amyloidogen. Tuy nhiên, các tế bào gốc đa năng đòi hỏi các quy trình phức tạp hơn nữa để thao tác và thời gian đáng kể để lựa chọn các dòng vô tính tốt nhất [ 9 ]. Ngoài ra, các tế bào iPS thậm chí không đồng nhất, với mỗi bản sao là duy nhất, do đó hạn chế khả năng sử dụng các tế bào iPS làm mô hình sàng lọc thuốc.
Các nucleases thời gian gần đây đã phát triển thiết kế ngón tay kẽm (ZFNs), một phản ứng tổng hợp khảm của một Cys 2 ông 2 protein kẽm ngón tay (ZFP) và lĩnh vực phân cắt của FokI endonuclease, được coi là nghiên cứu đáng tin cậy và các công cụ điều trị cho sửa đổi locus gen cụ thể. Mỗi Cys 2 Ngón tay 2 của anh ấy , mô-đun nhận dạng của ZFN, nhận ra khoảng 3 bp DNA [ 10 , 11], do đó, ba ngón tay của ZFN sẽ liên kết mục tiêu 9 bp, cho phép bộ điều chỉnh ZFN (loài hoạt động) xác định chuỗi DNA 18 bp làm vị trí phân tách. Sau khi thu nhỏ, các miền FokI, mô-đun phân tách của ZFN, sẽ cắt DNA tại vị trí được chọn trước, đưa các chuỗi đứt đôi (DSB) cụ thể vào trang web vào gen nội sinh được nhắm mục tiêu. Cơ chế sửa chữa DNA tế bào, được tạo ra bởi DSBs, làm tăng tỷ lệ HR lên vài bậc độ lớn. Điều chỉnh gen qua trung gian ZFN đã được áp dụng thành công ở chuột [ 12 ], chuột [ 13 ], zebrafish [ 14 – 16 ], C. Elegans [ 17 ], Drosophila [ 18 ], tế bào trứng Xenopus [ 19]] và Arabidopsis thaliana [ 20 ], đạt hiệu quả cao.
Trong nghiên cứu này, chúng tôi đã xây dựng thành công các tế bào nguyên bào sợi chuột biểu hiện quá mức APP bằng công nghệ ZFNs. Việc sử dụng ZFN mang lại hiệu quả cao trong chỉnh sửa gen qua trung gian HR với phổ giảm các thay đổi ngoài mục tiêu không mong muốn [ 6]. Các dòng tế bào chúng tôi thiết lập APP thể hiện ở mức cao và có khả năng tiết A vào môi trường nuôi cấy tế bào. Sản xuất Aβ42 bị ức chế trong các tế bào này bởi chất kích hoạt α-secretase (donepezil), chất ức chế β-secretase (galantamin) và bởi một loại thuốc chống viêm không steroid (NSAID, ibuprofen), cho thấy rằng con đường amyloidogen dự kiến sẽ tạo ra nó. Việc gõ APP đột biến trong dòng tế bào, s12c8, thể hiện tính nhạy cảm cao hơn đối với việc điều trị bằng thuốc, so với việc gõ APP hoang dã trong dòng tế bào w5c1. Các tế bào biến đổi đã được nhân giống dễ dàng trong nuôi cấy và các tế bào này sẽ cung cấp một mô hình thử nghiệm để làm sáng tỏ các khía cạnh của sinh bệnh học phân tử của AD,
Các kết quả
Xét nghiệm in vitro của hoạt động ZFN
Các ZFN đã được chuẩn bị bằng cách sử dụng Hệ thống phiên mã / dịch thuật ghép nhanh TNT® (Promega). Các protein thô được dịch đã được ủ với plasmid ZFN-TS ( Hình 1A ) chứa một đoạn DNA chứa vị trí nhắm mục tiêu ZFN trong chuột Rosa26 intron I để đánh giá hoạt động hạn chế DNA của chúng trong ống nghiệm. Điện di SDS-PAGE cho thấy kích thước của protein ZFN là 35,5KDa ( Hình 1B ) chỉ ra rằng các plasmid ZFN đã được dịch sang các protein có kích thước chính xác bởi hệ thống IVTT. Kết quả tiêu hóa của plasmid ZFN-TS được phân tích bằng phương pháp điện di trên gel agarose ( Hình 1B) trong đó một lần tiêu hóa ZFN-TS của EcoRI đã giải phóng đoạn DNA tuyến tính 3,62kb, sau đó được các protein thô ZFN tiêu hóa để giải phóng hai đoạn 0,65kb và 2,97kb cho thấy các ZFN được dịch mã tách ra ở khoảng cách mong đợi từ trang EcoRI. Để xác nhận vị trí cụ thể của vị trí phân cắt ZFN, plasmid đã được tiêu hóa bởi ZFN cũng như EcoRI và SalI tạo ra các mảnh có kích thước 0,65kb, 0,29kb và 2,68kb ( Hình 1B ) phù hợp với ZFN. trang web.
(A) Plasmid ZFN-TS, để thử nghiệm hoạt động của enzyme ZFN trong ống nghiệm. Đoạn DNA tương ứng với vị trí đích ZFN (TS) đã được sao chép vào pMD-19T để tạo thành ZFN-TS. Kích thước dự kiến của các sản phẩm được tạo ra bởi quá trình tiêu hóa ZFN-TS của ZFN và các enzyme hạn chế SalI và EcoRI được hiển thị bên dưới plasmid. (B) Xác định hoạt động ZFN. Protein ZFN được tạo ra bằng hệ thống phản ứng IVTT và được phân tích bằng điện di SDS-PAGE (trái). Lanes 1, 2 và 3 là các điều khiển T7, được dịch thành protein 61 KDa – kích thước dự kiến. Làn 4, 5 và 6 là các sản phẩm của vùng mã hóa trái ZFN (Ngõ 4), vùng mã hóa phải ZFN (Ngõ 5) và hỗn hợp của các vùng mã hóa trái và phải của ZFN (Ngõ 6). ZFN được dịch là các peptide 35,5KDa. Sản phẩm tiêu hóa ZFN-TS được xác định bằng điện di trên gel Agrose (phải). Ngõ 1 là véc tơ ZFN-TS chưa tiêu hóa; làn 2 là sự tiêu hóa của ZFN-TS bởi EcoRI; làn 3 và làn 4 được tiêu hóa kép bởi các enzyme EcoRI và ZFN, sử dụng các thứ tự tiêu hóa khác nhau (làn 3, EcoRI ZFN, làn 4, ZFN EcoRI). Ngõ 5 là tiêu hóa kép của EcoRI và SalI. Ngõ 6 là hệ thống tiêu hóa EcoRI, SalI và ZFN. Kích thước của các mảnh vỡ như mong đợi. (C) Xác định hoạt động ZFN trong các tế bào. Hoạt động ZFN tạo ra các đột biến không đồng nhất trongRosa26 intron I trong các tế bào. Phân tích trình tự được thực hiện trên 48 alen chuột nhân bản Rosa26 . Số lượng nucleotide bị xóa hoặc chèn tại vị trí đích ZFN (được gạch chân) trong mỗi bản sao được chỉ định ở bên phải của mỗi chuỗi. Không có đột biến ở Rosa26đã được quan sát trong một phân tích tương tự được thực hiện với các mẫu kiểm soát từ các ô nhận vectơ trống PMLM290 và PMLM292. (D) Chiến lược sơ đồ để tạo và xác định các dòng tế bào biểu hiện trên APP. Các tế bào đã được điện di động với ZFN và nhắm vào các plasmid và các tế bào biến đổi đã được lựa chọn theo lựa chọn với 600 năng lượng / ml G418 trong hai tuần. Sau khi hạn chế các phương pháp pha loãng, tổng số 192 dòng vô tính đơn bào (96 đột biến và 96 wildtype) đã được thu thập và phân tích để tích hợp vào vị trí mục tiêu ZFN (vị trí spacer 5bp ở giữa các vị trí nhận biết ZFN trong Rosa26 intron I) bằng phương pháp PCR, phân tích blot miền Nam bằng cách sử dụng đầu dò sp và phát hiện biểu hiện protein huỳnh quang màu xanh lá cây (GFP). Hai dòng vô tính, w5 và s12, được chọn làm các ô bị bất hoạt APP (APP gõ trong các ô nhưng không có biểu thức APP). Để kích hoạt biểu thức APP, w5 và s12 sau đó được thay thế bằng LV-CRE để tạo ra sự tái hợp và loại bỏ băng dừng. Sau khi hạn chế pha loãng, PCR và Southern Blot đã được sử dụng để kiểm tra xóa và kích hoạt APP ở cấp độ DNA. Western blot và miễn dịch huỳnh quang đã được sử dụng để kiểm tra biểu hiện APP và Aβ ở mức độ protein. Subclones w5c1 và s12c8 đã được chọn làm các tế bào biểu hiện quá mức APP.
Các đứt gãy hai sợi do ZFN gây ra được sửa chữa bằng cách nối cuối không phổ biến (NHEJ) thường dẫn đến những thay đổi không đồng nhất ở vị trí đích [ 21 ]. Chúng tôi đã sử dụng đặc tính này để điều tra xem liệu các tế bào Balb / c 3T3 có bị biến đổi với ZFN có trải nghiệm NHEJ do ZFN gây ra hay không. Tổng cộng có 48 alen Rosa26 riêng lẻ đã được giải trình tự sau khi khuếch đại từ các tế bào 48 giờ sau khi các đoạn DNA chứa trình tự khởi đầu và trình tự mã hóa ZFN được phân phối cho thấy 3 alen chứa đột biến tại vị trí đích của ZFN ( Hình 1C). Các locus bị đột biến chứa các đặc tính xóa 7 đến 27 bp và sự đa dạng chuỗi được quan sát mạnh mẽ cho thấy các tế bào Balb / c 3T3 đã được sửa đổi bởi các ZFN ( Hình 1C). Không có đột biến được phát hiện từ một nhóm đối chứng (50 alen Rosa26 riêng lẻ ), được truyền với các plasmid PMLM290 và PMLM292.
Các đoạn DNA được tuyến tính hóa chứa vùng mã hóa ZFN và bộ khởi động CMV cùng với vectơ nhắm mục tiêu APP được tuyến tính hóa ( Hình S1 ) đã được chuyển vào các tế bào, sau đó được nuôi cấy với sự hiện diện của G418 (600 Muffg / ml) trong 2 tuần để chọn lọc transfomants (2 tuần). Hình 1D ). Tổng số 192 dòng vô tính có nguồn gốc đơn bào (96 đột biến kép Thụy Điển và 96 ký tự hoang dã) đã thu được bằng cách hạn chế pha loãng và phân tích để tích hợp các chuỗi APP vào vị trí mục tiêu ZFN bằng PCR ( Hình 2 ), phân tích blot miền Nam bằng cách sử dụng đầu dò sp ( Hình 2 ) và phát hiện biểu hiện protein huỳnh quang màu xanh lá cây (GFP) ( Hình 3 ). Phân tích PCR ( Hình 2B) của các tế bào biến đổi (đối với băng biểu hiện APP bất hoạt) cho thấy hiệu quả chỉnh sửa gen là 7,2% (7/96, gõ tự nhiên) và 6,2% (6/96, APP đột biến kép của Thụy Điển gõ vào) (dữ liệu không được hiển thị) . Phân tích Nam blot ( Hình S2 ) đã xác nhận kết quả PCR. Các dòng tế bào s7, s9, s10, s12 và w5 (các dòng tế bào được dán nhãn s chứa chuỗi mã hóa APP với đột biến Thụy Điển, trong khi các dòng có w là wildtype) được tìm thấy là biến đổi gen ở cả hai nhiễm sắc thể (nghĩa là tích hợp băng cassette APP thành cả hai alen nhiễm sắc thể). Nội dung GFP và nội địa hóa, được phát hiện trực tiếp bằng kính hiển vi huỳnh quang, với kết quả cho các dòng tế bào w5 và s12 được hiển thị trong Hình 3. So sánh cường độ huỳnh quang cho thấy các dòng tế bào w5 và s12 cho thấy cường độ lớn hơn các dòng tế bào khác được kiểm tra (kết quả không được hiển thị).
(A) Vị trí bộ gen của mồi PCR và đầu dò blot phía Nam cho cấu trúc biểu hiện APP bị bất hoạt và kích hoạt. Sơ đồ minh họa các cấu trúc nhắm mục tiêu với vị trí của các đoạn mồi được sử dụng để phát hiện các sự kiện tái hợp. Để xác định các sự kiện tái tổ hợp trong các dòng tế bào biểu hiện APP không hoạt động, chúng tôi sử dụng cặp mồi primer1 và primer2. Các tế bào có sự kiện tái tổ hợp ở cả hai nhiễm sắc thể sẽ có các sản phẩm PCR có kích thước dự kiến sau: primer1: 0 bp; mồi2: 215 bp; Trong các tế bào có sự kiện tái tổ hợp chỉ ở một trong hai nhiễm sắc thể thì các sản phẩm PCR sẽ có các kích thước dự kiến sau: primer1: 204 bp; mồi2: 215 bp; Trong các tế bào không có sự kiện tái tổ hợp, các sản phẩm PCR sẽ có kích thước dự kiến là: prim1: 204 bp; mồi2: 0 bp; Để phát hiện xóa băng dừng trong các dòng ô biểu hiện APP đã kích hoạt, chúng tôi sử dụng primer cặpprimer3 và primer4. Trong các tế bào có sự kiện tái tổ hợp ở cả hai nhiễm sắc thể thì các sản phẩm PCR sẽ có các kích thước dự kiến sau: primer3: 0 bp; mồi4: 216 bp; Trong các tế bào có sự kiện tái tổ hợp chỉ có một trong hai nhiễm sắc thể thì các sản phẩm PCR sẽ có các kích thước dự kiến sau: primer3: 801 bp; mồi4: 216 và 2516 bp; Trong các tế bào không có sự kiện tái tổ hợp, các sản phẩm PCR sẽ có kích thước dự kiến: primer3: 801 bp; mồi4: 2516 bp. (B) phân tích PCR các dòng tế bào biểu hiện APP bất hoạt / kích hoạt bằng cách sử dụng cặp mồi primer1, primer2, primer3 và primer4. Kết quả sử dụng cặp mồi primer1, primer2, primer3 và primer4 được hiển thị. Trong hai bảng trên (primer1 và primer2), các làn từ 1 đến 5 là các chuỗi mã hóa APP gõ tự nhiên và các đường 7 đến 12 là các chuỗi mã hóa APP đột biến. Ngõ 6 là PCR từ DNA bộ gen của tế bào Balb / c3T3 chưa được truyền. Trong hai bảng thấp hơn (primer3 và primer4), các làn từ 1 đến 5 là các chuỗi mã hóa APP gõ tự nhiên và các đường 8 đến 11 là các chuỗi mã hóa APP đột biến gõ các dòng tế bào. Lanes 6 và 7 là kết quả PCR của các dòng tế bào w5 và s12, tương ứng. Đối với các sự kiện tái tổ hợp primer1 và primer2 đã được phát hiện cho cả hai nhiễm sắc thể ở các làn 1, 7, 9, 10 và 12, mà chúng tôi đặt tên là các dòng tế bào w5, s7, s9, s10 và s12. Các dòng tế bào w5 và s12 sau đó đã được sử dụng để chuyển đổi Cre để loại bỏ băng dừng, vì chúng là biểu thức GFP tốt nhất. Primer3 và primer4 đã được sử dụng để phát hiện việc xóa băng cassette. Ngõ 1 cho thấy cả hai băng dừng đã bị xóa khỏi dòng di động w5c1. Trong các làn 2, 3, 5 và 8, việc xóa băng cassette chỉ được phát hiện ở một trong hai nhiễm sắc thể và các dòng này được đặt tên là các dòng tế bào w5c2, w5c3, w5c5 và s12c8. Không phát hiện việc xóa băng cassette trong các điều khiển tiêu cực w5 và s12 ở làn 6 và 7.
Protein huỳnh quang màu xanh lá cây (GFP) đã được phát hiện trong các dòng tế bào w5 và s12, không có biểu hiện APP. Biểu hiện huỳnh quang GFP được quan sát thấy ở hơn 98% các tế bào trong cả hai dòng tế bào. Các tế bào bên trái được chụp ảnh dưới ánh sáng trắng trong khi các tế bào bên phải dưới ánh sáng kích thích GFP.
Biểu hiện quá mức Aβ gây ra apoptosis
Trong khi công cụ quảng bá gamma-actin gà (công cụ quảng bá CAG) nằm ở thượng nguồn của APP cDNA, biểu hiện của APP bị chặn bởi một băng STOP nằm giữa trình khởi động và trình tự mã hóa APP. Hai trang web LoxP đặt bên cạnh băng STOP tạo điều kiện loại bỏ nó và cho phép biểu hiện APP gây ra. Để loại bỏ băng STOP và tạo ra biểu thức APP, chúng tôi đã điện hóa 10ug vectơ LV-CRE (addgeneplasmid12105) vào các dòng tế bào w5 và s12 (có chèn APP chính xác), dẫn đến biểu hiện CRE recombinase loại bỏ điểm dừng cassette nằm giữa hai trang web LoxP. 24 giờ sau khi vectơ LV-CRE được điện hóa vào các ô, biểu thức A có thể được phát hiện ( Hình 4A). Tại cùng thời điểm này, apoptosis đã được quan sát thấy ở phần lớn các tế bào có cả dòng tế bào w5 và s12 ( Hình 4B ). Apoptosis phù hợp với các báo cáo trước đây rằng Aβ gây ra apoptosis thần kinh [ 22 ], và có thể gợi ý rằng các dòng tế bào w5 và s12 có thể là công cụ mạnh mẽ để xác định các loại thuốc bảo vệ tế bào khỏi bị apoptosis do biểu hiện quá mức peptide. Với cấy ghép, tỷ lệ apoptotic đã được tìm thấy giảm, trong đó sau 2 tuần, tốc độ apoptosis của các tế bào giảm xuống mức cơ bản ( Hình 4 ). Giới hạn pha loãng sau đó đã được sử dụng để thu được các dòng đơn bào ổn định được kích hoạt để thể hiện APP.
(A) Phát hiện biểu thức Aβ trong các dòng tế bào Balb / c 3T3, w5 và s12 trước và sau khi điện di véc tơ LV-CRE. Protein trong môi trường nuôi cấy tế bào được thu thập và lượng bằng nhau (100 g / làn) được phân tách bằng điện di gel SDS-polyacrylamide. Các mẫu protein (s12 và w5) tại các thời điểm khác nhau đến từ cùng một đĩa tế bào. Phương tiện được thu thập cứ sau 24 giờ và được thay thế bằng phương tiện mới. (B) Thay đổi mức độ apoptosis trong các dòng tế bào chuyển gen. Phụ lục nhuộm V / Propidium Iodide và phân tích FACS đã được sử dụng để định lượng sự xuất hiện phosphatidylserine và chết tế bào trong các tế bào 3T3, w5 và s12 sau khi điện di LV-CRE. Tỷ lệ tế bào dương tính với annexin V là tổng số các sự kiện ở góc phần tư phía trên bên phải và phía dưới bên phải và tỷ lệ tế bào dương tính với Propidium Iodide là tổng của các sự kiện ở góc phần tư phía trên bên trái và phía trên bên phải. (C) Mức độ apoptosis trong các dòng tế bào chuyển gen ở các thời điểm khác nhau. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0,001).
Biểu thức ổn định của APP và Aβ trong các dòng ô biểu thức APP được kích hoạt
Bằng cách hạn chế pha loãng, 60 phân thân APP có nguồn gốc đơn bào (30 đột biến kép Thụy Điển và 30 wildtype) đã được thu thập và phân tích để loại bỏ băng cassette bằng phương pháp PCR ( Hình 2B ) và phân tích Southern blot ( Hình S2 ). Cả hai phương pháp đều xác nhận loại bỏ băng dừng trong các dòng tế bào w5c1, w5c2, w5c3, w5c5 và s12c8. Phân tích Western blot được thực hiện bằng kháng thể APP Thr668 chống người (CST, # 2452) và kháng thể Aβ chống người (CST, # 2454). Kháng thể APP đã phát hiện các dải có kích thước dự kiến 90-140 kDa trong dung dịch tế bào và kháng thể Aβ đã phát hiện một dải có kích thước 5kDa trong cả môi trường và môi trường nuôi cấy tế bào từ các dòng tế bào w5c1, w5c2 và s12c8 ( Hình 5A – F). Trong khi Actin được tìm thấy trong môi trường nuôi cấy, nó có khả năng từ các tế bào chết. Tỷ lệ Abeta / actin cao hơn trong môi trường (1.6: 1) so với trong các tế bào (1.1: 1) cho thấy rằng ít nhất một số Abeta được giải phóng khỏi các tế bào sống. Các dải đại diện cho APP và Aβ mạnh hơn ở s12c8 so với w5c1 hoặc w5c2 ( Hình 5 ), chỉ ra rằng dòng s12c8, chứa chấp APP với đột biến kép của Thụy Điển, tạo ra nhiều APP và A hơn các dòng tế bào w5c1 và w5c2. Trình tự ứng dụng. Vì cả GFP và APP nên được biểu thị từ plasmid biểu hiện gen chuyển, chúng tôi đã nghiên cứu sự tập trung của GFP với APP trong các dòng tế bào w5c1 và s12c8 ( Hình 5G). Cấu trúc tế bào dương tính với GFP xuất hiện màu xanh lục, do huỳnh quang GFP và cấu trúc miễn dịch APP có màu đỏ, bởi TRITC, với mức độ huỳnh quang màu xanh lá cây tùy thuộc vào lượng GFP tích lũy trong các tế bào. Biểu hiện GFP ngoài tử cung không thường xuyên trong các tế bào âm tính APP và huỳnh quang đỏ hiếm khi được nhìn thấy trong các tế bào thiếu biểu hiện GFP.
W5c1 và w5c2 là các dòng tế bào gõ hAPP wildtype, trong khi dòng tế bào s12c8 chứa chuỗi hAPP với đột biến kép của Thụy Điển. (A) Top: Đại diện Western blot đồng nhất của hAPP gõ vào các dòng tế bào bằng kháng thể chống APP Thr668 của con người (CST, # 2452). Dưới cùng: Đại diện Western blot cho-actin (CST, # 4967) trong các dòng tế bào. Biểu hiện APP không thể phát hiện được trong các dòng tế bào w5 và s12. (B) Định lượng mức độ biểu hiện của APP trong các ô. (C) Đại diện Western blot đồng nhất tế bào từ APP gõ vào dòng tế bào được thực hiện với mAb đặc biệt nhận ra các đồng phân Aβ (CST, # 2454). (D) Định lượng mức biểu thức của Aβ trong các ô. (E) Đại diện Western blot của Aβ được phát hành vào phương tiện di động bằng cách sử dụng mAb đặc biệt nhận ra các đồng phân Aβ (CST, # 2454). Trong khi Actin được tìm thấy trong môi trường nuôi cấy thì khả năng này là từ các tế bào chết. Tỷ lệ Abeta / actin cao hơn trong môi trường (1.6: 1) so với trong các tế bào (1.1: 1). Điều này cho thấy rằng ít nhất một số Abeta đã được giải phóng khỏi các tế bào sống. (F) Phân tích định lượng mức độ biểu hiện Aβ trong môi trường nuôi cấy tế bào. Kết quả được trình bày trong B, D và F thu được từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SD. (G) Colocalization của GFP với APP sử dụng phương pháp miễn dịch huỳnh quang. Protein huỳnh quang màu xanh lá cây (GFP, màu xanh lá cây) và miễn dịch protein tiền chất Amyloid (APP) (màu đỏ) đồng địa hóa trong các dòng tế bào w5, w5c1 và s12c8. Các tế bào từ dòng tế bào w5 dương tính với GFP nhưng âm tính với APP. Thanh tỷ lệ = 200. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0.
Tác dụng của ibuprofen, donepezil và galantamin đối với biểu hiện APP và A42 của tế bào
Để kiểm tra tác động của các bộ điều biến tiềm năng của Aβ42peptide (đồng phân dư lượng 42 của amyloid-peptide), chúng tôi đã sử dụng High Content ( Hình 6 ) và Western blot ( Hình 7 ) với kháng thể APP Thr668 chống người (CST, # 2452 ) và kháng thể chống Aβ42 (CST, # 7672) để xác định những thay đổi về mức độ của peptide Aβ42 có tính amyloidogen cao. Chúng tôi thấy rằng việc điều trị bằng ibuprofen NSAID dẫn đến giảm nồng độ Aβ42peptide trong các dòng tế bào của chúng tôi w5c1 và s12c8, một kết quả tương tự như những người khác thấy trong các tế bào nuôi cấy khác [ 23 ]. Tuy nhiên, sự giảm nồng độ Aβ42 đã được quan sát cả trong các tế bào và trong môi trường nuôi cấy trên ibuprofen, tuy nhiên, không có sự thay đổi đáng kể nào về sự phong phú của protein holo-APP được quan sát ( Hình 6C), chỉ ra rằng sự thay đổi về mức Aβ42 là do thay đổi tốc độ xử lý APP. Theo thỏa thuận với các báo cáo trước đây [ 24 ], điều trị bằng aspirin không dẫn đến bất kỳ thay đổi đáng kể nào trong sản xuất hoặc bài tiết đồng phân Aβ42, hoặc mức APP ( Hình 6C ). Các chất ức chế acetylcholinesterase (AChEI) donepezil và galantamin, được sử dụng như là dòng đầu tiên trong dược trị liệu cho AD từ nhẹ đến trung bình [ 25 , 26 ], gây ra hiệu quả hạ thấp Aβ42 trong các dòng tế bào chuyển gen w5c1 và s12c8 phát hiện cả trong tế bào và trong môi trường nuôi cấy tế bào, không thay đổi nồng độ APP, sau khi điều trị bằng các thuốc này ( Hình 6 và 7). Thuốc chống loạn thần chlorpromazine có hiệu quả trong điều trị tâm thần phân liệt [ 27 ] và được sử dụng như một biện pháp kiểm soát tiêu cực trong nghiên cứu của chúng tôi. Khi các tế bào của chúng tôi được xử lý bằng chlorpromazine, không có sự thay đổi nào về sự phong phú của APP hoặc Aβ42 được quan sát thấy trong các tế bào hoặc trong môi trường nuôi cấy ( Hình 6C và 7B ). Định lượng sự thay đổi lượng Aβ42 được tiết ra từ tế bào vào môi trường nuôi cấy cho thấy dòng tế bào s12c8, có trình tự mã hóa APP chứa đột biến kép Thụy Điển, nhạy cảm hơn với các thuốc ức chế sản xuất Aβ42 so với dòng tế bào w5c1 ( Hình 7C ; Bảng 1).
Các dòng tế bào w5c1 và s12c8 được nhuộm cho các hạt nhân với Hoechst 33342 (màu xanh) và biểu thức GFP (màu xanh lá cây) đã được sử dụng để xác định vị trí các tế bào và vị trí APP. Biểu hiện Aβ42 được xác định bởi tetramethylrhodamineisothiocyanate (TRITC, màu đỏ). Hình ảnh được thu được với đầu đọc ArrayScan HCS với mục tiêu 10 lần. Định lượng được thực hiện với Ứng dụng sinh học tế bào sức khỏe tế bào (Cellomics, Pittsburgh, PA, Hoa Kỳ). Các tế bào được điều trị bằng ibuprofen, donepezil, galantamin, aspirin và chlorpromazine. PBS đã được sử dụng như một điều khiển. Dữ liệu được lấy từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SD. Thanh lỗi đại diện cho SD. (A) Hoạt động của thuốc trong dòng tế bào w5c1 được đo bằng Hàm lượng cao. (B) Hoạt động của thuốc trong dòng tế bào s12c8 được đo bằng Hàm lượng cao. (C) Định lượng thay đổi về mức độ APP và Aβ42 giữa các nhóm điều trị thuốc. APP đã được phát hiện trong Nội dung cao bằng cách sử dụng kháng thể APP Thr668 chống người làm kháng thể chính, CST # 2452 và kháng thể thứ cấp với TRITC khi phóng viên (dữ liệu không được hiển thị). Biểu hiện trong các tế bào bị ức chế đáng kể bởi ibuprofen, donepezil và galantamin trong cả dòng tế bào w5c1 và s12c8. Không có thay đổi đáng kể về sự phong phú của APP đã được nhìn thấy trong cả hai dòng tế bào sau khi điều trị bằng thuốc. Kết quả thu được từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SD. Thanh lỗi đại diện cho SD. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0,001). APP đã được phát hiện trong Nội dung cao bằng cách sử dụng kháng thể APP Thr668 chống người làm kháng thể chính, CST # 2452 và kháng thể thứ cấp với TRITC khi phóng viên (dữ liệu không được hiển thị). Biểu hiện trong các tế bào bị ức chế đáng kể bởi ibuprofen, donepezil và galantamin trong cả dòng tế bào w5c1 và s12c8. Không có thay đổi đáng kể về sự phong phú của APP đã được nhìn thấy trong cả hai dòng tế bào sau khi điều trị bằng thuốc. Kết quả thu được từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SD. Thanh lỗi đại diện cho SD. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0,001). APP đã được phát hiện trong Nội dung cao bằng cách sử dụng kháng thể APP Thr668 chống người làm kháng thể chính, CST # 2452 và kháng thể thứ cấp với TRITC khi phóng viên (dữ liệu không được hiển thị). Biểu hiện trong các tế bào bị ức chế đáng kể bởi ibuprofen, donepezil và galantamin trong cả dòng tế bào w5c1 và s12c8. Không có thay đổi đáng kể về sự phong phú của APP đã được nhìn thấy trong cả hai dòng tế bào sau khi điều trị bằng thuốc. Kết quả thu được từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SD. Thanh lỗi đại diện cho SD. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0,001). donepezil và galantamin trong cả hai dòng tế bào w5c1 và s12c8. Không có thay đổi đáng kể về sự phong phú của APP đã được nhìn thấy trong cả hai dòng tế bào sau khi điều trị bằng thuốc. Kết quả thu được từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SD. Thanh lỗi đại diện cho SD. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0,001). donepezil và galantamin trong cả hai dòng tế bào w5c1 và s12c8. Không có thay đổi đáng kể về sự phong phú của APP đã được nhìn thấy trong cả hai dòng tế bào sau khi điều trị bằng thuốc. Kết quả thu được từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SD. Thanh lỗi đại diện cho SD. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0,001).
(A) Cường độ băng tần Western blot được sử dụng để đo lường sự khác biệt về sự phong phú của Aβ42 trong môi trường nuôi cấy tế bào của tế bào w5c1 và s12c8 sau khi điều trị bằng thuốc. Blots đại diện được hiển thị. Các tế bào được điều trị bằng ibuprofen, donepezil, galantamin, aspirin và chlorpromazine. Kết quả thu được từ ba thí nghiệm độc lập, mỗi thí nghiệm được thực hiện ba lần và được biểu thị bằng trung bình ± SEM. Thanh lỗi đại diện cho SE. (B) Định lượng sự thay đổi nồng độ Aβ42 giữa các nhóm điều trị thuốc. Việc phát hành Aβ42 vào môi trường nuôi cấy tế bào đã bị ức chế đáng kể bởi ibuprofen, donepezil và galantamin trong cả hai dòng tế bào w5c1 và s12c8. Kết quả thu được từ ba thí nghiệm độc lập; từng được thực hiện trong ba lần và được biểu thị bằng trung bình ± SEM. Thanh lỗi đại diện cho SE. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (P <0,05). (C) So sánh tác dụng của thuốc đối với A42 giải phóng vào môi trường nuôi cấy tế bào bằng cách gõ wildtype và đột biến APP trong tế bào. Trong các nhóm điều trị ibuprofen và donepezil, s12c8 gây ra độ nhạy cao hơn đáng kể so với w5c1 đối với các phương pháp điều trị bằng thuốc. Dấu hoa thị cho thấy sự khác biệt có ý nghĩa thống kê giữa hai nhóm (* p <0,05, ** p <0,01, *** p <0,001).
| Điều trị | Mức Aβ1-42 (pg / ml) | Giảm so với kiểm soát PBS (pg / ml) | Phần trăm giảm (%) |
|---|---|---|---|
| w5c1 | |||
| PBS | 99,32 ± 0,49 | ||
| ibuprofen | 70,65 ± 0,62 | 28,59 ± 0,26 | 28,9 |
| donepezil | 68,48 ± 0,72 | 30,76 ± 0,30 | 31.0 |
| galantamin | 49,20 ± 0,62 | 50,04 ± 0,15 | 50,4 |
| aspirin | 99,83 ± 0,65 | -0,59 ± 0,18 | |
| chlorpromazine | 100,12 ± 0,96 | -0,88 ± 0,47 | |
| s12c8 | |||
| PBS | 120,00 ± 0,73 | ||
| ibuprofen | 79,20 ± 0,87 | 40,80 ± 0,52 | 34,0 |
| donepezil | 72,20 ± 0,81 | 47,80 ± 0,35 | 39,8 |
| galantamin | 59,10 ± 0,77 | 60,90 ± 0,60 | 50,8 |
| aspirin | 119,80 ± 0,73 | 0,20 ± 0,47 | |
| chlorpromazine | 120,12 ± 1,15 | -0,12 ± 0,79 |
Bảng 1. Tác dụng của các chất ức chế đối với việc giải phóng amyloid-β42 bằng cách gõ wildtype và đột biến APP trong các tế bào.
Tải xuống CSV
Thảo luận
AD là nguyên nhân gây mất trí nhớ phổ biến nhất ở người cao tuổi và Aβ được cho là đóng vai trò then chốt trong sinh bệnh học của nó [ 2 ]. Các liệu pháp điều trị AD hướng vào con đường trao đổi chất liên quan đến sự hình thành Aβ đã được phát triển trong hơn 20 năm qua, tuy nhiên, kết quả từ những phương pháp này đã gây thất vọng [ 28 – 30 ]. Các mô hình sàng lọc thuốc hiện tại không thỏa đáng do một số vấn đề bao gồm sự phức tạp của quy trình, tỷ lệ nhân sự thấp, thay đổi mục tiêu cao, chi phí cao và biểu hiện Aβ không ổn định [ 6]. Chúng tôi dự định xây dựng một mô hình tế bào sàng lọc thuốc mới cho AD và tập trung vào mục đích nghiên cứu của chúng tôi trên hai điểm: 1: Thiết lập gõ gen trong các dòng tế bào với hiệu quả chỉnh sửa gen cao và tỷ lệ thay đổi mục tiêu không mong muốn thấp.2: Xây dựng các dòng tế bào biểu hiện APP ở mức cao có khả năng phản ứng với các thuốc nhắm vào các điểm chính trong con đường amyloidogen hoặc các con đường khác ảnh hưởng đến chuyển hóa APP.
Với việc sử dụng ZFN, có nhiều ứng dụng trong nghiên cứu cơ bản, nông nghiệp và trị liệu cho con người, chúng tôi đã tạo ra các cú gõ APP trong các dòng tế bào với hiệu quả chỉnh sửa gen được cải thiện. Việc gõ APP trong các dòng tế bào được thiết lập với hiệu suất chỉnh sửa gen là 7,2% (7/96, gõ wildtype) và 6,2% (6/96, APP đột biến gõ), thấp hơn một chút so với hiệu quả được báo cáo bởi những người khác ( cao tới 10 đỉnh20% [ 31 – 33 ]). Tuy nhiên, tỷ lệ 7% của chúng tôi cao hơn nhiều so với hiệu quả chỉnh sửa gen được tạo ra bằng phương pháp truyền thống, mang lại tỷ lệ xấp xỉ 0,01% [ 34 ], với tần suất được báo cáo tối đa khoảng 0,4% [ 35 ]. Cặp ZFN mà chúng tôi đã sử dụng nhắm mục tiêu chuỗi 18bp ( cacctctcc CGTCA ggtggtgtt , với chuỗi mục tiêu được gạch chân) nằm trong intron đầu tiên củagen Rosa26 . Trong lựa chọn quỹ tích đích, ba yếu tố đã được xem xét: Đầu tiên, chúng ta cần chọn một trang web có độ đặc hiệu và ái lực theo trình tự ZFP cao. Thứ hai, do độ đặc hiệu và độ đặc hiệu của ZFP được thiết kế cho trang đích của họ chỉ cao nhất khi các thiết kế ZF riêng lẻ được chọn trong bối cảnh các ngón tay lân cận của chúng [ 36 ], chúng tôi phải xem xét khả năng tương thích giữa từng ngón tay được chọn. Thứ ba, một miếng đệm phù hợp giữa hai vị trí nhận dạng ZFN là bắt buộc. Sử dụng các tiêu chí này, chúng tôi đã xác định chuỗi 18 bp trong intron 1 củaRosa26locus là trang web mục tiêu ZFN của chúng tôi và chuỗi 18 bp phải đủ dài để chỉ định duy nhất một vị trí trong bộ gen của động vật có vú [ 37 – 39 ].
Để tăng hiệu quả chỉnh sửa gen và tránh các thay đổi mục tiêu không cần thiết, chúng tôi đã áp dụng phương pháp chuyển giao mRNA, trong đó một đoạn DNA có chứa chất khởi động và vùng mã hóa protein quan tâm được điện hóa vào các tế bào, để tạo ra mRNA cho hạt nhân ZFN dựa trên dị hợp Hiện tại, hai phương pháp ưa thích để thể hiện ZFN là: (1) biến đổi các plasmid biểu hiện ZFN [ 6 , 37 ] hoặc (2) chuyển đổi các đoạn DNA tuyến tính mã hóa các mRNA ZFN [ 40 , 41]. Mặc dù cần nghiên cứu thêm để xác định phương pháp nào trong số các phương pháp này phù hợp nhất để sửa đổi gen bằng ZFN, kiến thức hiện tại chỉ ra rằng có sự khác biệt rõ rệt giữa hai phương pháp này. Việc truyền plasmid có thể làm phát sinh khả năng biểu hiện vĩnh viễn của ZFN do sự tích hợp của plasmid vào bộ gen chủ [ 42 , 43] và sự tích hợp này làm tăng nguy cơ ảnh hưởng ngoài mục tiêu do khả năng cấu trúc biểu hiện ZFN được tích hợp vào gen nội sinh và do đó tạo ra đột biến chèn không mong muốn. Việc truyền một đoạn DNA tuyến tính mã hóa ZFN thường tránh được các vấn đề liên quan đến đột biến chèn chèn, nhưng thường có biểu hiện thoáng qua hơn của ZFN. Trong nghiên cứu hiện tại, chúng tôi đã khai thác những ưu điểm của phương pháp chuyển giao mRNA, sau khi các thử nghiệm in vitro của chúng tôi chứng minh tính hiệu quả của ZFN ( Hình 1). Các đoạn DNA bao gồm vùng mã hóa ZFN và chất kích thích CMV đã được đưa vào bằng cách điện hóa vào nguyên bào sợi bào thai Balb / c 3T3, sử dụng phương pháp để giảm thiểu đột biến qua trung gian ZFN gây ra hiệu ứng gây độc tế bào đối với sự phát triển của tế bào. Do độc tính trong các tế bào động vật có vú thường là do sự phân cắt của các chuỗi không phải mục tiêu [ 44 ] và sự phá vỡ mục tiêu của ZFN chủ yếu là do hoạt động của các monome ZFN tạo thành các homodim nhắm vào các vị trí không chính xác, các hiệu ứng này có thể giảm đáng kể sử dụng các biến thể nokease FokI chỉ có thể tạo thành các dị vòng [ 44]. Tóm lại, việc sử dụng một cách tiếp cận với một cặp ZFN đột biến cho phép chúng tôi tạo ra một cú gõ gen trong mô hình tế bào với hiệu quả nhân sự cao và với tỷ lệ thay đổi ngoài mục tiêu thấp, và minh họa rằng cách tiếp cận này cũng có khả năng được sử dụng bởi điều tra khác về chức năng protein.
Hệ thống Cre-LoxP tạo điều kiện cho các nghiên cứu của chúng tôi vì chúng tôi có thể tạo ra các dòng tế bào thực hiện hoặc không thể hiện APP, tùy thuộc vào mức độ tiếp xúc của chúng với Cre. Sự biểu hiện quá mức của APP, hoặc một tên miền phụ của nó, có thể dẫn đến một hiệu ứng gây chết người ngay lập tức, do đó ngăn chặn việc sử dụng các tế bào được chuyển đổi để điều tra thêm. Thật vậy, chúng tôi đã quan sát tỷ lệ apoptotic trên 80% trong 24 giờ sau khi phân phối LV-CRE (plasmid chứa chuỗi mã hóa Cre) vào các dòng tế bào w5 và s12, trong đó biểu thức Cre kích hoạt biểu thức APP ( Hình 4 ). Aβ đã được phát hiện trong môi trường nuôi cấy tế bào từ các dòng tế bào được xử lý bằng Cre ( Hình 4A), cho thấy rằng mức độ APP hoặc Aβ tăng có thể đã gây ra cái chết tế bào. Tỷ lệ apoptotic cao được quan sát thấy trong các dòng tế bào này có thể là một tính năng hữu ích, vì LV-CRE đã thay đổi w5 và s12 có thể được sử dụng để sàng lọc các loại thuốc bảo vệ các tế bào này khỏi tác động có hại của các đồng phân A trong ống nghiệm. Mặc dù có những tác động tiềm tàng của việc sản xuất quá mức amyloid, các nghiên cứu về các quá trình trao đổi chất thiết yếu trong các tế bào biểu hiện APP hiện có thể truy cập được. Một số tế bào biểu hiện quá mức APP đã được tìm thấy để tồn tại thông qua chuyển giao văn hóa, dẫn đến sự phát triển của chúng tôi về các dòng tế bào w5c1 và s12c8. Khi một băng biểu hiện cho protein huỳnh quang màu xanh lá cây (GFP) được đưa vào thượng nguồn của vùng mã hóa APP trong mẫu HR của chúng tôi và tạo ra protein hợp nhất GFP-APP,Hình 5 ).
Cả hai trình tự mã hóa APP đột biến kép của Thụy Điển và Thụy Điển đều ở các cấu trúc biểu thức sử dụng cùng một công cụ quảng bá gà gamma-Actin (CAG), với chất tăng cường CMV, tiếp theo là băng cassette biểu hiện cho protein huỳnh quang xanh và trình tự ức chế, và cả hai đều được chèn vào cùng một locus gen, chuỗi intron Rosa26 . Sự giống nhau của vùng kiểm soát di truyền cho cả hai cấu trúc APP (đột biến kép kiểu hoang dã và Thụy Điển) sẽ mang lại biểu hiện mô hình song song cho cả hai cấu trúc. Dòng tế bào w5c1 có hai bản sao của chuỗi APP wildtype, với một bản được chèn vào mỗi hai alen Rosa26trong bộ gen của dòng tế bào này. Ngược lại, các dòng tế bào 12c8 chỉ có một bản sao duy nhất của chuỗi APP (đột biến kép của Thụy Điển), vì chỉ một trong hai alen Rosa26 có gen chuyển vào. Khi chúng tôi mô tả các dòng tế bào w5c1 và s12c8 về mặt biểu hiện của APP và Aβ, cả hai đều tạo ra APP và Aβ có thể phát hiện miễn dịch ( Hình 5 ). Mặc dù có sự tương đồng về kiểm soát di truyền và chỉ có một bản sao của cấu trúc biểu hiện, mức độ APP và Aβ trong các tế bào hoặc môi trường có nguồn gốc từ dòng tế bào s12c8 cao hơn gần 1,2 lần so với dòng tế bào w5c1 ( Hình 5 ) . Quan sát này cho thấy đột biến kép của Thụy Điển trong trình tự mã hóa APP giúp tăng cường tính ổn định của APP và Aβ.
Chuyển hóa APP trong đó con đường hình thành Aβ chứa ba giai đoạn giả định (α, và γ- secretase) dường như còn nguyên vẹn trong các tế bào của chúng ta. Để xác nhận rằng con đường secretase đang được sử dụng trong các tế bào của chúng tôi, chúng tôi đã sửa đổi hoạt động của các giai đoạn bí mật và đo mức APP, Aβ và Aβ42. Chúng tôi xác nhận rằng cả w5c1 và s12c8 đều có những thay đổi trong sản xuất Aβ42 để đáp ứng với điều trị bằng thuốc ( Hình 6 và 7 ). Donepezil, chất gây ra sự gia tăng nồng độ của α-secretase ADAM 10 [ 25 ] và galantamin (Gal), ức chế sự biểu hiện của enzyme phân cắt APP tại chỗ 1 (BACE 1,-secretase) [ 26 ], đáng kể giảm sản xuất42 trong cả hai dòng tế bào ( Hình 6 và 7). NSAID, chẳng hạn như ibuprofen, được biết là làm giảm mức Aβ42 [ 23 ] bằng cách điều chỉnh hoạt động secret-secretase [ 45 ]. Trong các tế bào của chúng tôi, ibuprofen, ở 250mM, đã ức chế sản xuất Aβ42 (hàm lượng tế bào, Hình 6 ) và bài tiết (trong môi trường nuôi cấy, Hình 7 ), trong khi điều trị bằng aspirin không cho thấy tác dụng hạ A42 ( Hình 6 và 7). Kết quả của chúng tôi cho thấy các tế bào của chúng tôi đang sử dụng con đường secretase, do đó chúng sẽ hữu ích cho việc sàng lọc các loại thuốc bổ sung có thể làm thay đổi sản xuất Aβ42 thông qua con đường này. Tác dụng ức chế của donepezil, galantamin và ibuprofen trong sản xuất Aβ42 cho thấy sự khác biệt nhất quán giữa các dòng tế bào w5c1 và s12c8, với các thuốc cho thấy tác dụng mạnh hơn trong dòng tế bào s12c8 ( Bảng 1 , Hình 7 ). Độ nhạy cao hơn của dòng tế bào s12c8, có chứa APP với đột biến kép của Thụy Điển, cho thấy rằng nó có thể hữu ích nhất để sàng lọc thuốc.
Vì các dòng tế bào biến đổi gen của chúng tôi w5c1 và s12c8 cho thấy sản xuất Aβ42 có thể phát hiện được có thể bị ức chế bởi các chất ức chế và điều chế secretase đã biết, các tế bào này sẽ là công cụ hữu ích để làm rõ các cơ chế liên quan đến chuyển hóa amyloid. Hệ thống của chúng tôi có thể dễ dàng bị thao túng bởi các quy trình sinh học dược lý và tế bào, do đó nghiên cứu quy định sản xuất amyloid ở các mức độ phiên mã, dịch mã, sửa đổi hậu biến và / hoặc suy thoái, trong các dòng tế bào này sẽ mang lại hiểu biết sâu sắc hơn và dẫn đến các ứng dụng điều trị để điều trị AD.
Vật liệu và phương pháp
1: Plasmid xây dựng
Cặp bổ sung của các hạt nhân ngón tay kẽm (ZFN) ZFL (pmlm290, plasmid 21872) và ZFR (pmlm292, plasmid 21873) đã được mua từ Addgene. Các ZFNs, ZFL và ZFR, nuôi dưỡng một cặp đột biến trong lĩnh vực FokI nuclease (E490K và I538K, và Q486E và I499L, cho ZFL và ZFR, tương ứng; dấu “+” và “-“đột biến, xem 44 ) mà trao heterodimeric hành vi cho các lĩnh vực này. Các vectơ xương sống đã được tiêu hóa bằng BamHI và XbaI và các vùng mã hóa ngón tay kẽm đã được thay thế bằng các đoạn DNA chứa các chuỗi mã hóa được thiết kế cho tay trái và phải của Protein Finger Finger (ZFP) dành riêng cho chuỗi mục tiêu của chúng tôi. Các mRNA ZFP được thiết kế dựa trên trình tự đồng thuận khung kẽm-ngón tay được mô tả trước đây [ 46]. Các ZFP nhận ra từng chuỗi 3 bp cụ thể trong vị trí mục tiêu đã chọn được thiết kế dựa trên dữ liệu từ Phòng thí nghiệm Kỹ thuật di truyền nâng cao Sigma (SAGE) và trình tự mã hóa được Invitrogen tổng hợp.
Cặp ZFN dựa trên FokI, không đồng nhất của chúng tôi nhắm vào chuỗi 18 bp trong intron đầu tiên của gen Rosa26 . Chuỗi này bao gồm một cặp gồm 9 chuỗi cơ sở (được gạch chân) nằm bên cạnh một vùng đệm 5bp (được in đậm): 5′- cacctctcc CGTCA ggtggtgtt -3. Hai chuỗi DNA 9bp, cacctctcc và và ggtggtgttTHER là các trang web nhận dạng ZFN, được phân tách bằng trình tự spacer 5 bitp CGTCA , sẽ là trang web mục tiêu ZFN nơi ZFN tạo ra Double Break Breaks. Một chuỗi 18 bp phải đủ dài để xác định một vị trí duy nhất trong bộ gen của động vật có vú [ 37 – 39]. Các chuỗi axit amin của dư lượng xác định độ đặc hiệu của ba ngón tay kẽm trong ZFL là: ngón tay 1, RRHILDR (nhận ra GTG); ngón 2, RQDNLGR (GAG); và ngón 3, QANHLSR (GGA). Trong ZFR, chúng là: ngón 1, AATALRR (GTT); ngón 2, EAHHLSR (GGT); và ngón 3, IRHHLKR (GGT).
Các cấu trúc biểu thức ZFN chứa cả trình khởi động phage T7 và trình khởi tạo CMV cho phép biểu hiện trong cả tế bào nhân sơ và tế bào nhân chuẩn. Đối với tất cả các thí nghiệm biểu hiện, các plasmid biểu hiện ZFN lần đầu tiên được tuyến tính hóa bằng cách tiêu hóa với BstBI và SacI.
Một đoạn DNA (0,98kb) tương ứng với vị trí đích ZFN (TS) đã được trích xuất từ DNA bộ gen của các tế bào Balb / c 3T3 và được nhân bản vào vị trí nhân bản của pMD-19T để tạo thành vectơ ZFN-TS ( Hình 1A ) phục vụ như là chất nền cho quá trình tiêu hóa ZFN trong ống nghiệm.
Các thành phần của vectơ nhắm mục tiêu Rosa26 (pRosa26 wt và pRosa26 swe) (được minh họa trong hình S1 ) được mô tả như sau: Băng cassette độc tố bạch hầu (DTA) là từ plasmid DTA (Addgene plasmid 22730). Các nhánh tái tổ hợp tương đồng được chiết xuất từ DNA bộ gen của tế bào Balb / c 3T3. Công cụ quảng bá Chicken-Actin-CMV (công cụ quảng bá CAG, Addgene plasmid 11150) là một công cụ quảng bá phổ biến mạnh mẽ, với chất tăng cường CMV, tiếp theo là băng cassette cho protein huỳnh quang màu xanh lá cây (GFP) [ 47]. Ngay sau băng cassette biểu hiện GFP, có một chuỗi chấp nhận ghép nối adenovirus (SA) theo sau là một trang web loxP, một băng biểu hiện neomycin và một chuỗi dừng phiên mã mạnh (ba chuỗi đa chuỗi SV40). Trình tự dừng phiên mã sau đó được theo sau bởi một trang web loxP khác, theo cùng hướng với trình tự đầu tiên, trình tự mã hóa APP và trình tự polyadenylation hormone tăng trưởng của bò. APP sẽ chỉ được thể hiện nếu trình tự dừng phiên mã mạnh được loại bỏ bằng cách tái tổ hợp qua trung gian Cre recombinase giữa hai vị trí loxP. Một địa điểm PacI nằm ở vị trí 5 ‘so với SA, và một địa điểm AscI là 3’ đối với các địa điểm polyadenytation hormone tăng trưởng của bò, và được sử dụng để tiêu hóa giành chiến thắng ở miền Nam. Các cấu trúc chứa cả hai loại wildtype (con người APP751 cDNA) và chứa đột biến kép của Thụy Điển (con người APP751 cDNA với KM670 / 671NL2) đã được tạo ra. Vectơ LV-CRE (addgene plasmid 12105) mã hóa Cre recombinase bằng tín hiệu vị trí hạt nhân (nls) dưới sự kiểm soát của bộ khởi động CMV bên trong. Để tạo ra biểu hiện Cre trong các tế bào, chúng tôi đã điều hòa LV-CRE được tiêu hóa kép (KpnI và NotI), chứa chất kích hoạt CMV và vùng mã hóa Cre-nls, vào các ô biến đổi APP của chúng tôi.
2: Đặc tính in vitro của sự phân tách theo trình tự bởi các ZFN được thiết kế
Xét nghiệm dịch mã phiên mã in vitro (IVTT) đã được sửa đổi [ 48 ] đã được sử dụng để dịch ZFN để sàng lọc sự phân tách DNA theo trình tự cụ thể của chúng. Giao thức này sử dụng phage T7 RNA polymerase để tạo ra các mRNA từ các plasmid biểu hiện ZFN được tuyến tính hóa của chúng tôi và hệ thống IVTT của hồng cầu lưới thỏ để tạo ra các sản phẩm protein tổng hợp được mã hóa bởi các mRNA này trong một chiết xuất thô để nghiên cứu sự phân tách của chuỗi ZFN. Các quy trình tuân thủ theo hướng dẫn của nhà sản xuất Hệ thống Phiên âm / Phiên dịch ghép nhanh TNT® T7 (Promega).
3: Phân tích NHEJ sau khi phân tách theo trình tự ZFN của các tế bào Balb / c 3T3
Các tế bào Balb / c 3T3 (ATCC ® CCL-164 ™) đã được đồng bộ hóa với 2,5 đoạn DNA tuyến tính (xem ở trên) có chứa vùng mã hóa ZFR và ZFL và bộ khởi động CMV. Khoảng 1 × 10 6 tế bào đã được thay thế với tổng số 5 ug DNA bằng cách điện hóa ở 260v trong 30ms theo giao thức của nhà sản xuất. Các tế bào đã được thu hoạch sau 48 giờ sau khi truyền và DNA bộ gen được phân lập bằng DNA MasterPure Kit (TaKaRa). Sự điều chỉnh do ZFN gây ra của locus gen bao gồm Rosa26 đã được phân tích bằng cách khuếch đại PCR các vùng quan tâm bằng cách sử dụng cặp mồi primer1 ( Bảng S1). Điều kiện PCR: Biến tính ban đầu 95 ° C trong 10 phút, sau đó là 30 chu kỳ 90 ° C trong 60 giây; 60 ° C trong 60 giây; 72 ° C trong 30 giây. Độ giãn dài cuối cùng là trong 10 phút ở 72 ° C. 3 ul của sản phẩm PCR đã được thử nghiệm trên gel agarose 1,5% TAE để xác nhận khuếch đại. Các đoạn PCR được TA nhân bản vào vector plasmid PMD-19T (TaKaRa). Thư viện của các phân đoạn intron I của Rosa26 đã được chuyển thành các tế bào E. coli và tổng cộng 48 khuẩn lạc tái tổ hợp đã được giải trình tự để xác định loại và phân bố tổn thương tại vị trí Intron 1. Các chuỗi có> 2 bp đột biến indel nằm trong spacer ± 1 bp được coi là sửa đổi bộ gen do ZFN gây ra. Trình tự sắp xếp đã được xác nhận thêm bằng cách so sánh với bộ gen của chuột bằng BLAST.
4: Vectơ và tải nạp tế bào
Để tạo mục tiêu chèn các plasmid biểu hiện ZFN được nhắm mục tiêu theo chuỗi nhắm mục tiêu Rosa26 và vectơ nhắm mục tiêu Rosa26 được tuyến tính hóa được truyền vào các ô. DNA ZFN tuyến tính đã được mô tả ở trên. Plasmids pRosa26 (pRosa26wt và pRosa26swe) đã được tuyến tính hóa ở mức 5end của nhánh tương đồng ngắn với BstBI. Các tế bào Balb / c 3T3 được điện di với tổng số 50ng DNA sử dụng tỷ lệ ZFN: nhà tài trợ là 3: 1. DNA đã được hòa tan trong bộ đệm điện hóa ở nồng độ làm việc 15 ng L (pRosa26) cùng với các đoạn bao gồm cả vùng mã hóa ZFN và chất kích thích CMV. Balb / c 3T3 tế bào, ở nồng độ 10 7/ ml (300ul), được điều hòa điện với hỗn hợp nhắm mục tiêu tuyến tính và vectơ biểu thức ZFN ở 260v trong 30ms. Các tế bào được truyền đã được mở rộng để phân tích tế bào học dòng chảy (FACSCalibur; Becton Dickinson Pharmingen) và trích xuất DNA bộ gen. Các tế bào được giữ trong lựa chọn với 60018g / ml G418 trong hai tuần và tổng số 192 dòng vô tính đơn bào (96 đột biến và 96 wildtype) đã thu được bằng cách hạn chế pha loãng và phân tích để tích hợp vào vị trí mục tiêu ZFN bằng PCR, Southern blot phân tích và phát hiện GFP. Tổng cộng có 7 ký tự đại diện và 6 đột biến APP của Thụy Điển trong các dòng tế bào đã được thiết lập có chèn APP chính xác. Sau đó, vectơ LV-CRE được điện hóa vào các dòng tế bào đã được thiết lập s12 (với trình tự APP đột biến kép của Thụy Điển) và w5 (với trình tự APP kiểu wildtype) để loại bỏ băng cassette giữa hai vị trí LoxP, cho phép liên kết của trình quảng bá CAG APP cDNA và do đó gây ra biểu hiện APP. Bằng cách hạn chế pha loãng, 60 dòng vô tính đơn bào (30 đột biến và 30 wildtype) đã được thu thập và phân tích để loại bỏ băng cassette bằng phương pháp PCR và phân tích blot miền Nam. Các dòng tế bào được tạo ra được đặt tên bằng cách sử dụng các quy ước sau: chữ cái đầu tiên w hoặc s đề cập đến đột biến kép hoặc kiểu Thụy Điển tương ứng; số chỉ số của bản sao; c (nếu có) đề cập đến việc bổ sung Cre recombinase; số thứ hai (nếu có) trọng tài sao chép số sau bổ sung Cre. cho phép liên kết của trình quảng bá CAG với cDNA của APP và do đó tạo ra biểu thức APP. Bằng cách hạn chế pha loãng, 60 dòng vô tính đơn bào (30 đột biến và 30 wildtype) đã được thu thập và phân tích để loại bỏ băng cassette bằng phương pháp PCR và phân tích blot miền Nam. Các dòng tế bào được tạo ra được đặt tên bằng cách sử dụng các quy ước sau: chữ cái đầu tiên w hoặc s đề cập đến đột biến kép hoặc kiểu Thụy Điển tương ứng; số chỉ số của bản sao; c (nếu có) đề cập đến việc bổ sung Cre recombinase; số thứ hai (nếu có) trọng tài sao chép số sau bổ sung Cre. cho phép liên kết của trình quảng bá CAG với cDNA của APP và do đó tạo ra biểu thức APP. Bằng cách hạn chế pha loãng, 60 dòng vô tính đơn bào (30 đột biến và 30 wildtype) đã được thu thập và phân tích để loại bỏ băng cassette bằng phương pháp PCR và phân tích blot miền Nam. Các dòng tế bào được tạo ra được đặt tên bằng cách sử dụng các quy ước sau: chữ cái đầu tiên w hoặc s đề cập đến đột biến kép hoặc kiểu Thụy Điển tương ứng; số chỉ số của bản sao; c (nếu có) đề cập đến việc bổ sung Cre recombinase; số thứ hai (nếu có) trọng tài sao chép số sau bổ sung Cre. chữ cái đầu tiên w hoặc s tương ứng với kiểu đột biến hoang dã hoặc đột biến kép của Thụy Điển; số chỉ số của bản sao; c (nếu có) đề cập đến việc bổ sung Cre recombinase; số thứ hai (nếu có) trọng tài sao chép số sau bổ sung Cre. chữ cái đầu tiên w hoặc s tương ứng với kiểu đột biến hoang dã hoặc đột biến kép của Thụy Điển; số chỉ số của bản sao; c (nếu có) đề cập đến việc bổ sung Cre recombinase; số thứ hai (nếu có) trọng tài sao chép số sau bổ sung Cre.
5: Chuẩn bị DNA bộ gen
Các tế bào được đồng nhất hóa trong dung dịch đệm ly giải (50 mM Tris-HCl, pH 8.0; 100 mM EDTA, pH 8.0; 1% SDS, 100 mM NaCl, 350 g μL Proteinase K) và được ủ ở 55 ° C trong 2 giờ rung lắc mạnh mẽ. DNA bộ gen được phân lập sau khi chiết xuất phenol / chloroform và kết tủa isopropanol. Các viên đã được bán lại trong bộ đệm EDTA 10 mMTris / 1 mM (pH 7,5).
6: Phân tích trình tự và PCR
Cặp mồi primer1 đã được sử dụng để khuếch đại cánh tay tương đồng 5′ / bộ khởi động CAG và primer2was được sử dụng để khuếch đại đường giao nhau của nhánh tương đồng. Để phân tích xem các alen Rosa26 đã kết hợp lại với pRosa26 hay chưa, chúng tôi đã sử dụng primer3 để khuếch đại trình tự mã hóa 5′-CAG / Neo. Primer4 được sử dụng để khuếch đại đường giao nhau của hai vị trí LoxP ( Hình 2A ) để phân tích cắt bỏ băng cassette từ Rosa26các alen trong các dòng tế bào biểu hiện APP được kích hoạt. Quá trình khuếch đại được thực hiện bằng cách sử dụng PrimerSTAR HS DNA polymerase (TaKaRa), giúp giảm thiểu lượng khuếch đại không đặc hiệu trong các phản ứng 20 μl. PCR sử dụng các điều kiện chu trình sau: 1 chu kỳ ở 95 ° C trong 5 phút, 38 chu kỳ [60 giây ở 94 ° C; 60 giây ở 60 ° C; 3 phút ở 72 ° C], 1 chu kỳ ở 72 ° C trong 10 phút. Các sản phẩm PCR từ các tế bào biểu hiện các sự kiện tái tổ hợp tương đồng đã được giải trình tự trực tiếp và so sánh với trình tự vector pRosa26.
7: Phân tích Nam Blot
DNA bộ gen được tiêu hóa được phân tách trên gel agarose 1% và làm mờ trên màng Hybond Np (GE Health). Các màng sau đó được liên kết ngang với tia cực tím và được ủ trước trong bộ đệm lai dễ dàng (Roche) trong 10 giờ ở 42 ° C khi quay. Các đầu dò được phân lập thành các mảnh 204-bp (sp) và 472bp (spn). Các sp thăm dò (204bp) (nằm ở thượng nguồn của trang web mục tiêu ZFN ngay sau khi trang web XbaI như thể hiện trong Hình 2A ) đã được chuẩn bị bằng phương pháp PCR sử dụng cặp mồi 5′ GGCTAACCTGGTGTGTGG 3′ và 5′ AATACTCCGAGGCGGATC 3′ sử dụng toàn bộ chiều dài cánh tay tái tổ hợp tương đồng plasmid làm mẫu với bộ tổng hợp PCR DIG (Roche). Đầu dò spn (472bp) (nằm trong vùng mã hóa APP như trong Hình 2A ) đã được chuẩn bị bằng PCR bằng cách sử dụng mồi5 ‘AGAGAGGCTTGAGGCCAA 3’ và 5 ‘AGGCACGTTGTAGAGCAG 3’ , và bản sao plasmid hAPP cDNA có độ dài đầy đủ làm mẫu, sử dụng bộ tổng hợp PCR DIG (Roche) (xem Hình S2 ). Các đầu dò lai được dán nhãn bằng cách sử dụng bộ khởi động phát hiện và dán nhãn DNA High Prime DNA(Roche) và được lai với màng qua đêm ở 42 ° C. Màng được rửa và đầu dò lai được phát hiện miễn dịch.
8: Miễn dịch huỳnh quang
Các tế bào (hợp lưu 80%) được rửa ba lần trong dung dịch muối đệm phốt phát (PBS, pH 7.2), và sau đó cố định trong Paraformaldehyd 4% trong PBS chứa 0,1% (vol / vol) Triton X-100 (PBST) ở nhiệt độ phòng trong 10 tối thiểu Trước khi nhuộm miễn dịch huỳnh quang, các vị trí liên kết không đặc hiệu đã bị chặn bằng cách ủ các tế bào trong 5% Bovine Serum Albumin (BSA, Boehringer) trong PBST trong 30 phút ở 37 ° C. Kháng thể chính cho APP (CST, # 2452) và Actin (CST, # 4967) đã được sử dụng. Kháng thể được pha loãng trong PBST và ủ được thực hiện qua đêm ở 4 ° C. Các tế bào đã được rửa ba lần với PBST. Ủ bằng kháng thể thứ cấp [kháng thể chống thỏ kết hợp với tetramethylrhodamineisothiocyanate ( TRITC) (Phân tử Probes Inc.)] pha loãng trong đệm chặn được thực hiện trong 30 phút ở 37 ° C. Các tế bào đã được rửa ba lần trong PBST.
9: Phân tích Western Blot
Phân tích blot Western được thực hiện như mô tả trước đây với sửa đổi nhỏ [ 49]. Các phân tử tế bào được lấy từ các tế bào được rửa rộng rãi bằng PBS và được lọc trực tiếp trong ba dung dịch lysate của tế bào khử nhiễm. Nồng độ protein được xác định bằng máy quang phổ tử ngoại. Lượng bằng nhau (100 μg / làn) của dung dịch tế bào hoặc môi trường nuôi cấy được phân tách bằng điện di gel natri dodecyl sulfate polyacrylamide (SDS-PAGE) hoặc Tricineedom SDS-PAGE và được chuyển sang màng polyvinylidenedifluoride (Hybond P). Các blots đã được thử nghiệm với một kháng thể chính thích hợp, tiếp theo là IgG kháng thỏ kết hợp HRP (Công nghệ tín hiệu tế bào, CST). Các dải protein được hiển thị bằng phương pháp phát hiện hóa phát quang (ECL) nâng cao (Bio-Rad) và cường độ của dải được phân tích bằng mật độ kế (LAS-4000; GE Health). Hàm lượng protein miễn dịch trong mỗi mẫu được tính toán dựa trên đường cong chuẩn được xây dựng bằng A42; chất lượng tải của các mẫu được đánh giá dựa trên đường cong chuẩn được xây dựng bằng BSA. Mỗi bộ thí nghiệm được lặp lại ít nhất 3 lần để xác nhận kết quả. Mức độ protein-actin, được đo bằng phương pháp định lượng phương Tây bằng cách sử dụng kháng thể β-actin (CST, # 4967), được sử dụng làm chất chiết xuất và kiểm soát tải.
10: Hoạt động của chất ức chế secret-secretase, chất kích hoạt α-secretase và NSAID
Các tế bào được ủ trong 96 đĩa giếng cho hàm lượng cao và 6 đĩa giếng để phân tích Western blot với mật độ 2,0 × 104 / ml tế bào mỗi giếng qua đêm. Ibuprofen, aspirin, donepezil, galantamin và chlorpromazine được điều chế trong PBS và thuốc được thêm vào tế bào trong môi trường tươi ở nồng độ cuối cùng lần lượt là 250 mM, 250 mM, 1.5μM, 0.9M và 250 mM. Điều trị được tiếp tục trong 24 giờ. Các tế bào trong 96 đĩa giếng đã được chuẩn bị cho Nội dung cao để kiểm tra các thay đổi về biểu hiện APP và Aβ42 trong các ô. Các tế bào trong 6 đĩa giếng đã được chuẩn bị cho Western Blots để phân tích sự thay đổi nồng độ peptide trong cả tế bào và trong môi trường nuôi cấy tế bào. Tất cả các thử nghiệm được lặp lại 3 lần và kết quả là từ một thử nghiệm đại diện hoặc tất cả các thử nghiệm (có nghĩa là ± SD) được hiển thị.
Thông tin hỗ trợ
Hình S1.
Bản đồ của các vectơ nhắm mục tiêu (pRosawt và pRosaswe). Vectơ pRosa26swe chứa cDNA APP751 của con người với đột biến kép của người Thụy Điển (KM670 / 671NL2). Vectơ pRosa26wt chứa ký tự đại diện APP751 cDNA. Phiên mã được điều khiển bởi chất kích thích gamma-actin gà (chất hoạt hóa CAG, với chất tăng cường CMV, sau đó là băng cassette biểu hiện cho Protein huỳnh quang xanh (GFP)). Vùng mã hóa APP (APPwt và APPswe) nằm ở hạ lưu của chuỗi chấp nhận mối nối adenovirus, sau đó là trang LoxP, PGK-Neo-pA và ba bản sao của tín hiệu polyA SV40, có chức năng như một băng cassette, trang web LoxP thứ hai, trong cùng định hướng như lần đầu tiên, với tất cả những điều này là thượng nguồn của chuỗi polyadenylation hormone tăng trưởng bò. Cánh tay tái tổ hợp tương đồng nằm ở hai bên của những mảnh vỡ này. DTA hoạt động như một điểm đánh dấu chọn lọc.
https://doi.org/10.1371/journal.pone.0075493.s001
(TIF)
Hình S2.
Phân tích miền Nam blot của các dòng tế bào biểu hiện APP biến đổi gen. Đầu dò sp (204bp) đã được chuẩn bị bằng cách sử dụng bản sao plasmid cánh tay ngắn có chiều dài đầy đủ làm mẫu với các mồi 5 ‘GGCTAACCTGGTGTGTGG 3’ và 5 ‘AATACTCCGAGGCGGATC 3’và bộ tổng hợp PCR DIG (Roche). Spn đầu dò (472bp) đã được chuẩn bị bằng cách sử dụng bản sao plasmid hAPP cDNA plasmid có độ dài đầy đủ làm mẫu với các đoạn mồi 5 ‘AGAGAGGCTTGAGGCCAA 3’ và 5 ‘AGGCACGTTGTAGAGCAG 3’ và bộ tổng hợp PCR (Ro). Vị trí của hai đầu dò này được hiển thị trong Hình 2A. DNA bộ gen (6 g) đã được tiêu hóa qua đêm với 30 đơn vị enzyme hạn chế XbaI (đối với các dòng tế bào biểu hiện APP đã được thay đổi ban đầu) và SacII (đối với các dòng tế bào được xử lý bằng Cre receiveobinase (LV-CRE)) với thể tích 30 μL. (A) Xác định các ô chứa cấu trúc biểu thức APP. Phân tích blot phía Nam bằng cách sử dụng sp thăm dò đã được tiến hành để xác nhận việc chèn đoạn APP vào vị trí gen của Rosa26 . DNA bộ gen được tiêu hóa với giới hạn endonuclease XbaI. Băng tần hoang dã (wt) có kích thước tính toán là 4,3 kb. Một sự kiện tái tổ hợp ở một trong hai nhiễm sắc thể tạo ra các dải tương ứng với độ dài 2,3 kb và 4,3 kb. Các tế bào có sự kiện tái tổ hợp ở cả hai nhiễm sắc thể có các dải tương ứng với độ dài 2,3 kb. Kiểm soát (lane1) là DNA bộ gen của các tế bào Balb / c 3T3. Ngõ 3 được đặt tên là w5, một dòng tế bào có hAPPwt gõ vào cả hai nhiễm sắc thể. Lanes 5, 6 và 7 được đặt tên là s7, s9 và s12 là các dòng tế bào gõ hAPPswe có chứa các sự kiện tái tổ hợp trong cả hai nhiễm sắc thể. (B) Xác định các dòng tế bào với biểu thức APP được kích hoạt. Phân tích blot miền Nam đã được thực hiện bằng cách sử dụng đầu dò spn để xác nhận việc xóa băng dừng giữa hai vị trí LoxP. DNA bộ gen được tiêu hóa với endonuclease giới hạn SacII. Trước khi xóa, kích thước của băng tần được tính là 5,8 kb. Sự tái tổ hợp giữa các vị trí LoxP ở một trong hai nhiễm sắc thể sẽ tạo ra các dải có độ dài 3,1 kb và 5,8 kb. Các tế bào có băng dừng bị xóa trong cả hai nhiễm sắc thể sẽ có dải 3,1 kb. Kiểm soát (lane1 và 2) là DNA bộ gen của w5 và s12. Lanes 4, 5, 6 và 7 là w5c2, w5c3, w5c5 và s12c8, các dòng tế bào có băng cassette dừng ở một trong hai nhiễm sắc thể. Lane3 được đặt tên là w5c1, một dòng tế bào chứa chấp việc xóa băng cassette trong cả hai nhiễm sắc thể.
https://doi.org/10.1371/journal.pone.0075493.s002
(TIF)
Bảng S1.
Mồi PCR được sử dụng trong đặc tính tế bào.
https://doi.org/10.1371/journal.pone.0075493.s003
(DOCX)
Sự đóng góp của tác giả
Được hình thành và thiết kế các thí nghiệm: XZ HL DMI HT. Thực hiện các thí nghiệm: XZ HL. Đã phân tích dữ liệu: XZ HL DMI HT. Thuốc thử / vật liệu / công cụ phân tích đóng góp: YM Z. Lei RW TG LJ RS WX NZ YZ RH XW HH Z. Li GN XZ HL DMI HT. Đã viết bản thảo: XZ HL DMI HT.
Tài liệu tham khảo
- 1.Hardy JA, Higgins GA (1992) Bệnh Alzheimer: Giả thuyết Cascade Amyloid. Khoa học 256: 184-185. doi: https://doi.org/10.1126/science.1566067 . PubMed: 1566067 .
- 2.Hardy J, Selkoe DJ (2002) Giả thuyết amyloid về bệnh Alzheimer: tiến triển và các vấn đề trên con đường trị liệu. Khoa học 297: 353-356. doi: https://doi.org/10.1126/science.1072994 . PubMed: 12130773 .
- 3.Harrill JA, Robinette BL, Mundy WR (2011) Sử dụng phân tích hình ảnh hàm lượng cao để phát hiện những thay đổi do hóa chất gây ra trong quá trình tổng hợp synap trong ống nghiệm. Toxicol_Vitro25: 368-387. PubMed: 20969947 .
- 4.Kounnas MZ, Danks AM, Cheng S, Tyree C, Ackerman E et al. (2010) Điều chế-secretase làm giảm lắng đọng-amyloid trong mô hình chuột biến đổi gen của bệnh Alzheimer. Thần kinh 67: 769-780. doi: https://doi.org/10.1016/j.neuron.2010.08.018 . PubMed: 20826309 .
- 5.Asai M, Iwata N, Tomita T, Iwatsubo T, Ishiura S et al. (2010) Hiệu quả bốn liệu pháp cocktail thuốc nhắm mục tiêu amyloid-peptide cho bệnh Alzheimer. J Neurosci Res 88: 3588-3597. doi: https://doi.org/10.1002/jnr.22503 . PubMed: 20890992 .
- 6.Urnov FD, Miller JC, Lee YL, Beausejour CM, Rock JM và cộng sự. (2005) Hiệu chỉnh gen người nội sinh hiệu quả cao bằng cách sử dụng các hạt nhân ngón tay kẽm được thiết kế. Thiên nhiên 435: 646-651. doi: https://doi.org/10.1038/nature03556 . PubMed: 15806097 .
- 7.Shaughnessy L, Chamblin B, McMahon L, Nair A, Thomas MB và cộng sự. (2004) Tiểu thuyết tiếp cận các mô hình bệnh lý Alzheimer để sàng lọc và phát triển thuốc. J Mol_Neurosci 24: 23-32. PubMed: 15314246 .
- số 8.Yahata N, Asai M, Kitaoka S, Takahashi K, Asaka I và cộng sự. (2011) Nền tảng sàng lọc thuốc chống A sử dụng tế bào thần kinh có nguồn gốc tế bào iPS của con người để điều trị bệnh Alzheimer. PLOS MỘT 6: e25788. doi: https://doi.org/10.1371/journal.pone.0025788 . PubMed: 21984949 .
- 9.Yamanaka S (2009) Một cái nhìn mới mẻ về các tế bào iPS. Ô 137: 13-17. doi: https://doi.org/10.1016/j.cell.2009.03.034 . PubMed: 19345179 .
- 10.Miller J, McLachlan AD, Klug A (1985) Các miền liên kết kẽm lặp đi lặp lại trong yếu tố phiên mã protein IIIA từ tế bào trứng Xenopus. EMBO J 4: 1609-1614. PubMed: 4040853 .
- 11.Nhận dạng DNA của Wolfe SA, Nekludova L, Pabo CO (2000) bằng protein ngón tay kẽm Cys2His 2 . Annu Rev Biophys Biomol Cấu trúc 29: 183-212. doi: https://doi.org/10.1146/annurev.biophys.29.1.183 . PubMed: 10940247 .
- 12.Geurts AM, Cost GJ, Freyvert Y, Zeitler B, Miller JC và cộng sự. (2009) Chuột Knockout thông qua vi tiêm phôi của các hạt nhân ngón tay kẽm. Khoa học 325: 433. doi: https://doi.org/10.1126/science.1172447 . PubMed: 19628861 .
- 13.Meyer M, de Angelis MH, Wurst W, Kühn R (2010) Nhắm mục tiêu gen bằng cách tái tổ hợp tương đồng trong hợp tử chuột qua trung gian của các hạt nhân ngón tay kẽm. Proc Natl Acad Sci Hoa Kỳ (Hoa Kỳ) 107: 15022-15026. doi: https://doi.org/10.1073/pnas.1009424107 . PubMed: 20686113 .
- 14.Meng X, Noyes MB, Zhu LJ, Lawson ND, Wolfe SA (2008) Nhắm mục tiêu bất hoạt gen ở cá ngựa vằn bằng cách sử dụng các hạt nhân ngón tay kẽm được thiết kế. Nat Biotechnol 26: 695-701. doi: https://doi.org/10.1038/nbt1398 . PubMed: 18500337 .
- 15.Doyon Y, McCammon JM, Miller JC, Faraji F, Ngo C et al. (2008) Sự gián đoạn gen mục tiêu có thể có ở cá ngựa vằn bằng cách sử dụng các hạt nhân ngón tay kẽm được thiết kế. Nat Biotechnol 26: 702-708. doi: https://doi.org/10.1038/nbt1409 . PubMed: 18500334 .
- 16.Foley JE, Yeh JR, Maeder ML, Reyon D, Sander JD và cộng sự. (2009) Đột biến nhanh chóng các gen của cá ngựa vằn nội sinh bằng cách sử dụng các hạt nhân ngón tay kẽm được tạo ra bởi kỹ thuật Oligomeized Pool (OPEN). PLOS MỘT 4: e4348. doi: https://doi.org/10.1371/journal.pone.0004348 . PubMed: 19198653 .
- 17.Morton J, Davis MW, Jorgensen EM, Carroll D (2006) Cảm ứng và sửa chữa các đứt gãy sợi đôi nhắm mục tiêu nuclease ngón tay kẽm trong các tế bào soma Caenorhabditiselegans. Proc Natl Acad Sci Hoa Kỳ (Hoa Kỳ) 103: 16370-16375. doi: https://doi.org/10.1073/pnas.0605633103 .
- 18.Beumer KJ, Trautman JK, Bozas A, Liu JL, Rutter J et al. (2008) Nhắm mục tiêu gen hiệu quả trong Drosophila bằng cách tiêm phôi trực tiếp với các hạt nhân ngón tay kẽm. Proc Natl Acad Sci Hoa Kỳ (Hoa Kỳ) 105: 19821-19826. doi: https://doi.org/10.1073/pnas.0810475105 . PubMed: 19064913 .
- 19.Bibikova M, Carroll D, DJ Segal, Trautman JK, Smith J et al. (2001) Kích thích tái tổ hợp tương đồng thông qua sự phân cắt mục tiêu bởi các hạt nhân tinh tinh. Biol Biol 21: 289-297. doi: https://doi.org/10.1128/MCB.21.1.289-297.2001 . PubMed: 11113203 .
- 20.Lloyd A, Plaisier CL, Carroll D, Drews GN (2005) gây đột biến nhắm mục tiêu bằng cách sử dụng các hạt nhân ngón tay kẽm trong cây Arabidopsis. Proc Natl Acad Sci Hoa Kỳ (Hoa Kỳ) 102: 2232-2237. doi: https://doi.org/10.1073/pnas.0409339102 . PubMed: 15677315 .
- 21.Perez EE, Wang J, Miller JC, Jouvenot Y, Kim KA và cộng sự. (2008) Thiết lập tính kháng HIV-1 trong các tế bào T CD4 + bằng cách chỉnh sửa bộ gen bằng cách sử dụng các hạt nhân ngón tay kẽm. Nat Biotechnol 26: 808-816. doi: https://doi.org/10.1038/nbt1410 . PubMed: 18587387 .
- 22.Morishima Y, Gotoh Y, Zieg J, Barrett T, Takano H và cộng sự. (2001) Beta-amyloid gây ra apoptosis tế bào thần kinh thông qua một cơ chế liên quan đến con đường kinase c-Jun N-terminal và sự khởi phát của phối tử Fas. J Neurosci 21: 7551-7560. PubMed: 11567045 .
- 23.Weggen S, Eriksen JL, Das P, Sagi SA, Wang R et al. (2001) Một tập hợp con NSAID thấp hơn Abeta42 amyloidogen độc lập với hoạt động cyclooxygenase. Thiên nhiên 414: 212-216. doi: https://doi.org/10.1038/35102591 . PubMed: 11700559 .
- 24.Skovronsky DM, Lee VM, Praticò D (2001) Protein tiền chất Amyloid và peptide beta amyloid trong tiểu cầu của con người. Vai trò của cyclooxygenase và protein kinase C. J Biol_Chem 276: 17036-17043. PubMed: 11278299 .
- 25.Zimmermann M, Gardoni F, Marcello E, Colciaghi F, Borroni B et al. (2004) Các chất ức chế Acetylcholinesterase làm tăng hoạt động ADAM10 bằng cách thúc đẩy buôn bán các dòng tế bào u nguyên bào thần kinh. J Neurochem 90: 1489-1499. doi: https://doi.org/10.1111/j.1471-4159.2004.02680.x . PubMed: 15341532 .
- 26.Li Q, Wu D, Zhang L, Zhang Y (2010) Tác dụng của galantamine đối với sự giải phóng-amyloid và biểu hiện enzyme cắt tại chỗ 1 trong các tế bào SH-SY5Y khác biệt của u nguyên bào thần kinh ở người. Exp_Gerontol 45: 842-847. PubMed: 20600777 .
- 27.Kane JM, Correll CU (2005) Tiến bộ trong quá khứ và hiện tại trong điều trị dược lý của bệnh tâm thần phân liệt. J Tâm thần học lâm sàng 71: 1115-1124. PubMed: 20923620 .
- 28.Sambamurti K, Greig NH, Utsuki T, Barnwell EL, Sharma E et al. (2011) Mục tiêu điều trị AD: thông điệp mâu thuẫn từ các chất ức chế-secretase. J Neurochem 117: 359-374. doi: https://doi.org/10.1111/j.1471-4159.2011.07213.x . PubMed: 21320126 .
- 29.Forsyth E, Ritzline PD (1998) Tổng quan về nguyên nhân, chẩn đoán và điều trị bệnh Alzheimer. Vật lý 78: 1325-1331. PubMed: 9859951 .
- 30.Hampel H, Lista S, Khachaturian ZS (2012) Phát triển các dấu ấn sinh học để lập biểu đồ cho tất cả các giai đoạn bệnh Alzheimer: con đường hoàng gia để cắt nút Gordian trị liệu. Bệnh Alzheimer 8: 312-336. doi: https://doi.org/10.1016/j.jalz.2012.05.859 . PubMed: 22736138 .
- 31.Townsend JA, Wright DA, Winfrey RJ, Fu F, Maeder ML et al. (2009) Điều chỉnh tần số cao các gen thực vật bằng cách sử dụng các hạt nhân ngón tay kẽm. Thiên nhiên 459: 442-445. doi: https://doi.org/10.1038/nature07845 . PubMed: 19404258 .
- 32.Maeder ML, Thibodeau-Beganny S, Osiak A, Wright DA, Anthony RM et al. (2008) Kỹ thuật “nguồn mở” nhanh chóng của các hạt nhân ngón tay kẽm tùy chỉnh để chỉnh sửa gen hiệu quả cao. Tế bào mol. 31: 294-301. doi: https://doi.org/10.1016/j.molcel.2008.06.016 . PubMed: 18657511 .
- 33.Rô bốt A, Genovese P, Beausejour CM, Colleoni S, Lee YL et al. (2007) Chỉnh sửa gen trong các tế bào gốc của con người bằng cách sử dụng các hạt nhân ngón tay kẽm và phân phối vec tơ lentivirus khiếm khuyết tích hợp. Nat Biotechnol25: 1298-1306. doi: https://doi.org/10.1038/nbt1353 . PubMed: 17965707 .
- 34.Vasileva A, Linden RM, Jessberger R (2006) Tái tổ hợp tương đồng là cần thiết để nhắm mục tiêu gen qua trung gian AAV. Axit nucleic Res 34: 3345-3360. doi: https://doi.org/10.1093/nar/gkl455 . PubMed: 16822856 .
- 35.Tsuchiya H, Harashima H, Kamiya H (2005) Tăng hiệu quả chỉnh sửa gen SFHR với DNA chuỗi đơn có ý nghĩa. J Gene Med 7: 486 bóng493. doi: https://doi.org/10.1002/jgm.673 . PubMed: 15521053 .
- 36.Bhakta MS, Henry IM, Ousterout DG, Das KT, Lockwood SH et al. (2013) Các hạt nhân ngón tay kẽm hoạt động cao bằng cách lắp ráp mô đun mở rộng. Bộ gen Res 23: 530-538. doi: https://doi.org/10.1101/gr.143693.112 . PubMed: 23222846 .
- 37.Hurt JA, Thibodeau SA, Hirsh AS, Pabo CO, Joung JK (2003) Protein ngón tay kẽm đặc hiệu cao thu được bằng cách xáo trộn miền định hướng và lựa chọn dựa trên tế bào. Proc Natl Acad Sci Hoa Kỳ (Hoa Kỳ) 100: 12271-12276. doi: https://doi.org/10.1073/pnas.2135381100 . PubMed: 14527993 .
- 38.Biali RR, Barbas CF 3 (2002) Kỹ thuật sao chép các ngón tay bằng kẽm polydactyl. Nat Biotechnol 20: 135-141. doi: https://doi.org/10.1038/nbt0202-135 . PubMed: 11821858 .
- 39.Moore M, Klug A, Choo Y (2001) Cải thiện tính đặc hiệu liên kết DNA từ các peptide ngón tay poly kẽm bằng cách sử dụng chuỗi các đơn vị hai ngón tay. Proc Natl Acad Sci Hoa Kỳ (Hoa Kỳ) 98: 1437-1441. doi: https://doi.org/10.1073/pnas.98.4.1437 .
- 40.Gỗ AJ, Lo TW, Zeitler B, Pickle CS, Ralston EJ et al. (2011) Chỉnh sửa bộ gen được nhắm mục tiêu trên các loài bằng cách sử dụng ZFN và TALEN. Khoa học 333: 307. doi: https://doi.org/10.1126/science.1207773 . PubMed: 21700836 .
- 41.Mashimo T, Takizawa A, Voigt B, Yoshimi K, Hiai H et al. (2010) Tạo ra chuột Knockout với suy giảm miễn dịch kết hợp nghiêm trọng liên kết với X (SC-SC) bằng cách sử dụng các hạt nhân ngón tay kẽm. PLOS MỘT 5: e8870. doi: https://doi.org/10.1371/journal.pone.0008870 . PubMed: 20111598 .
- 42.Kar Nam S, Konishi Y, Ota A, Takahashi M, Damdindorj L et al. (2012) Giám sát đơn giản về hiệu quả nhắm mục tiêu gen trong các dòng tế bào Soma của con người bằng cách sử dụng gen PIGA. PLOS MỘT 7: e47389. doi: https://doi.org/10.1371/journal.pone.0047389 . PubMed: 23056640 .
- 43.Amarir-Bouhram J, Goin M, Petit MA (2011) Hiệu quả tái tổ hợp bất hợp pháp được tạo thuận lợi tương đồng trong quá trình kết hợp ở Escherichia coli. PLOS MỘT 6: e28876. doi: https://doi.org/10.1371/journal.pone.0028876 . PubMed: 22194937 .
- 44.Miller JC, Holmes MC, Wang J, Guschin DY, Lee YL và cộng sự. (2007) Một kiến trúc nuclease ngón tay kẽm được cải tiến để chỉnh sửa bộ gen rất đặc biệt. Nat Biotechnol 25: 778-785. doi: https://doi.org/10.1038/nbt1319 . PubMed: 17603485 .
- 45.Eriksen JL, Sagi SA, Smith TE, Weggen S, Das P et al. (2003) NSAID và các chất đối kháng của flurbiprofen nhắm mục tiêu γ-secretase và hạ Aβ 42 in vivo. J Đầu tư 112: 440-449. doi: https://doi.org/10.1172/JCI200318162 . PubMed: 12897211 .
- 46.Cui X, Ji D, Fisher DA, Wu Y, Briner DM và cộng sự. (2011) Tích hợp có mục tiêu trong phôi chuột và chuột với các hạt nhân ngón tay kẽm. Nat Biotechnol 29: 64-67. doi: https://doi.org/10.1038/nbt.1731 . PubMed: 21151125 .
- 47.Niwa H, Yamamura K, Miyazaki J (1991) Lựa chọn hiệu quả cho các chất cấy có biểu hiện cao với một vectơ nhân chuẩn mới lạ. Gen 108: 193-199. doi: https://doi.org/10.1016/0378-1119(91)90434-D . PubMed: 1660837 .
- 48.Ruminy P, Derambure C, Chandrasegaran S, Salier JP (2001) Xác định tầm xa của các vị trí gắn kết tế bào hạt nhân tế bào gan-3 (FoxA) tầm xa với một nhân tế bào. J Mol_Biol 310: 523-535. PubMed: 11439020 .
- 49.Koob AO, Bruns L, Prassler C, Masliah E, Klopstock T et al. (2012) Phân tích protein thông qua Western blot của các tế bào được tách ra từ não người và mô cơ. Sinh hóa hậu môn 425: 120-124. doi: https://doi.org/10.1016/j.ab.2012.02.034 . PubMed: 22402104 .