Các phương thức điều trị cho chứng sa sút trí tuệ trong hội chứng Down
trừu tượng
Hội chứng Down (DS) là bất thường nhiễm sắc thể được biết đến nhiều nhất, đặc trưng bởi một nhiễm sắc thể 21 thừa và nhiều vấn đề toàn thân. Việc sản xuất cao hơn protein tiền thân amyloid (APP), peptide tiền chất của beta-amyloid, khiến những người mắc bệnh DS mắc bệnh Alzheimer giai đoạn đầu (AD). Tỷ lệ sa sút trí tuệ đã tăng lên như một hàm số của tuổi thọ kéo dài của những người mắc bệnh DS. Bởi vì chúng tôi biết rất ít về việc điều trị chứng sa sút trí tuệ ở những người mắc bệnh DS, bài tổng quan này tập trung vào sinh lý bệnh và các chiến lược quản lý để cải thiện chất lượng cuộc sống tổng thể.
Giới thiệu & Cơ sở
Hội chứng Down (DS), còn được gọi là Trisomy 21, là chứng rối loạn di truyền phổ biến nhất ảnh hưởng đến khoảng 1/100 đến 1/1000 ca sinh trên toàn cầu [1] . Hội chứng này là kết quả của việc thừa kế thêm một nhiễm sắc thể 21 hoặc một phần bị lệch của nhiễm sắc thể 21. Điều này dẫn đến khuyết tật trí tuệ và các bất thường về thể chất thường được đặc trưng bởi [2] các đặc điểm khuôn mặt khác biệt và tăng trưởng còi cọc [3] . Hội chứng cũng có thể liên quan đến đục thủy tinh thể bẩm sinh, dị tật tim, bệnh Hirschsprung, hội chứng West, động kinh, bệnh bạch cầu, ngưng thở khi ngủ, thiếu hụt cảm giác, bệnh lý tự miễn dịch và nội tiết, lão hóa sớm hơn và suy giảm nhận thức và bệnh lý thần kinh loại Alzheimer [4]. Với tuổi thọ của người mắc bệnh DS được cải thiện, nguy cơ mắc bệnh sa sút trí tuệ ở độ tuổi càng sớm càng cao. Tỷ lệ hiện mắc là 10% ở độ tuổi từ 40 đến 49 tuổi, 40% ở độ tuổi từ 50-59 và 56% ở những người trên 60 tuổi [1,2] .
Những người có DS có thể phát triển các triệu chứng của bệnh Alzheimer (AD) sớm hơn những người khác vì sự gia tăng sản xuất protein tiền thân amyloid (APP), peptide tiền thân của beta-amyloid nằm trên nhiễm sắc thể 21. Tăng biểu hiện protein của các gen trên nhiễm sắc thể 21 gây ra một loạt các tác động đến sự phát triển cấu trúc não bộ của thai nhi, tác động đến hành vi trong suốt cuộc đời của người mắc bệnh DS [4] . Một nghiên cứu gần đây cho thấy rằng mức tăng của amyloid beta-peptide gây ra mức độ căng thẳng oxy hóa cao và thoái hóa thần kinh sau đó ở bệnh nhân DS lớn tuổi [5]. Ngoài khuynh hướng di truyền này, các nghiên cứu đã đề xuất các yếu tố có thể thay đổi được cũng ảnh hưởng đến sức khỏe nhận thức và tăng nguy cơ sa sút trí tuệ, đặc biệt là ở bệnh AD khởi phát lẻ tẻ. Các yếu tố nguy cơ có thể thay đổi này bao gồm béo phì, ăn kiêng kém, hút thuốc, uống rượu, bệnh tim mạch, huyết áp cao và mức độ xã hội hóa thấp [1] .
Hoạt động thể chất cũng là một yếu tố nguy cơ quan trọng có thể có tác dụng bảo vệ thần kinh. Một số nghiên cứu cho thấy mối liên hệ nghịch giữa hoạt động thể chất và nguy cơ sa sút trí tuệ trong dân số nói chung [1] . Mặc dù các phương pháp điều trị tâm lý xã hội đã được chứng minh là có hiệu quả trong việc giúp bệnh nhân kiểm soát các triệu chứng của họ, nhưng chứng sa sút trí tuệ vẫn chưa được biết đến. Thuốc ức chế men cholinesterase (donepezil, galantamine và rivastigmine) và chất đối kháng thụ thể N-methyl-D aspartate (NMDA), memantine, điều trị AD. Các liệu pháp khác, bao gồm vitamin E, B và statin, đã mang lại nhiều kết quả khác nhau trong các thử nghiệm lâm sàng. Cũng không rõ liệu có bất kỳ can thiệp nào có thể làm chậm sự tiến triển của suy giảm nhận thức ở những người chưa được chẩn đoán mắc chứng sa sút trí tuệ hay không [2,4,6]. Tổng quan này nhằm mục đích tóm tắt bệnh lý thần kinh, các chiến lược để cải thiện hiệu suất nhận thức và các phương thức điều trị chứng sa sút trí tuệ ở DS.
Các phương pháp tìm kiếm
Chúng tôi đã thu thập và xem xét các bài báo từ năm 2009 đến năm 2022. Cơ sở dữ liệu được sử dụng là PubMed, Google Scholar, PubMed Central và Science Direct. Các từ khóa được sử dụng: hội chứng Down, tam nhiễm sắc thể 21, mông cổ, dị tật bẩm sinh, liệu pháp tập thể dục, memantine, donepezil, chất ức chế acetylcholinesterase, sa sút trí tuệ, bệnh Alzheimer.
Kiểm tra lại
Phần này sẽ trình bày về sinh lý bệnh của AD ở những người có DS cũng như các lựa chọn điều trị, bao gồm các phương pháp tiếp cận dùng thuốc và không dùng thuốc.
Cơ chế bệnh sinh của AD ở những người có DS
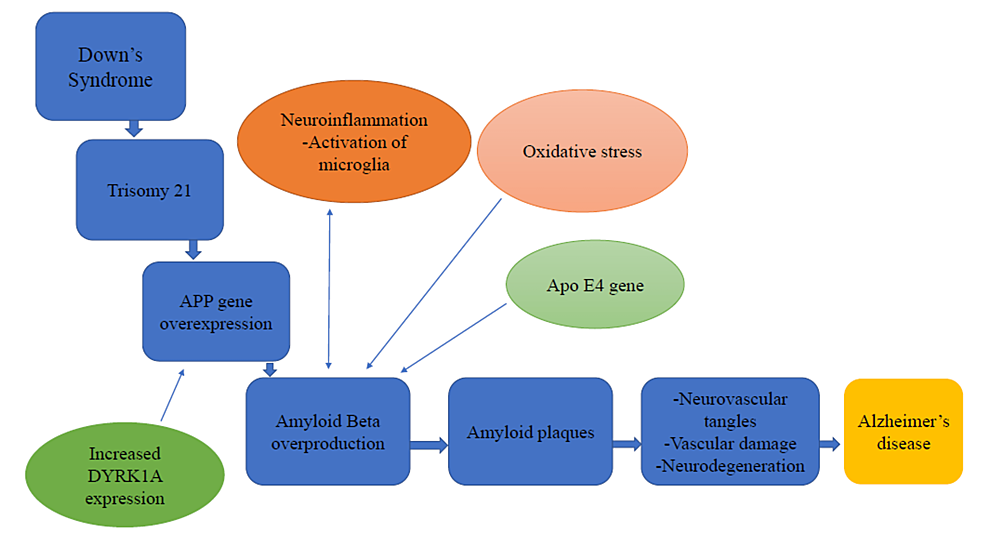
AD phát triển ở tuổi trung niên được đặc trưng bởi những thay đổi bệnh lý thần kinh trong chuyển hóa gốc tự do, giảm hoạt động của ty thể và thoái hóa tế bào thần kinh. Nguyên nhân phân tử của AD là chủ đề của nhiều cuộc điều tra, và không ai biết nguyên nhân gây bệnh là gì [5] . Hình 1 minh họa bệnh lý thần kinh của AD ở những người có DS.
Sự biểu hiện quá mức của gen APP dường như là một thành phần quan trọng trong sự phát triển của AD ở DS [3] . Các enzym phân giải protein alpha, beta và gamma-secretase phân cắt gen APP. Alpha-secretase và gamma-secretase chịu trách nhiệm cho sự phân cắt bình thường của APP, dẫn đến các sản phẩm không hòa tan. Gen APP bị Beta-secretase và Gamma secretase phân cắt trong con đường truyền tín hiệu AD, tạo ra các monome không hòa tan được gọi là peptit Beta-amyloid (Aβ). Vì gen Beta secretase nằm trên nhiễm sắc thể 21, bản sao bổ sung của nhiễm sắc thể này tạo ra nhiều Beta secretase hơn, dẫn đến lượng Aβ và các mảng amyloid cao hơn trong DS [3] . Các mảng amyloid phát triển các đám rối sợi thần kinh giữa các tế bào thần kinh, làm gián đoạn tín hiệu giữa chúng [8]và kích hoạt các phản ứng miễn dịch gây viêm, tổn thương mạch máu và quá trình apoptosis tế bào thần kinh [9] . Mối liên hệ giữa AD khởi phát sớm và các đột biến trong gen APP và gen presenilin là trọng tâm của giả thuyết phân tầng amyloid. Do gen APP nằm trên nhiễm sắc thể 21 và do đó, được di truyền lần ba bởi những người có DS cùng với các gen khác trên nhiễm sắc thể 21, nguy cơ mắc AD khởi phát sớm liên quan đến DS cao hơn làm nổi bật gen APP như một yếu tố quan trọng [ 8,9] .
Các biến số khác, chẳng hạn như kiểu gen apolipoprotein E (ApoE) [10] , đóng một vai trò trong mức độ nghiêm trọng của bệnh lý AD ở cả dân số nói chung và những người mắc bệnh DS. ApoE cần thiết để bảo tồn và tái tạo mạch tiếp hợp sau khi bị hư hỏng. Gen ApoE tạo ra ba dạng đồng dạng protein ApoE: ApoE-2, ApoE3 và ApoE4. Những người mang ApoE4 có nguy cơ mắc AD và bệnh mạch vành cao hơn, nhưng ApoE3 và ApoE2 bảo vệ tương đối chống lại cả hai tình trạng này [11] . Sự hiện diện của ApoE4 làm tăng nguy cơ AD, với lượng amyloid tích tụ trong não tăng gấp hai lần [9,11] . Sự hiện diện của tất cả bốn alen có liên quan đến việc tăng nguy cơ mắc AD trong dân số nói chung và khởi phát sớm hơn ở DS[1] .
Viêm thần kinh cũng được công nhận là có vai trò nhất định trong căn nguyên của AD, chủ yếu là thông qua việc kích hoạt các microglia [9] . Microglia là các tế bào não chuyên biệt có vai trò bảo vệ hệ miễn dịch của não. Tùy thuộc vào các kích thích và bối cảnh, nó có thể tham gia vào tín hiệu chống viêm hoặc chống viêm [12,13]. Theo các nghiên cứu, sự tương tác giữa Aβ và microglia trong AD làm trầm trọng thêm phản ứng viêm. Microglia thiết lập một rào cản xung quanh mảng bám Aβ để ngăn chặn sự lây lan thêm trong khi cũng cố gắng loại bỏ Aβ. Microglia có thể thực bào Aβ sau khi được kích hoạt xung quanh mảng bám Aβ. Sự tích tụ của Aβ trong tế bào vi mô có thể dẫn đến chết tế bào vi mô, tăng tình trạng viêm và tạo ra nhiều vi mô đệm hơn, do đó kéo dài đợt viêm. Ngoài ra, microglia hoạt hóa có thể bắt đầu phản ứng tiền viêm, giải phóng các cytokine như yếu tố hoại tử khối u-α (TNF-α) và interleukin 1β (IL-1β), cũng như các chất khác, gây tổn thương mô [13] .
Lý thuyết stress oxy hóa cũng có thể giải thích sự phát triển của AD ở bệnh nhân DS. Sự mất cân bằng giữa việc tạo ra các gốc tự do và sự bảo vệ chống oxy hóa được gọi là stress oxy hóa (OS). Các loại oxy phản ứng (ROS) như gốc superoxide, hydrogen peroxide (H2O2), và các loại hydroxyl, gây ra sự thoái hóa thần kinh, được gặp rộng rãi trong quá trình chuyển hóa oxy hóa [5] . Các enzym chống oxy hóa như superoxide dismutase (SOD), glutathione peroxidase (GPx) và catalase (CAT) hỗ trợ loại bỏ ROS. Trong số đó, enzyme SOD là chất cảm ứng hệ điều hành tiềm năng nhất. Ba đồng dạng tồn tại trong cơ thể: (1) nội bào, đồng / kẽm SOD (còn được gọi là SOD1); (2) SOD ngoại bào, đồng / kẽm; và (3) mangan SOD nằm ở ty thể (còn được gọi là SOD2) [14]. Theo nghiên cứu, SOD1 đóng một vai trò quan trọng trong việc đẩy nhanh quá trình chuyển đổi gốc tự do superoxide thành H2O2 trong dịch bào. CAT và GPx chứa selen chuyển hóa H2O2 thành nước. Gen SOD 1 được tìm thấy trên nhiễm sắc thể 21 [15] . Bộ ba của nhiễm sắc thể 21, chứa gen SOD-1, gây ra sự mất cân bằng trong tỷ lệ SOD-1 với CAT và GPx, dẫn đến tích tụ H2O2 [5] . Việc tạo ra một lượng lớn H2O2 là do hoạt tính của SOD tăng lên. Các enzym khác, chẳng hạn như CAT, GPx và peroxidase thioredoxin, có thể dễ dàng loại bỏ enzym. Nồng độ H2O2 tăng trong DS không được cân bằng bởi mức CAT và GPx tăng, dẫn đến sản xuất quá mức ROS [16] .
Yếu tố di truyền chịu trách nhiệm chính cho sự khởi phát sớm của AD ở DS. Theo nghiên cứu gần đây, gen kinase 1A (DYRK1A) điều hòa tyrosine-phosphoryl hóa có tính đặc hiệu kép cung cấp hướng dẫn cho sự phát triển hệ thần kinh. Trong DS, nó được thể hiện ở mức độ cao hơn. Sự biểu hiện quá mức của nó có liên quan đến một số thay đổi tế bào và suy giảm nhận thức. Thông qua quá trình tăng phosphoryl hóa tau và cơ chế bệnh sinh amyloid, DYRK1A có thể đóng một vai trò quan trọng trong các bất thường phát triển của não và thoái hóa thần kinh khởi phát sớm [4,17] . Thực tế là số lượng đám rối sợi thần kinh dương tính DYRK1A và 3 lần lặp lại (3R tau) được tăng lên nhiều lần trong DS liên quan đến DYRK1A trong cơ chế bệnh sinh của AD.
Hơn nữa, sự biểu hiện quá mức của DYRK1A dẫn đến tăng phosphoryl hóa APP, làm tăng tốc độ phân cắt protein tiền chất amyloidogenic, nâng cao mức Aβ40 và 42 và bệnh β-amyloidosis ở não. Presenilin 1 (PS1), một protein kích hoạt quan trọng trong căn nguyên của AD, có liên quan đến quá trình này [4] . Ngoài ra, PS1 là thành phần chính của phức hợp γ-secretase, tạo thành Aβ. Hơn nữa, việc ức chế DYRK1A cải thiện hành vi nhận thức ở các mô hình chuột khác nhau của DS. Cuối cùng, một thí nghiệm lâm sàng gần đây cho thấy rằng cho những người trẻ tuổi có DS epigallocatechin gallate (EGCG) (9 mg / kg / ngày), một chất ức chế DYRK1A, giúp tăng cường trí nhớ nhận dạng thị giác, khả năng ghi nhớ làm việc và hành vi thích ứng [17] .
AD khởi phát sớm ở DS chủ yếu do yếu tố di truyền mà còn do yếu tố dinh dưỡng và lối sống: chế độ ăn giàu chất béo và carbohydrate tinh chế làm tăng tích tụ các lớp mảng xơ vữa và tăng cholesterol máu; thiếu hụt vitamin và khoáng chất; và thiếu các hoạt động thể chất và các bài tập nhằm mục đích phát triển tinh thần bình thường [15] .
Chiến lược quản lý
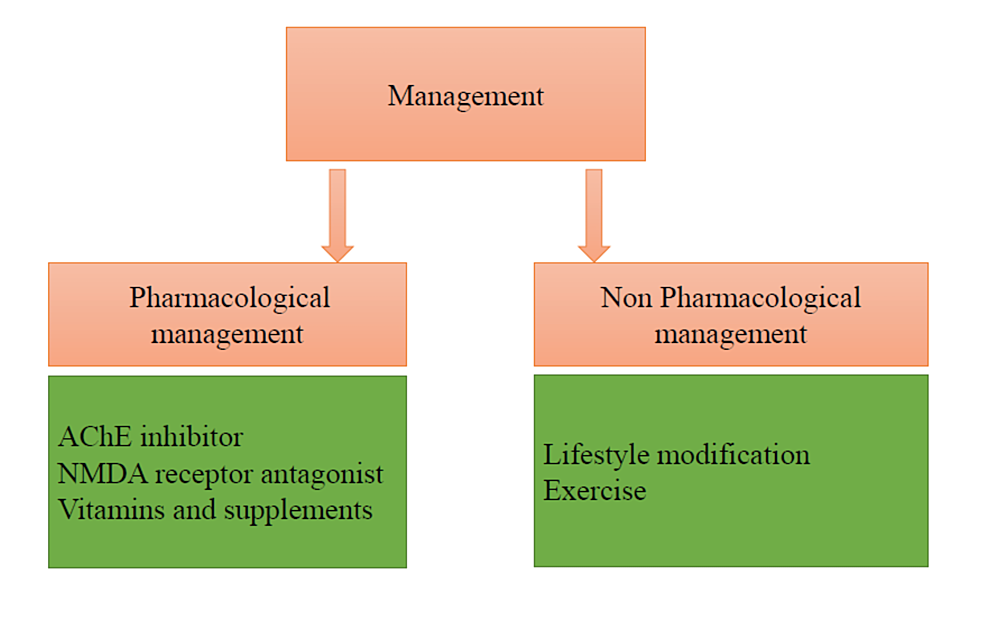
AD là một rối loạn tiến triển và không thể đảo ngược. Hình 2 minh họa các phương pháp tiếp cận dùng thuốc và không dùng thuốc đối với sự tiến triển của chứng sa sút trí tuệ ở AD.
Quản lý dược lý
Chất ức chế acetylcholinesterase (AChE)
Thuốc ức chế AChE, còn được gọi là chất ức chế cholinesterase, là một nhóm thuốc ngăn chặn sự phân hủy bình thường của chất dẫn truyền thần kinh acetylcholine, do đó làm tăng nồng độ của nó ở khớp thần kinh. Acetylcholine đóng một vai trò quan trọng trong học tập, trí nhớ và sự chú ý [18] . Mặc dù các chất ức chế AChE như donepezil, galantamine và rivastigmine được sử dụng như một phương pháp điều trị ở bệnh nhân Alzheimer, tác dụng của chúng vẫn đang được nghiên cứu trên DS. Donepezil và rivastigmine được Cục Quản lý Thực phẩm và Dược phẩm (FDA) phê duyệt [10,19,20] và được dán nhãn cho chứng sa sút trí tuệ nhẹ, vừa và nặng. Galantamine, tuy nhiên, chỉ được chấp thuận cho AD nhẹ và trung bình [10] .
Donepezil là một chất ức chế AChE có thể đảo ngược và chọn lọc được sử dụng để cải thiện hiệu suất nhận thức ở các loại AD nhẹ đến trung bình. Do đó, những người không có DS nhưng bị AD nhẹ đến nặng có thể được hưởng lợi từ donepezil. Mặt khác, những người có DS có xu hướng phát triển AD ở độ tuổi trẻ hơn so với dân số chung và thể chất khác nhau về kích thước, chuyển hóa và nhịp tim; do đó, họ có thể có những nhu cầu khác nhau [18]. Một thử nghiệm ngẫu nhiên có đối chứng so sánh donepezil với một nhóm giả dược bao gồm 30 người bị DS và AD. 16 người nhận được donepezil và 14 người nhận được giả dược. Trong bốn tuần đầu tiên của thử nghiệm, liều lượng là 5 mg donepezil mỗi ngày, sau đó 10 mg mỗi ngày. Thí nghiệm kéo dài trong 24 tuần. Sau khi tìm kiếm kỹ lưỡng, họ phát hiện ra rằng chỉ có một nghiên cứu đủ điều kiện để đưa vào. Không có kết quả có ý nghĩa thống kê cho bất kỳ kết cục nào [18] . Đánh giá này đã được thay thế vào năm 2015 bằng một đánh giá mới [2]. Nghiên cứu đã so sánh hiệu quả của donepezil với nhóm giả dược trong bốn thử nghiệm đối chứng ngẫu nhiên (192 người tham gia). Sau 12-24 tuần, kết quả được tổng kết dựa trên khả năng nhận thức, những khó khăn trong hành vi và những biểu hiện bất lợi. Không có lợi ích rõ ràng, nhưng có nguy cơ dẫn đến kết quả khó chịu [2] . Rối loạn tiêu hóa, tiểu không kiểm soát, yếu cơ [18] và tăng trương lực phế vị của tim dẫn đến nhịp tim chậm [2,12] là một số tác dụng phụ.
Galantamine là một chất ức chế chọn lọc, cạnh tranh và có thể hồi phục nhanh chóng của AChE, làm chậm quá trình phân hủy acetylcholine. Các tác dụng ngoại ý bao gồm rối loạn tiêu hóa [12] .
Rivastigmine là một chất ức chế carbamate có khả năng hồi phục thấp, ức chế cả Butyrylcholinesterase và AChE, không giống như donepezil, nhưng tác dụng của nó kéo dài hơn [12,19] . Nó có khả năng hấp thụ qua da và được sử dụng như một miếng dán thẩm thấu qua da. Nó có thể được sử dụng cho những người bị suy thận hoặc suy gan, và nó không có tương tác với các thuốc khác, vì vậy nó có khả năng hữu ích cho những bệnh nhân mắc các bệnh đồng mắc khác [19] . Một thử nghiệm ngẫu nhiên có đối chứng đã kiểm tra những người tham gia mắc chứng AD trên DS với rivastigmine. Tuy nhiên, sau khi tìm kiếm toàn diện, không có nghiên cứu liên quan nào được tìm thấy để đưa vào [19] . Mặc dù nó có hiệu quả trong việc điều trị AD, nhưng nó đã được chứng minh là làm tổn thương chức năng nhận thức [12]. Ngoài ra, rối loạn tiêu hóa, nhức đầu, chóng mặt [12] , kích ứng da và viêm da tại vị trí dán miếng dán trong da [10] cũng là một số tác dụng phụ khác.
Theo Nhận xét của Cochrane gần đây về donepezil và rivastigmine, không có đủ dữ liệu để đưa ra quyết định mang tính giáo dục về công dụng tiềm năng của các chất ức chế cholinesterase trong điều trị sa sút trí tuệ ở người lớn mắc DS [2,18,19] .
Chất đối kháng thụ thể N-methyl-D-aspartate (NMDA)
Memantine là một chất đối kháng thụ thể NMDA liên kết với thụ thể NMDA và ngăn không cho glutamate liên kết, ngăn canxi xâm nhập vào các tế bào thần kinh. Hai cuộc điều tra trên mô hình chuột DS đã chỉ ra rằng memantine cải thiện chức năng nhận thức và bệnh lý thần kinh ở AD [6] . Bởi vì nghiên cứu tiền lâm sàng cho thấy memantine cải thiện khả năng học tập và trí nhớ ở chuột Ts65Dn, một thử nghiệm ngẫu nhiên, mù đôi, có đối chứng với giả dược đã được thực hiện trên 40 người (từ 18-30 tuổi) để nghiên cứu sự cải thiện chức năng phụ thuộc vào hồi hải mã. Bài kiểm tra học tập bằng lời nói của California-II (CTLV-II), một phép đo kết quả trí nhớ thứ cấp được kết nối với giả thuyết ban đầu, cho thấy hiệu quả đáng kể của 16 tuần điều trị bằng memantine [21] (Bảng 1). Một thử nghiệm ngẫu nhiên, mù đôi, có đối chứng giả dược khác ở những cá nhân có DS từ 40 tuổi trở lên không tìm thấy lợi ích nào từ việc điều trị bằng memantine [6] (Bảng 1 ). Thử nghiệm có 173 người tham gia. Trong số đó, 88 người được dùng memantine và 85 người được dùng giả dược trong 52 tuần. Giải trình tự do máy tính tạo ra và một thuật toán giảm thiểu được sử dụng để đảm bảo phân bổ cân bằng cho năm yếu tố tiên lượng (giới tính, sa sút trí tuệ, nhóm tuổi, tổng số điểm của hội chứng Down, trí nhớ và chức năng điều hành thang điểm [DAMES] và trung tâm.) [6]. Một nghiên cứu khác, một thử nghiệm ngẫu nhiên, mù đôi, có đối chứng với giả dược, sử dụng memantine (20 mg / ngày uống) hoặc giả dược trong 16 tuần trên thanh thiếu niên và thanh niên (15-32 tuổi) với DS, cho thấy không có nhận thức- tác dụng tăng cường [22] (Bảng 1 ). Tổng quan Cochrane [2] đã trích dẫn lợi thế của memantine ở những người bị AD vừa hoặc nặng, những người đã dùng thuốc ức chế men cholinesterase. Vai trò của memantine trong điều trị mất nhận thức ở những người mắc bệnh DS không được chứng minh do các nghiên cứu hạn chế và không kết luận [23] .
Vitamin và chất bổ sung
Bởi vì bệnh nhân có cả DS và AD rất dễ bị OS, các nghiên cứu khác nhau đã được thực hiện trên cả hai nhóm để giảm tổn thương do oxy hóa và cải thiện nhận thức [16] . Trong các thử nghiệm với bệnh mất trí nhớ Alzheimer mức độ nặng và nhẹ đến trung bình, vitamin E liều cao (900 IU), một chất chống oxy hóa, tỏ ra có lợi [2] . Nó là một chất chống oxy hóa phá vỡ chuỗi mạnh mẽ, ngăn chặn việc tạo ra ROS trong quá trình oxy hóa chất béo và sự lây lan của các phản ứng gốc tự do [16] . Các đồng dạng tocopherol và tocotrienol của vitamin E có nhiều phẩm chất khác nhau, bao gồm các đặc tính chống oxy hóa và chống viêm đáng kể, điều biến miễn dịch, tín hiệu tế bào và giảm cholesterol. Nồng độ vitamin E trong máu thấp hơn ở những người bị AD [24]. Một nghiên cứu gần đây đã phát hiện ra vai trò của vitamin E đối với các bệnh tâm thần nhấn mạnh vai trò thiết yếu của nó đối với hoạt động bình thường của não người [16] .
Chu trình homocysteine methionine, bao gồm việc sản xuất S adenosylmethionine, một chất nền quan trọng để methyl hóa deoxyribonucleic acid (DNA), đòi hỏi nhóm vitamin B. Về mặt biểu sinh, sự methyl hóa DNA ảnh hưởng đến sự biểu hiện của gen. Các nghiên cứu dịch tễ học đã liên kết AD với DNA ít bị methyl hóa, dẫn đến sự biểu hiện quá mức của các gen liên quan đến AD. Vitamin B6, B9 và B12 đặc biệt bảo vệ chống lại AD [12] . Ngoài ra, liều lượng cao vitamin B12 và folate đã được chứng minh trong một nghiên cứu duy nhất để làm chậm tốc độ co rút não ở người suy giảm nhận thức nhẹ và mang lại lợi ích nhận thức ở những người có mức homocysteine cao [2]. Tuy nhiên, các kết quả trái ngược từ các nghiên cứu khác cho thấy việc chỉ bổ sung vitamin B không hiệu quả lắm trong việc giảm các triệu chứng giống như sa sút trí tuệ [12] .
Mức vitamin D thấp được tìm thấy ở bệnh nhân AD và có liên quan đến chứng mất trí và thiếu hụt nhận thức. Thông qua liên kết với các thụ thể của chính nó, vitamin D có liên quan đến việc làm sạch mảng bám amyloid, chống viêm, giảm stress oxy hóa và bảo vệ thần kinh [12] .
Chất ức chế DYRK1A
DYRK1A đóng một vai trò quan trọng trong quá trình thoái hóa thần kinh. Hoạt động kinase của DYRK1A bị ức chế bởi hợp chất tự nhiên trong trà xanh EGCG [4,14,25] . EGCG là chất loại bỏ gốc tự do mạnh hơn vitamin E hoặc C [16] . Một phân tích ngẫu nhiên mù đôi các phương pháp điều trị EGCG chống lại giả dược cho thấy sự cải thiện hiệu suất làm việc của trí nhớ ngay lập tức [4] . Một số mô hình chuột DS đã chứng minh những tiến bộ trong nghiên cứu DYRK1A. Tuy nhiên, các nghiên cứu về con người đã bị hạn chế bởi khó khăn trong việc lấy tế bào từ não người. Do đó, chỉ có một số mô hình tế bào người được sử dụng để điều tra vai trò của DYRK1A trong DS [17]. Khi 10 micromolar EGCG được sử dụng chống lại DYRK1A, kết quả cho thấy tăng sinh tế bào và giảm quá trình chết rụng. Các kết quả tích cực đạt được với mô hình chuột DS và gần đây, trong tế bào gốc đa năng của người từ bệnh nhân DS (DS-iPSCs), cho thấy lý do để tin rằng ức chế DYRK1A có thể là một chiến lược khả thi để cải thiện nhận thức ở bệnh nhân DS [17] .
Coenzyme Q10
Coenzyme Q (CoQ) là một chất chống oxy hóa tự nhiên trong cơ thể con người. Nó chống lại hệ điều hành ở bệnh nhân DS bằng cách hoạt động như một trình quét ROS. Một nghiên cứu bao gồm trẻ em mắc bệnh DS để xem CoQ ảnh hưởng như thế nào đến tổn thương DNA khi chúng lớn lên. Họ nhận được liều hàng ngày 4 mg / kg CoQ hoặc giả dược trong sáu tháng. CoQ ngăn ngừa tổn thương oxy hóa đối với DNA pyrimidine ở nhóm tuổi trẻ hơn (5-12 tuổi) và giảm purine bị oxy hóa ở nhóm tuổi lớn hơn (13-17 tuổi) [14,16] . Một thử nghiệm khác, bao gồm bệnh nhân DS từ 5 đến 17 tuổi, được thực hiện trong 20 tháng với CoQ10 4mg / kg / ngày. Họ đã phát hiện ra một số biến thể liên quan đến tuổi trong quá trình oxy hóa DNA [16]. Một nghiên cứu khác cho thấy liệu pháp điều trị dài hạn (tức là 4 năm) với CoQ10 với liều 4 mg / kg / ngày không ảnh hưởng đến quá trình oxy hóa DNA hoặc axit ribonucleic (RNA) ở trẻ em mắc bệnh DS [16,26] .
Quản lý không dùng thuốc
Có rất nhiều phương pháp không dùng thuốc để nâng cao chất lượng cuộc sống cho những người bị sa sút trí tuệ. Ví dụ, người lớn mắc bệnh DS có thể thay đổi lối sống, thói quen ăn uống lành mạnh, hoạt động thể chất thường xuyên và phục hồi nhận thức để cải thiện khả năng nhận thức.
Sửa đổi lối sống
Một lối sống lành mạnh là rất quan trọng. Các can thiệp thúc đẩy thói quen ăn uống lành mạnh và bổ dưỡng giúp cải thiện sức khỏe tổng thể của bệnh nhân AD [16] . Các biến số dinh dưỡng đóng một vai trò nhất định vào thời kỳ đầu của AD ở những người có DS. Ví dụ, một chế độ ăn nhiều lipid và carbohydrate chuỗi thẳng sẽ thúc đẩy sự hình thành mảng xơ vữa động mạch và tăng cholesterol kết hợp với sự thiếu hụt vitamin và khoáng chất. Rối loạn chức năng nhiễm sắc thể 21 ở các đối tượng DS tương quan thuận với các cấu hình lipid bất lợi như chất béo trung tính cao, mức lipoprotein mật độ cao thấp và mức độ leptin cao [15]. Để làm chậm AD ở người mắc bệnh DS, cha mẹ nên cung cấp thực phẩm lành mạnh giàu vitamin, đặc biệt là vitamin E (chất chống oxy hóa), vitamin nhóm B, khoáng chất (đặc biệt là magiê), chất xơ và axit béo omega-3 [16] .
Tập thể dục
Hoạt động thể chất có thể là một phương pháp điều trị không dùng thuốc hiệu quả để ngăn ngừa và quản lý chứng sa sút trí tuệ. Theo một nghiên cứu, tăng cường hoạt động thể chất có thể rất quan trọng đối với việc duy trì các thành phần nhận thức như sự chú ý, trí nhớ và chức năng điều hành ở những người bị AD [27,28] . Tăng cường hoạt động thể chất cũng có thể giúp ngăn ngừa hoặc trì hoãn sự khởi phát AD bằng cách tăng thể tích hồi hải mã, cải thiện tưới máu não, tạo điều kiện thuận lợi cho quá trình hình thành thần kinh và synapto, đồng thời làm giảm thuận lợi các thay đổi bệnh lý như tích tụ Aβ [27] . Nghiên cứu thuần tập với những người có DS đã được thực hiện để xem xét mối quan hệ giữa tập thể dục thể chất và những thay đổi trong nhận thức và chức năng liên quan đến sa sút trí tuệ [1]. Hai trăm mười bốn người trưởng thành mắc chứng DS không bị sa sút trí tuệ đã được thu thập thông tin nhân khẩu học, lối sống và sức khỏe của họ ở mức ban đầu, sau đó là một cuộc theo dõi hai năm. Đánh giá liên quan đến việc sử dụng Kỳ thi Cambridge dành cho Rối loạn Tâm thần của Người lớn tuổi mắc Hội chứng Down và Những Người bị Khuyết tật Trí tuệ (CAMDEX-DS) và phân tích di truyền. Trong khi điều chỉnh các biến có liên quan, các mô hình hồi quy logistic đã được sử dụng để điều tra các mối tương quan tiềm năng giữa sự sụt giảm trong các miền CAMDEX-DS và việc tập thể dục. Ở mức cơ bản, tập thể dục cường độ vừa phải làm giảm nguy cơ suy giảm kỹ năng hàng ngày xuống 47%. Ngược lại, tập thể dục cường độ cao làm giảm nguy cơ nhân cách và hành vi giảm xuống 62%. Sau đó, mức độ tập thể dục cao làm giảm nguy cơ suy giảm nhân cách và hành vi xuống 87%. Ở cơ sở,[1] (Bảng 1 ). Một thử nghiệm ngẫu nhiên để đánh giá những thay đổi trong chức năng nhận thức sau khi hoàn thành can thiệp tập thể dục kéo dài 12 tuần được tiến hành từ xa thông qua hội nghị truyền hình trên máy tính bảng [28] do các vấn đề liên quan đến nhiều rào cản như hỗ trợ xã hội, nhu cầu người chăm sóc, tài chính gánh nặng và vận chuyển. Chức năng nhận thức sau 12 tuần được cải thiện so với lúc ban đầu (Bảng 1 ) [28] . Một thử nghiệm ngẫu nhiên khác kéo dài 12 tháng [27] cho thấy rằng hoạt động thể chất vừa phải đến mạnh (MVPA) đã cải thiện hiệu suất nhận thức và chất lượng cuộc sống ở bệnh nhân DS mắc AD (Bảng 1 ).
Bản tóm tắt của can thiệp được sử dụng để xác định hiệu quả của các chiến lược quản lý và kết quả của chúng được minh họa dưới đây trong Bảng 1 .
Hạn chế
Hạn chế chính của tổng quan này là không có đủ bằng chứng về vai trò của các liệu pháp dược phẩm trong việc quản lý chứng sa sút trí tuệ ở những người mắc bệnh DS. Cần có một dân số đáng kể với nhiều năng lượng hơn để nghiên cứu. Bài viết đánh giá này đề cập đến mối liên hệ tích cực giữa tập thể dục và cải thiện chức năng nhận thức nhưng không cung cấp rõ ràng hơn về việc sử dụng vitamin và chất bổ sung.
Kết luận
Tổng quan này tập trung vào sinh lý bệnh và các lựa chọn điều trị, bao gồm các lựa chọn dùng thuốc và không dùng thuốc trong việc giảm sự tiến triển của chứng sa sút trí tuệ ở những người mắc bệnh DS. Sự biểu hiện quá mức của APP dường như là một thành phần quan trọng trong việc phát triển bệnh Alzheimer ở những người mắc bệnh DS. Trong bối cảnh của các phát hiện được báo cáo đã thảo luận ở trên, các liệu pháp dược lý như Donepezil và Memantine có thể có vai trò trong việc kiểm soát chứng sa sút trí tuệ; tuy nhiên, nghiên cứu với nhiều người có DS là cần thiết. Những người có DS có khuynh hướng bị stress oxy hóa và tổn thương DNA sau đó. Vitamin E, chất ức chế DYRK1A và CoQ là những chất chống oxy hóa giúp người mắc bệnh DS chống lại stress oxy hóa. Có mối liên hệ tích cực giữa tập thể dục thường xuyên và việc duy trì trí nhớ, tính cách, hành vi, và khả năng trò chuyện trong nhận thức và chức năng liên quan đến sa sút trí tuệ ở người lớn mắc bệnh DS. Có rất ít bằng chứng về điều trị dược lý thích hợp đối với chứng suy giảm nhận thức và sa sút trí tuệ ở những người mắc hội chứng Down. Do đó, các nghiên cứu sâu hơn nên tập trung vào các thử nghiệm rộng rãi hơn với các nhóm thuần tập được hỗ trợ tốt để khám phá việc ngăn ngừa suy giảm nhận thức trong dân số DS.
Người giới thiệu
- Pape SE, Baksh RA, Startin C, Hamburg S, Hithersay R, Strydom A: Mối liên quan giữa hoạt động thể chất và những thay đổi CAMDEX-DS trước khi bắt đầu bệnh Alzheimer trong Hội chứng Down . J Clin Med. 2021, 10: 10,3390 / jcm10091882
- Livingstone N, Hanratty J, McShane R, Macdonald G: Các can thiệp bằng dược lý đối với sự suy giảm nhận thức ở những người mắc hội chứng Down . Cơ sở dữ liệu Cochrane Syst Rev. 2015, CD011546. 10.1002 / 14651858.CD011546.pub2
- Malakooti N, Pritchard MA, Adlard PA, Finkelstein DI: Vai trò của các ion kim loại trong sự suy giảm nhận thức của hội chứng Down . Tế bào thần kinh lão hóa phía trước. 2014, 6: 136. 10.3389 / fnagi.2014.00136
- de la Torre R, Dierssen M: Các phương pháp trị liệu trong việc cải thiện hoạt động nhận thức trong hội chứng Down: quá khứ, hiện tại và tương lai . Prog Brain Res. 2012, 197: 1-14. 10.1016 / B978-0-444-54299-1.00001-7
- Perluigi M, Butterfield DA: Căng thẳng oxy hóa và hội chứng Down: một con đường dẫn đến chứng mất trí nhớ giống Alzheimer . Curr Gerontol Geriatr Res. 2012, 2012: 724904. 10.1155 / 2012/724904
- Hanney M, Prasher V, Williams N và cộng sự: Memantine điều trị chứng sa sút trí tuệ ở người lớn trên 40 tuổi mắc hội chứng Down (MEADOWS): một thử nghiệm ngẫu nhiên, mù đôi, có đối chứng với giả dược. Các . Cây thương. 2012, 379: 528-36. 10.1016 / S0140-6736 (11) 61676-0
- Puttagunta SM, Islam R, Kundu S. Cureus. 2022, 14: e22125. 10.7759 / Cureus.22125
- Priebe GA, Kanzawa MM: Giảm sự tiến triển của bệnh Alzheimer ở bệnh nhân hội chứng Down với lithium liều vi lượng . Giả thuyết về Med. 2020, 137: 109573. 10.1016 / j.mehy.2020.109573
- Castro P, Zaman S, Holland A: Bệnh Alzheimer ở những người mắc hội chứng Down: triển vọng và thách thức của việc phát triển các phương pháp điều trị phòng ngừa . J Neurol. 2017, 264: 804-13. 10.1007 / s00415-016-8308-8
- Atri A: Phổ lâm sàng của bệnh Alzheimer: chẩn đoán và quản lý . Med Clin Bắc Am. 2019, 103: 263-93. 10.1016 / j.mcna.2018.10.009
- Jeremic D, Jiménez-Díaz L, Navarro-López JD: Quá khứ, hiện tại và tương lai của các chiến lược điều trị chống lại peptide amyloid-β trong bệnh Alzheimer: một đánh giá có hệ thống . Aging Res Rev. 2021, 72: 101496. 10.1016 / j.arr.2021.101496
- Ghosh S, Durgvanshi S, Agarwal S, Raghunath M, Sinha JK: Tình trạng hiện tại của mục tiêu thuốc và các chiến lược điều trị mới nổi trong quản lý bệnh Alzheimer . Curr Neuropharmacol. Năm 2020, 18: 883-903. 10.2174 / 1570159X18666200429011823
- Kloske CM, Wilcock DM: Giao diện quan trọng giữa apolipoprotein E và chứng viêm thần kinh trong bệnh Alzheimer . Immunol phía trước. Năm 2020, 11: 754. 10.3389 / fimmu.2020.00754
- Muchová J, Žitňanová I, Ďuračková Z: Căng thẳng oxy hóa và hội chứng Down. Chất chống oxy hóa có đóng một vai trò nào đó trong liệu pháp không? . Physiol Res. 2014, 63: 535-42. 10.33549 / Physolres.932722
- Mazurek D, Wyka J: Hội chứng Down-các khía cạnh di truyền và dinh dưỡng của các rối loạn kèm theo . Biên niên sử của Viện Vệ sinh Quốc gia. 2015, 66: 875614.
- Ravancic ME, Obradovic V: Sử dụng các chất bổ sung dinh dưỡng cho người mắc hội chứng Down . Tiến bộ trong Dinh dưỡng. 2021, 23: 10.23751 / pn.v23i3.9335
- Feki A, Hibaoui Y: Protein DYRK1A, một mục tiêu điều trị đầy hứa hẹn để cải thiện sự thiếu hụt nhận thức trong hội chứng Down . Khoa học trí não. 2018, 8: 10.3390 / brainsci8100187
- Mohan M, Carpenter PK, Bennett C: Donepezil cho bệnh mất trí nhớ ở những người mắc hội chứng Down . Cơ sở dữ liệu Cochrane Syst Rev. 2009, CD007178. 10.1002 / 14651858.CD007178.pub2
- Mohan M, Bennett C, Carpenter PK: Rivastigmine cho bệnh mất trí nhớ ở những người mắc hội chứng Down . Cơ sở dữ liệu Cochrane Syst Rev. 2009, CD007658. 10.1002 / 14651858.CD007658
- Stephens MM, Herge E, Wright C: Hội chứng Down và sa sút trí tuệ: Phương pháp tiếp cận lấy bệnh nhân và người chăm sóc làm trung tâm . Dela J Y tế công cộng. Năm 2021, 7: 128-30. 10.32481 / djph.2021.09.016
- Boada R, Hutaff-Lee C, Schrader A, Weitzenkamp D, Benke TA, Goldson EJ, Costa AC: Sự đối kháng của các thụ thể NMDA như một phương pháp điều trị tiềm năng cho hội chứng Down: một thử nghiệm ngẫu nhiên có đối chứng . Dịch Tâm thần học. 2012, 2: 141.
- Costa AC, Brandão AC, Boada R, et al: An toàn, hiệu quả và khả năng dung nạp của memantine đối với các biện pháp kết quả nhận thức và thích ứng ở thanh thiếu niên và thanh niên mắc hội chứng Down: một thử nghiệm giai đoạn 2 ngẫu nhiên, mù đôi, có đối chứng với giả dược . Lancet Neurol. 2022, 1: 31-41. 10.1016 / S1474-4422 (21) 00369-0
- Mohan M, Bennett C, Carpenter PK: Memantine điều trị chứng mất trí nhớ ở những người mắc hội chứng Down . Cơ sở dữ liệu Cochrane Syst Rev. 2009, CD007657. 10.1002 / 14651858.CD007657
- Browne D, McGuinness B, Woodside JV, McKay GJ: Vitamin E và bệnh Alzheimer: chúng ta biết gì cho đến nay? . Clin Interv Lão hóa. 2019, 14: 1303-17. 10.2147 / CIA.S186760
- Franceschi C, Garagnani P, Gensous N, Bacalini MG, Conte M, Salvioli S: Tăng tốc độ lão hóa nhận thức sinh học trong hội chứng Down: Hiện đại và các chiến lược giảm tốc có thể có . Tế bào Lão hóa. 2019, 18: e12903. 10.1111 / acel.12903
- Larsen EL, Padella L, Bergholdt HK, và cộng sự: Ảnh hưởng của việc điều trị lâu dài bằng coenzyme Q10 đối với sự thay đổi axit nucleic bằng quá trình oxy hóa ở trẻ em mắc hội chứng Down . Lão hóa thần kinh. 2018, 67: 159-61. 10.1016 / j.neurobiolaging.2018.03.001
- Ptomey LT, Szabo-Reed AN, Martin LE, et al: Việc thúc đẩy hoạt động thể chất để ngăn ngừa bệnh Alzheimer ở người lớn mắc hội chứng Down: Cơ sở và thiết kế cho một thử nghiệm ngẫu nhiên 12 tháng . Xem thử Clin Thử nghiệm Commun. 2020, 19: 100607. 10.1016 / j.conctc.2020.100607
- Ptomey LT, Szabo AN, Willis EA, Gorczyca AM, Greene JL, Danon JC, Donnelly JE: Những thay đổi về chức năng nhận thức sau can thiệp tập thể dục kéo dài 12 tuần ở người lớn mắc hội chứng Down . Disabil Health J. 2018, 11: 486-90. 10.1016 / j.dhjo.2018.02.003