Nhắm mục tiêu trục endothelin như một chiến lược điều trị cho di căn và đau của ung thư miệng

- Dongmin Dang ,
- Yi Ye ,
- Bradley E. Aouizerat ,
- Yogin K. Patel ,
- Dân T. Việt ,
- Vua Chong Chan ,
- Kentaro Ono ,
- Coleen Doan ,
- Johnny D. Figueroa ,
- Gary Yu &
- Chi T. Viet
trừu tượng
Di căn làm giảm khả năng sống sót ở bệnh nhân ung thư miệng và đau đớn là điều họ phàn nàn nhiều nhất. Trước đây chúng tôi đã chỉ ra rằng sự di căn và đau của ung thư miệng được kiểm soát bởi trục endothelin, là một con đường bao gồm các thụ thể endothelin A và B (ET A R và ET B R). Trong nghiên cứu này, chúng tôi tập trung vào các gen riêng lẻ của con đường, chứng minh rằng các gen trục endothelin bị methyl hóa và rối loạn điều hòa trong mô ung thư. Dựa trên những phát hiện này ở bệnh nhân, chúng tôi đưa ra giả thuyết rằng ET A R và ET B R đóng vai trò phân đôi trong sinh ung thư miệng và đau, như vậy ET A R kích hoạt và ET B im lặng.Biểu hiện R dẫn đến tăng sinh ung thư và đau. Chúng tôi thử nghiệm một chiến lược điều trị nhắm vào các chức năng phân đôi của hai thụ thể bằng cách ức chế ET A R với macitentan, một chất đối kháng ET A R đã được phê duyệt để điều trị tăng áp động mạch phổi và biểu hiện lại gen ET B R với sự tải nạp adenovirus và xác định tác dụng điều trị đối với sự xâm lấn của ung thư (tức là di căn), sự tăng sinh và giảm đau trong ống nghiệm và in vivo. Chúng tôi chứng minh rằng điều trị kết hợp giữa macitentan và ET BLiệu pháp gen R ức chế sự xâm lấn, nhưng không tăng sinh, trong nuôi cấy tế bào và trên mô hình chuột bị ung thư lưỡi. Hơn nữa, sự kết hợp điều trị tạo ra tác dụng chống ung thư thông qua việc ức chế kích hoạt tế bào thần kinh qua trung gian endothelin-1, tiết lộ tiềm năng giảm đau của macitentan. Phương pháp điều trị của chúng tôi nhắm đến một lộ trình được chứng minh là không được kiểm soát ở bệnh nhân ung thư miệng, sử dụng liệu pháp gen và thay thế một loại thuốc có sẵn để điều trị hiệu quả cả di căn và đau của ung thư miệng trong mô hình tiền lâm sàng.
Giới thiệu
Bất chấp những tiến bộ liên tục trong việc phát triển liệu pháp nhắm mục tiêu, bệnh nhân ung thư biểu mô tế bào vảy ở miệng (SCC) vẫn tiếp tục chịu đau đớn và sống sót kém. Điều trị thất bại dẫn đến tái phát hoặc di căn. Những bệnh nhân thất bại trong việc điều trị sẽ phải chịu đựng những cơn đau do ung thư gây ra. Bệnh nhân SCC đường miệng bị đau nhiều hơn đáng kể so với các bệnh nhân ung thư khác 1 . Chúng tôi và những người khác đã chỉ ra rằng di căn tương quan với tăng đau và chức năng vận động kém 2 , 3. Trong nghiên cứu này, chúng tôi đề xuất rằng mối tương quan lâm sàng giữa tăng sinh SCC miệng, di căn và đau là hậu quả của một con đường phân tử chung liên quan đến tín hiệu giữa các tế bào ung thư và các dây thần kinh xung quanh. Chúng tôi khám phá một con đường như vậy có tên là trục endothelin. Trục endothelin bao gồm các yếu tố sau: (1) ba dạng đồng phân của hormone peptide endothelin (ET-1, ET-2 và ET-3), (2) hai thụ thể liên kết với protein G riêng biệt (ET A R và ET B R ), và (3) các enzym chuyển đổi ET (ECE-1 và ECE-2), kích hoạt các dạng pro của peptit. Nghiên cứu trước đây từ phòng thí nghiệm của chúng tôi về các gen trục endothelin đã chứng minh rằng EDNRB, gen ET BR, được làm im lặng bởi quá trình methyl hóa trong mô SCC miệng của bệnh nhân. Hơn nữa, quá trình methyl hóa EDNRB tương quan với di căn cổ ở bệnh nhân SCC đường uống. Sự tái hiện EDNRB trên tế bào ung thư tạo ra chất chống ung thư thông qua bài tiết opioid nội sinh. Ngược lại, việc kích hoạt ET A R bởi ET-1 tạo ra khả năng thụ thai ung thư miệng và sự đối kháng ET A R ức chế sự thụ thai trong mô hình SCC miệng 4 , 5 của chuột .
Our findings thus far in patient tissues and preclinical models suggest that the endothelin axis genes play an important role in oral SCC invasion and pain. However what remains unknown is the distinct contribution of each endothelin axis component to cancer neuron signaling, and ultimately, to cancer invasion, proliferation and pain. Furthermore, a treatment strategy targeting the multiple dysregulated components of the pathway at the same time, has yet to be developed. In this study we hypothesize that the cancer cell employs endothelin axis gene dysregulation, specifically ETBR gene silencing and ETAR gene overexpression, to mediate processes of invasion, proliferation, and pain. We first confirm dysregulation of these endothelin axis genes in oral SCC tissues from patients. Next, we develop a treatment strategy involving inhibition of ETAR with macitentan, an ETAR antagonist approved for treatment of pulmonary hypertension, and re-expression of the ETBR gene with adenoviral gene therapy. We determine the efficacy of this strategy in treating cancer invasion, proliferation, and pain using in vitro and preclinical models.
Results
Endothelin pathway genes are dysregulated in human oral SCC tissues
Sự liên quan lâm sàng của một con đường gen liên quan đến việc chứng minh sự rối loạn điều hòa của nó trong bệnh tật ở người. Sau khi xác định được trong một nhóm riêng biệt gồm các bệnh nhân SCC đường miệng rằng EDNRB bị hypermethyl hóa và im lặng trong mô ung thư, nhưng không phải là mô bình thường bên cạnh 1 , chúng tôi đã mở rộng trọng tâm để xác định mức độ rối loạn điều hòa trong các gen trục endothelin còn lại. Chúng tôi đã định lượng ECE1, ECE2, EDN1, EDNRA và EDNRB methyl hóa và biểu hiện gen với dữ liệu mảng từ một nhóm riêng biệt gồm 22 bệnh nhân SCC đường miệng . Những phát hiện quan trọng của chúng tôi như sau: (1) có mối quan hệ nghịch đảo giữa EDNRA và biểu thức EDNRB ( p = 0.02, EDNRB_ILMN_1751904 vs EDNRA_ILMN_1796629), và (2) sự biểu hiện của ECE1 và ECE2 được tương quan nghịch với methyl, ví dụ , mẫu hypermethylated có biểu hiện gen thấp (Hình. 1 ). Vị trí CpG ECE1 cg19273683 có tương quan nghịch (r = −0,4985, p = 0,0417) với mức mRNA của ECE1. Sử dụng phân tích hồi quy tuyến tính, chúng tôi nhận thấy rằng cứ tăng 10% sự methyl hóa vị trí CpG, thì biểu hiện của ECE1 giảm 0,0832 đơn vị (KTC 95%: – 0,1629, – 0,0036; p = 0,042). Sự metyl hóa ECE2 CpG có tương quan nghịch với các mức bảng điểm ECE2 1 (NM_014693.2, ECE2_ILMN_1787185; r = – 0,5290, p = 0,0290). Cứ tăng 10% sự metyl hóa vị trí CpG, thì sự biểu hiện của ECE2 giảm đi 0,0377 đơn vị (KTC 95%: – 0, 0710, – 0,0044; p = 0,029). Tổng hợp lại, những phát hiện của chúng tôi ở mô bệnh nhân cho thấy biểu hiện EDNRA và EDRB có quan hệ nghịch với nhau, và EDNRB, ECE1 và ECE2 bị rối loạn điều hòa bởi quá trình methyl hóa trong SCC đường uống.
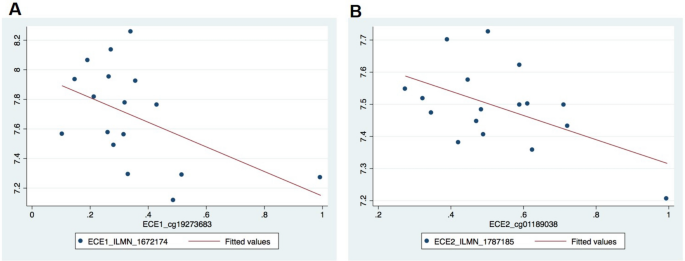
Mô hình hồi quy tuyến tính của ECE1 và ECE2 methyl hóa và biểu thức. Trục x biểu thị quá trình metyl hóa trung bình; trục y biểu thị mức biểu thức trung bình. Có mối quan hệ nghịch đảo giữa ( A ) ECE1 và ( B ) ECE2 methyl hóa ở vị trí CpG được phân tích và mức phiên mã gen ( ECE1 r = – 0,4985, p = 0,0417, ECE2 ; r = – 0,5290, p = 0,0290). Cứ mỗi 10% tăng methyl hóa vị trí CpG, thì sự biểu hiện của ECE1 giảm đi 0,0832 đơn vị (KTC 95%: – 0,1629, – 0,0036; p = 0,042). Cứ tăng 10% sự methyl hóa vị trí CpG, thì sự biểu hiện của ECE2 giảm đi 0,0377 đơn vị (KTC 95%: – 0, 0710, – 0,0044; p = 0,029).
Điều trị kết hợp giữa liệu pháp gen macitentan và EDNRB ức chế sự xâm lấn của ung thư miệng trong ống nghiệm
Ba biến kết quả mà chúng tôi đo lường trong nghiên cứu này là xâm lấn (tức là di căn), tăng sinh và đau, trong đó di căn có ảnh hưởng đáng kể nhất đến sự sống còn tổng thể của bệnh nhân 2 . Đầu tiên, chúng tôi xác định liệu chiến lược điều trị của chúng tôi là ức chế ET A R bằng macitentan và tái biểu hiện EDNRB (gen ET B R) có thể ngăn chặn hiệu quả sự xâm lấn của ung thư trong ống nghiệm và trong một mô hình tiền lâm sàng của SCC đường miệng. Mô hình xâm lấn in vitro được thiết lập với Hela-O3, một dòng tế bào có tiềm năng xâm lấn cao 3 . Chúng tôi đã chỉ ra rằng macitentan ức chế sự xâm nhập của Hela-O3 theo cách phụ thuộc vào liều lượng so với việc kiểm soát phương tiện (Hình 2A). Chúng tôi đã tính toán giá trị IC50 (liều cần thiết để ức chế sự xâm nhập 50%) bằng cách so sánh phần trăm ức chế đối với các liều được sử dụng trong Hình 2 A. IC50 cho macitentan là 4,6 µM (Hình 2 B) .
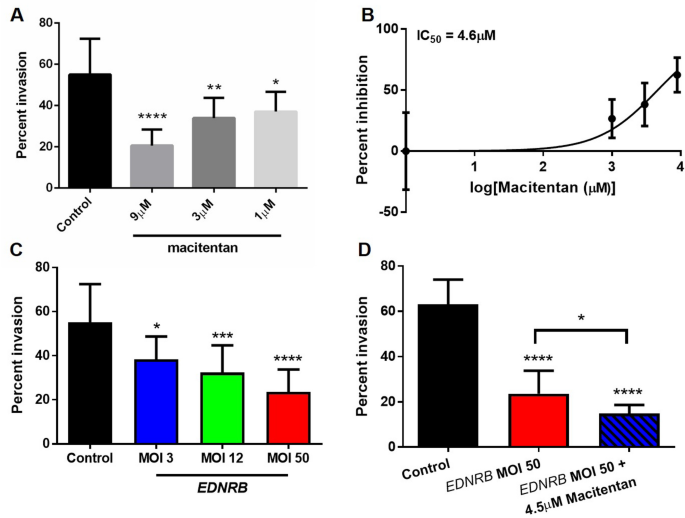
Macitentan ức chế sự xâm nhập của Hela-O3 trong ống nghiệm. ( A ) Sự xâm nhập của Hela-O3 giảm đáng kể khi điều trị macitentan phụ thuộc vào liều lượng (ANOVA một chiều, thử nghiệm Holm Sidak, * p <0,05, ** p <0,01, **** p <.0001 , so với đối chứng). ( B ) Đường cong đáp ứng liều macitentan dựa trên các liều được sử dụng trong Hình 1 A chứng minh rằng giá trị IC50 là 4,6 µM. ( C ) Sự truyền tải vi rút Ad-EDNRB ức chế sự xâm nhập của Hela-O3 theo cách phụ thuộc vào liều lượng (ANOVA một chiều, thử nghiệm Holm Sidak, * p <0,05, *** p <0,001, **** p <.0001 ). ( D) điều trị kết hợp Ad-EDNRB và macitentan ở liều IC50 có hiệu quả hơn trong việc ức chế sự xâm nhập của Hela-O3 so với đối chứng (ANOVA một chiều, thử nghiệm Holm Sidak, **** p <.0001) hoặc điều trị Ad-EDNRB đơn thuần (* p <.05).
Tiếp theo, chúng tôi xác định xem liệu tải nạp EDNRB đơn thuần có ức chế sự xâm nhập của Hela-O3 hay không, so với các tế bào kiểm soát được chuyển nạp bằng GFP. Chúng tôi xác định rằng liệu pháp gen EDNRB ức chế đáng kể sự xâm nhập của Hela-O3 so với đối chứng, ở MOI 3, 12 và 50 (Hình 2 C). Hơn nữa, liệu pháp gen EDNRB ức chế sự xâm nhập của Hela-O3 theo cách phụ thuộc vào liều lượng, với MOI cao hơn tạo ra tác dụng ức chế sự xâm nhập mạnh hơn. Sự truyền EDNRB ở MOI 50 tạo ra tác dụng ức chế mạnh nhất đối với sự xâm nhập mà không làm chết tế bào đáng kể (được xác định thông qua các thí nghiệm sơ bộ ở liều MOI cao hơn). Cuối cùng, chúng tôi đã thử nghiệm sự kết hợp của EDNRBdẫn truyền ở MOI 50 và macitentan ở 4,5 µM. Chúng tôi cho thấy rằng điều trị kết hợp tạo ra tác dụng ức chế sự xâm lấn mạnh hơn so với điều trị kiểm soát hoặc liệu pháp gen EDNRB đơn thuần (Hình 2 D).
Điều trị kết hợp giữa liệu pháp gen macitentan và EDNRB ức chế sự di căn của ung thư miệng đến các hạch bạch huyết cổ tử cung
Tiếp theo, chúng tôi xác định liệu điều trị kết hợp với liệu pháp gen EDNRB và macitentan có ức chế di căn cổ trong mô hình SCC lưỡi chuột được thiết lập bằng cách sử dụng dòng tế bào Hela-O3 hay không. Chuột được theo dõi về sự giảm cân theo quy trình động vật của chúng tôi; không có con chuột nào trong bất kỳ nhóm thí nghiệm nào bị sụt cân đáng kể (tức là hơn 15%) trong suốt thời gian thí nghiệm. Hình ảnh ung thư lưỡi và các hạch cổ tử cung được thực hiện sau 21 ngày bằng máy phân tích sinh học Xenogen IVIS Lumina II (Hình 3A). Di căn cổ tử cung được định lượng cho mỗi nhóm điều trị, với ba phần được xem xét trên mỗi con chuột. Đối với tất cả các động vật có di căn nút cổ tử cung trong một phần, chúng tôi cũng thấy sự hiện diện của di căn trong hai phần được phân tích bổ sung (Hình 3 B). Tỷ lệ di căn cổ tử cung là 46% đối với nhóm Ad-GFP / xe đối chứng (n = 13), 21% đối với nhóm Ad-GFP / macitentan (n = 14), 29% đối với Ad-EDRNB / nhóm xe ( n = 14) và 0% cho nhóm Ad-EDNRB / macitentan (n = 14). Nhóm điều trị phối hợp (Ad-EDNRB / macitentan) có tỷ lệ di căn thấp hơn đáng kể so với nhóm chứng (Ad-GFP / xe) với p = 0,006. Các nhóm được điều trị bằng EDNRBchuyển gen hoặc macitentan đơn thuần không khác biệt đáng kể so với nhóm chứng (Bảng 1 ).
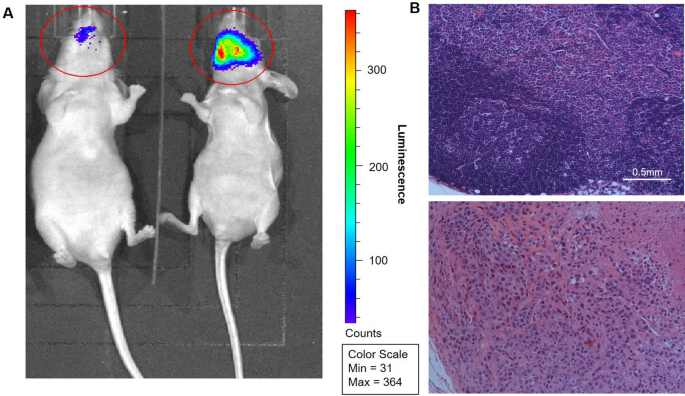
Hình ảnh đại diện cho thấy sự khác biệt về mô hình di căn giữa các nhóm điều trị. ( A ) Hình ảnh phát quang sinh học thu được bằng máy phân tích sinh học Xenogen IVIS Lumina II cho phép định lượng thể tích khối u và xác định di căn cổ tử cung, với hai hình ảnh đại diện được hiển thị ở đây: một con chuột có SCC lưỡi không di căn (trái) và một con có SCC lưỡi với di căn cổ tử cung ( đúng). Tổng tín hiệu phát quang được tính toán cho từng vùng quan tâm (hiển thị dưới dạng vòng tròn màu đỏ); tổng tín hiệu ở con chuột bên trái thấp hơn con bên phải (9,47 × 10 3 so với 8,37 × 10 4 ). ( B) Các mẫu vật bóc tách cổ hai bên được xử lý và nhuộm bằng hematoxylin và eosin (H&E), với hình ảnh hiển thị ở 10x, chứng minh cấu trúc hạch bạch huyết bình thường đối với chuột không có di căn cổ tử cung trên hình ảnh phát quang sinh học và các tế bào ung thư biểu mô di căn và hoại tử trung tâm của hạch bạch huyết cho chuột bị di căn cổ tử cung.
Điều trị kết hợp giữa liệu pháp gen macitentan và EDNRB không ảnh hưởng đến sự tăng sinh ung thư miệng in vitro hoặc in vivo
Tiếp theo, chúng tôi tập trung vào sự gia tăng. Chúng tôi đã chỉ ra rằng liệu pháp gen EDNRB đơn thuần không tạo ra tác dụng chống tăng sinh trong SCC đường miệng in vitro hoặc in vivo 1 . Tại đây, chúng tôi xác định liệu liệu pháp gen EDNRB kết hợp và macitentan có ức chế sự tăng sinh trong ống nghiệm hay không. Tế bào Hela-O3 được chuyển nạp bằng EDNRB hoặc GFP, sau đó được xử lý bằng macitentan. IC50 của macitentan là 2,30 × 10 –8 M đối với tế bào Hela-O3- GFP và 2,18 × 10 –8 M đối với tế bào Hela-O3- EDNRB (Hình 4A), không khác biệt đáng kể, cho thấy điều trị kết hợp không tạo ra tác dụng chống tăng sinh đáng kể. Xét nghiệm MTS được sử dụng như một xét nghiệm tăng sinh bổ sung, và cũng không cho thấy sự khác biệt về khả năng tăng sinh giữa nhóm đối chứng, chỉ điều trị gen EDNRB , chỉ macitentan và nhóm điều trị kết hợp (Hình 4 B).
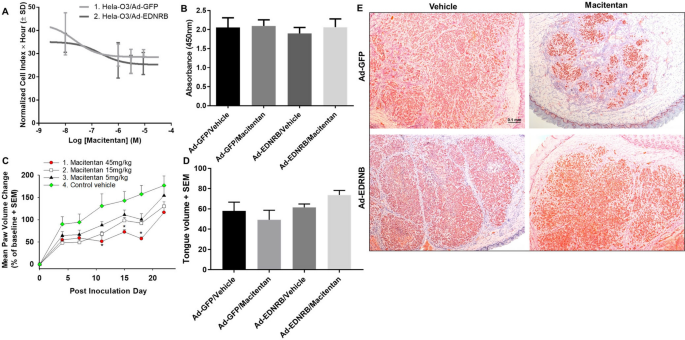
Điều trị bằng Macitentan và sự tái biểu hiện EDNRB không có ảnh hưởng đáng kể đến sự tăng sinh trong ống nghiệm hoặc trên mô hình chuột . ( A ) Hai biểu đồ hiển thị nồng độ macitentan so với diện tích dưới đường cong (AUC) cho các nhóm Ad-GFP và Ad-EDNRB trong một thử nghiệm RTCA trong thời gian 72 giờ, với AUC từ giờ 45 đến 64 so với log10 của nồng độ macitentan được hiển thị . Sự tái biểu hiện EDNRB trên tế bào Hela-O3 không tạo ra ảnh hưởng đáng kể đến sự tăng sinh so với Hela-O3 / GFP đối chứng. ( B) Kết quả của xét nghiệm MTS trong đó độ hấp thụ được định lượng như chỉ số tăng sinh chứng tỏ không có sự khác biệt về độ hấp thụ giữa các nhóm xử lý. Truyền Ad-EDNRB và điều trị macitentan ở liều IC50 không tạo ra tác dụng chống tăng sinh đáng kể trên tế bào Hela-O3. ( C ) Biểu đồ cho thấy sự thay đổi về khối lượng bàn chân so với đường cơ sở. Trong khi điều trị macitentan ở liều cao nhất (45 mg / kg) tạo ra tác dụng chống tăng sinh giữa PID 11 và PID18 trong mô hình ung thư HSC-3 có chân, tác dụng này không duy trì (n = 8 chuột cái mỗi lần điều trị; * p <0,05, ANOVA một chiều, thử nghiệm Holm Sidak). Khi so sánh toàn bộ thời gian thử nghiệm của mỗi nhóm điều trị bằng RM ANOVA hai chiều, có sự khác biệt đáng kể giữa điều trị macitentan 15 mg / kg và 45 mg / kg so với nhóm đối chứng (xem Bảng 2 để biết tóm tắt thống kê) , tuy nhiên, khi mỗi mốc thời gian được phân tích riêng biệt, điều trị macitentan không có tác dụng chống tăng sinh bền vững. ( D ) Kết hợp truyền Ad-EDNRB và điều trị macitentan trong ung thư Hela-O3 ở lưỡi không tạo ra tác dụng chống tăng sinh đáng kể so với điều trị kiểm soát (thanh đen, liệu pháp gen GFP và phương tiện). ( E) Nhuộm sắc tố Ki-67 (được thấy trong các hình ảnh chụp này như một vết màu đỏ) được thực hiện trên ung thư biểu mô lưỡi chuột để đánh giá sự tăng sinh chứng tỏ sự gia tăng đáng kể ở tất cả các nhóm điều trị, cho thấy rằng điều trị bằng macitentan và Ad-EDNRB không làm thay đổi đáng kể sự tăng sinh của ung thư biểu mô. Thanh chia độ biểu thị 0,1 mm.
Chúng tôi đã sử dụng mô hình ung thư chân được thiết lập bằng cách sử dụng các tế bào HSC-3 để kiểm tra tác động của điều trị macitentan đối với sự phát triển của ung thư. Mô hình chân cung cấp hai ưu điểm so với mô hình lưỡi: 1) Mô hình chân HSC-3 đã được sử dụng trong nghiên cứu trước đây của chúng tôi để kiểm tra ảnh hưởng của biểu hiện lại EDNRB đối với sự tăng sinh, vì vậy kết quả của chúng tôi có thể so sánh trực tiếp với kết quả của nghiên cứu trước đó ; 2) thể tích bàn chân có thể được đo trong suốt thí nghiệm để theo dõi sự phát triển của ung thư, trong khi các phép đo lặp lại không thể thực hiện được với mô hình ung thư lưỡi nếu không gây mê cho chuột. Ba liều thử nghiệm (5 mg / kg, 15 mg / kg và 45 mg / kg) được xác định dựa trên các nghiên cứu trước đây trên các mô hình ung thư chuột 4 , 5 , 6. Không có giảm cân đáng kể, mất nước hoặc hôn mê trong xe hoặc các nhóm điều trị. Điều trị bằng Macitentan không ngăn chặn được sự phát triển của ung thư. Nhóm macitentan 5 mg / kg và 15 mg / kg cho thấy không có sự khác biệt đáng kể về sự phát triển ung thư với nhóm xe trong suốt quá trình thử nghiệm. Mặc dù có tác dụng ức chế tạm thời đối với sự phát triển của ung thư ở nhóm macitentan 45 mg / kg giữa các ngày sau khi tiêm (PID) 11 và 18, tác dụng này không được duy trì vào cuối thử nghiệm trên PID 22. Bởi PID 22, có không có sự khác biệt đáng kể về sự thay đổi khối lượng chân (tức là sự phát triển ung thư) giữa nhóm phương tiện và ba nhóm macitentan (Hình 4 C).
Tiếp theo, chúng tôi xác định liệu sự kết hợp giữa macitentan 45 mg / kg và EDNRB tái biểu hiện có thể ức chế sự phát triển của ung thư hay không. Sử dụng cùng một mô hình chân, chúng tôi đã thử nghiệm macitentan 45 mg / kg một mình, EDNRBliệu pháp gen đơn thuần, và sự kết hợp của hai phương pháp điều trị so với phương tiện đối chứng. Theo PID 28, thể tích chân trung bình như sau: Ad-EDNRB riêng 0,28 ml, Ad-EDNRB / macitentan 0,39 ml, macitentan 0,37 ml, xe đối chứng 0,37 ml. Không có sự khác biệt đáng kể giữa bốn nhóm điều trị. Các phương pháp điều trị cũng được thử nghiệm trong mô hình SCC lưỡi chuột được thiết lập với Hela-O3. Chúng tôi đã cấy tế bào Hela-O3 vào lưỡi bên phải. Chúng tôi đã theo dõi những con chuột ở tất cả các nhóm để giảm cân, mất nước và hôn mê. Trên PID 21, chúng tôi thu hoạch mô lưỡi và đo thể tích của ung thư biểu mô. Thể tích khối u trung bình cho bốn nhóm là: 58 ± 8,68 (SD) mm 3 (Ad-GFP / xe, n = 8), 49,29 ± 9,39 mm 3 (Ad-GFP / macitentan, n = 8), 61,5 ± 9,49 mm 3(Ad-EDNRB / xe, n = 8), 73,75 ± 12,75 mm 3 (Ad-EDNRB / macitentan, n = 8), không có sự khác biệt đáng kể giữa các nhóm (Hình 4 D). Do đó, điều trị bằng macitentan và EDNRB tái biểu hiện không có tác dụng lên sự phát triển của ung thư trong mô hình ung thư lưỡi chuột.
Chúng tôi thực hiện phương pháp nhuộm màu Ki67 để xác định xem liệu sự tái biểu hiện macitentan và EDNRB có tác dụng chống tăng sinh ở cấp độ tế bào trong mô hình chuột ung thư lưỡi hay không. Chúng tôi nhuộm các phần đại diện của bệnh ung thư lưỡi trong mỗi nhóm điều trị. Nhuộm Ki67 cho kết quả dương tính ở cả 4 nhóm điều trị, cho thấy sự tái biểu hiện macitentan và EDNRB không ức chế đáng kể sự tăng sinh ung thư (Hình 4 E). Các slide được phân tích bằng Hình ảnh J và các giá trị trung bình từ việc định lượng như sau: GFP / Xe 184,9, GFP / Macitentan 207,2, EDNRB / Xe 194,1, EDNRB / Macitentan 177,9, không có sự khác biệt đáng kể giữa các kết quả được định lượng.
Macitentan có tác dụng chống ung thư trong mô hình ung thư chân HSC-3
Chúng tôi đã xác định khả năng chống ung thư của macitentan. Công việc trước đây của chúng tôi ở những bệnh nhân và các mô hình tiền lâm sàng thành lập các đường endothelin như một người hòa giải đau ung thư miệng, cụ thể là thông qua tiết ở mức độ cao ET-1 bởi các tế bào ung thư 1 , 7 . Cấy HSC-3 vào chân sau để tạo ra cảm ứng nhiệt và cơ học đáng kể (Hình 5 ), được biểu thị bằng sự giảm ngưỡng rút nhiệt và cơ học ở nhóm xe đối chứng sau khi cấy ghép ung thư. Điều trị Macitentan ở cả ba liều (5 mg / kg, 15 mg / kg và 45 mg / kg) tạo ra tác dụng chống ung thư đối với các kích thích cơ học và nhiệt (Hình 5). Tác dụng chống ung thư của macitentan độc lập với tác dụng chống khối u của nó, vì ba liều không tạo ra tác dụng chống khối u mặc dù cho thấy tác dụng chống ung thư.
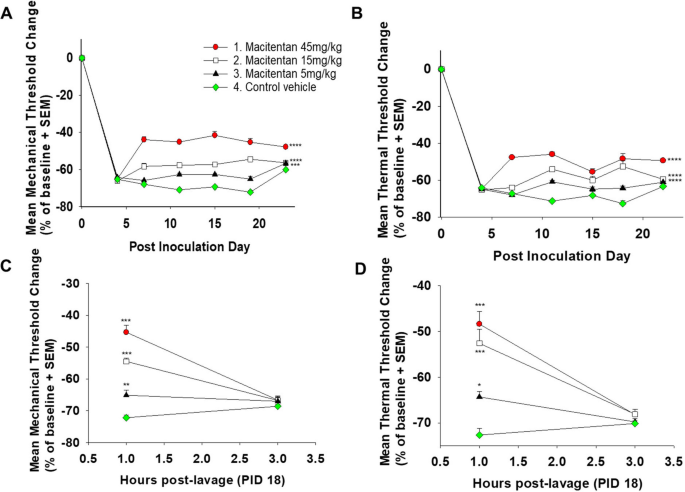
Macitentan có tác dụng chống ung thư trên mô hình chuột HSC-3 có chân. ( A ) và ( B ) Cấy HSC-3 vào chân sau để tạo khối u ở chân dẫn đến khả năng thụ thai đáng kể được thể hiện bằng sự giảm cả ngưỡng nhiệt và cơ học. Điều trị bằng Macitentan ở cả ba liều (5, 15 và 45 mg / kg) tạo ra khả năng chống ung thư đối với cả kích thích nhiệt và cơ học (n = 8 con chuột cái mỗi lần điều trị, *** p <.001, **** p <.0001 , RM ANOVA hai chiều, thử nghiệm Holm Sidak, xem Bảng 2 để biết tóm tắt thống kê). ( C ) và ( D) Thời gian tác dụng chống ung thư của macitentan (sử dụng bằng đường uống) ít hơn ba giờ. Macitentan ở cả ba liều đều tạo ra tác dụng chống ung thư bằng nhiệt và cơ học sau một giờ, nhưng không phải ba giờ, sau khi dùng (n = 8 con chuột cái cho mỗi lần điều trị, * p <0,05, ** p <0,01, *** p <. 001, ANOVA một chiều, thử nghiệm Holm Sidak).
Để xác định thời gian của tác dụng chống ung thư do macitentan tạo ra, chúng tôi đã thực hiện một thử nghiệm theo khóa học thời gian, trong đó chúng tôi đo lặp lại các ngưỡng ngừng cơ học và nhiệt sau khi điều trị macitentan. Thử nghiệm khóa học thời gian được thực hiện trên PID 18 vào một và ba giờ sau khi quản lý macitentan. Chúng tôi xác định rằng mặc dù macitentan tạo ra tác dụng chống ung thư ở cả ba liều dùng (5, 15 và 45 mg / kg) vào một giờ sau khi dùng, tác dụng chống ung thư này không duy trì sau ba giờ (Hình 5 ).
Điều trị kết hợp giữa liệu pháp gen macitentan và EDNRB tạo ra khả năng chống ung thư trên mô hình chuột ung thư có chân Hela-O3
Tiếp theo, chúng tôi xác định liệu sự kết hợp giữa liệu pháp gen macitentan và EDNRB có tạo ra tác dụng chống ung thư đáng kể hơn so với việc điều trị đơn lẻ hay không. Trong bộ thí nghiệm này, chúng tôi đã sử dụng mô hình ung thư ở chân với các tế bào HSC-3 được cấy vào chân sau. Chúng tôi đã xác định các ngưỡng rút nhiệt và cơ học tại thời điểm ban đầu trước khi cấy ghép ung thư; trên PID 18, chúng tôi đo quá mẫn cảm nhiệt và cơ học ở mỗi nhóm điều trị. Mức giảm ngưỡng trung bình (tức là mức độ nhận biết) là cao nhất ở nhóm xe đối chứng. Mô hình chuột Hela-O3 không tạo ra nhiều cảm giác như mô hình chân HSC-3 (Hình 6; nhóm phương tiện kiểm soát có mức giảm> 60% so với ban đầu đối với cả ngưỡng cơ và nhiệt). Trong ba nhóm điều trị, chỉ có nhóm điều trị kết hợp macitentan và EDNRB có ngưỡng nhiệt và cơ học cao hơn đáng kể so với nhóm xe đối chứng. Sự thay đổi ngưỡng trung bình đối với nhóm liệu pháp gen đơn trị liệu macitentan và EDNRB thấp hơn so với nhóm chứng, nhưng không đạt được ý nghĩa thống kê (Hình 6 ).
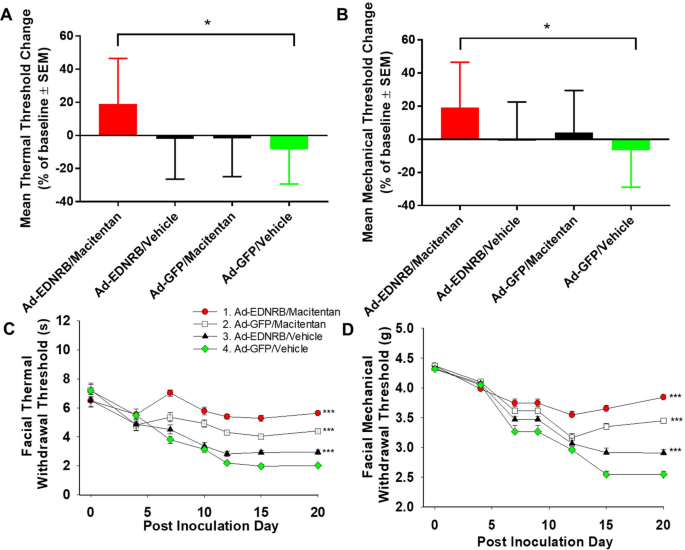
Điều trị kết hợp giữa liệu pháp gien macitentan và EDNRB tạo ra tác dụng chống thụ tinh đáng kể đối với các kích thích cơ học và nhiệt trong mô hình ung thư Hela-O3 ở chân và mô hình ung thư Hela-O3 ở lưỡi. ( A ) Đồ thị thay đổi ngưỡng nhiệt và ( B ) cơ học trên PID 18 so với ban đầu (với sự thay đổi tiêu cực cho thấy tăng khả năng thụ thai) chứng minh rằng điều trị kết hợp với liệu pháp gen macitentan và EDNRB dẫn đến khả năng chống nhận thức đáng kể đối với kích thích nhiệt và cơ học so với đối chứng trong mô hình chân Hela-O3 (n = 8 con chuột cái cho mỗi nghiệm thức, * p <0,05, ANOVA một chiều, thử nghiệm Holm Sidak). ( C ) Đồ thị nhiệt và ( D) thay đổi ngưỡng cơ học so với ban đầu (ngày 0). Trong khi cả ba phương pháp điều trị đều tạo ra khả năng chống ung thư so với phương tiện đối chứng (Ad-GFP / phương tiện), phương pháp điều trị kết hợp giữa liệu pháp gen macitentan và EDNRB tạo ra mức chống ung thư cao nhất đối với cả kích thích nhiệt và cơ học (n = 8 con chuột cái trên mỗi phương pháp điều trị, ** * p <.001 RM ANOVA hai chiều, thử nghiệm Holm Sidak, xem Bảng 2 để biết tóm tắt thống kê).
Điều trị kết hợp giữa liệu pháp gen macitentan và EDNRB tạo ra khả năng chống ung thư trên mô hình chuột ung thư lưỡi Hela-O3
Chúng tôi đã đánh giá độ nhạy cảm cơ học và nhiệt của khuôn mặt 8 ở những con chuột bị ung thư lưỡi được tạo ra từ việc cấy vi khuẩn Hela-O3. Điều trị kết hợp với liệu pháp gen macitentan và EDNRB tạo ra hiệu quả chống ung thư cao nhất trong tất cả các phương pháp điều trị, mặc dù liệu pháp gen macitentan hoặc EDNRB đơn lẻ cũng tạo ra tác dụng chống cảm ứng đối với các kích thích cơ học và nhiệt (Hình 6 ; Bảng 2 ).
Macitentan ức chế kích hoạt tế bào thần kinh sinh ba trong ống nghiệm
Chúng tôi đã sử dụng hình ảnh canxi thời gian thực để xác định liệu macitentan có tạo ra chất chống ung thư thông qua việc ức chế kích hoạt tế bào thần kinh phụ thuộc canxi hay không. Ban đầu, chúng tôi định lượng những thay đổi về nồng độ canxi trong tế bào thần kinh để đáp ứng với ET-1. Chúng tôi đã điều trị các tế bào thần kinh bằng 100 nM ET-1. Để chọn các tế bào thần kinh còn sống trong các trường đã phân tích của chúng tôi, chúng tôi đã xử lý các tế bào thần kinh với KCl vì các tế bào thần kinh sống phản ứng với KCl với một dòng canxi lớn. Trong số những người có phản ứng KCl dương tính, chúng tôi xác định sự thay đổi trong tỷ lệ 340/380 nm trong quá trình xử lý ET-1, sử dụng sự thay đổi tỷ lệ 0,2 làm ngưỡng cho phản ứng tích cực 9 . Chúng tôi nhận thấy rằng 18 trong số 70 tế bào thần kinh được phân tích (26%) có phản ứng tích cực với canxi đối với ET-1 (Hình 7). Tỷ lệ tế bào thần kinh sinh ba của chuột nhạy ET-1 này có thể so sánh với kết quả ở tế bào thần kinh sinh ba của chuột, trong đó 29% tế bào thần kinh đáp ứng với ET-1 10 . Sau đó, chúng tôi xử lý trước các tế bào thần kinh với 20 µM macitentan trước khi ứng dụng ET-1. Chúng tôi phát hiện ra rằng tiền xử lý macitentan ức chế đáng kể phản ứng canxi (tức là kích hoạt tế bào thần kinh) với ET-1, với 4/78 (5%) tế bào thần kinh được phân tích phản ứng với ET-1. Tác dụng ức chế này có ý nghĩa thống kê ( p = 0,001).
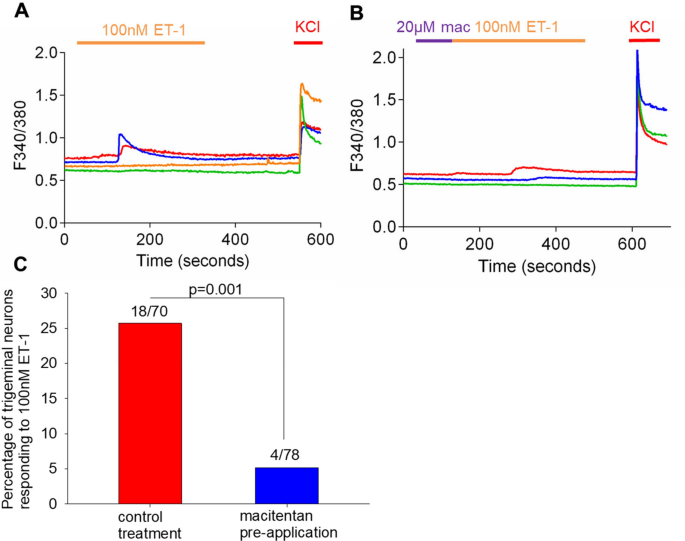
Macitentan ức chế đáng kể sự hoạt hóa tế bào thần kinh sinh ba thành endothelin-1. ( A ) Chúng tôi thực hiện hình ảnh tỷ lệ canxi và xác định rằng 18/70 (26%) tế bào thần kinh trong quần thể tế bào thần kinh sinh ba chuột phân ly được kích hoạt bởi ET-1 (với liều 100 nM). Tỷ lệ phần trăm này tương tự như tỷ lệ phần trăm được báo cáo trước đây trong tế bào thần kinh sinh ba của chuột. ( B ) và ( C ) Sau đó, chúng tôi xử lý trước các tế bào thần kinh sinh ba phân ly bằng 20 µM macitentan và cho thấy rằng việc xử lý trước làm giảm đáng kể số lượng tế bào thần kinh sinh ba được kích hoạt bởi ET-1 ( p = 0,001).
Thảo luận
Trục endothelin, sự xâm lấn và di căn của ung thư
Nghiên cứu này xác định vai trò của trục endothelin đối với sự di căn, tăng sinh và đau của ung thư miệng. Các protein trục endothelin đã được phát hiện trong các khối u ác tính khác nhau, bao gồm ung thư buồng trứng, vú, u ác tính, đại trực tràng, bàng quang và SCC 11 ở miệng . ET-1 làm trung gian cho sự di căn thông qua việc điều hòa nội tiết của các tương tác khối u-mô đệm 12 . ET-1 do tế bào ung thư tiết ra gây ra quá trình hóa học đại thực bào, tăng sinh cơ trơn mạch máu và hình thành mạch, dẫn đến sự di chuyển và di căn của tế bào ung thư 12 , 13 . Trục endothelin góp phần vào sự di căn trong các bệnh ung thư khác thông qua sự kích hoạt ET-1 của ET A R 12. Nghiên cứu trước đây của chúng tôi cho thấy rằng các tế bào SCC ở miệng tiết ra mức ET-1 cao hơn so với các bệnh ung thư khác và mức ET-1 trong nước bọt của bệnh nhân SCC ở miệng cao hơn đối tượng bình thường 7 . Trong SCC đường uống, ET-1 kích hoạt thụ thể yếu tố tăng trưởng biểu bì (EGFR) để tạo ra nhu động của tế bào, yếu tố quan trọng đối với sự di căn 14 . Mặt khác, các chất đối kháng ET A R, ức chế sự hoạt hóa ET-1 của thụ thể này, làm giảm sự phát triển và xâm nhập của các tế bào SCC ở miệng 15 . Thuốc đối kháng con đường endothelin đã được sử dụng trong các thử nghiệm lâm sàng giai đoạn II và III của ung thư tuyến tiền liệt di căn mà không có hiệu quả đáng kể. Tuy nhiên, những thử nghiệm này sử dụng các chất đối kháng đặc hiệu ET A R 16 mà không đề cập đến sự đóng góp của ETB R. Vai trò của ET B R trong việc di căn qua các phân nhóm ung thư khác nhau chưa được hiểu rõ, và việc thiếu lợi ích điều trị bằng thuốc đối kháng ET A R trong các thử nghiệm lâm sàng cho thấy cần phải chuyển trọng tâm sang ET B R. Chúng tôi đã chỉ ra rằng im lặng biểu sinh của EDNRB , gen ET B R, tương quan với di căn cổ ở bệnh nhân SCC đường miệng 1 . Phát hiện của chúng tôi rằng sự im lặng của gen ET B R làm tăng khả năng di căn SCC ở miệng cho thấy rằng hai thụ thể ET có chức năng phân đôi và cần được nhắm mục tiêu khác nhau. Chiến lược điều trị của chúng tôi trong nghiên cứu này, khai thác các chức năng khác biệt của hai thụ thể, thông qua ET đồng thờiỨc chế A R và tái biểu hiện ET B R, ức chế hiệu quả sự di căn SCC qua đường miệng in vitro và trong mô hình tiền lâm sàng. Trong khi điều trị kết hợp giữa liệu pháp gen macitentan và EDNRB không tác động đến sự tăng sinh ung thư, kết quả âm tính này không làm giảm trục endothelin như một mục tiêu quan trọng cho các nghiên cứu trong tương lai về điều trị ung thư miệng, bởi vì di căn, không phải tăng sinh, là yếu tố dự báo quan trọng nhất của sống sót ở những bệnh nhân SCC miệng 2 , 17 .
Trục endothelin và đau do ung thư
ET-1 có tác dụng phân đôi đối với cơn đau. Sự kích hoạt ET-1 của các thụ thể của nó có thể tạo ra cả cơn đau và giảm đau; phản ứng phụ thuộc vào thụ thể nào và tế bào nào được kích hoạt 18 , 19 . EDNRB bị hypermethyl hóa đáng kể trong mô ung thư của bệnh nhân SCC miệng so với mô bình thường bên cạnh của họ; sự biểu hiện quá mức và kích hoạt ET B R (bởi ET-1 trong vi môi trường ung thư) làm giảm cơn đau do ung thư thông qua việc giải phóng β-endorphin 1 . Những phát hiện của chúng tôi trong thập kỷ qua đã đưa chúng tôi đến cách tiếp cận của chúng tôi trong nghiên cứu này để xác định rõ hơn cách trục endothelin góp phần gây đau SCC miệng. Ức chế ET A R đồng thời với macitentan và EDNRBtái biểu hiện tạo ra một hiệu ứng chống ung thư đáng kể trong hai mô hình ung thư chuột riêng biệt. Ở cấp độ tế bào thần kinh, macitentan làm giảm dòng canxi trong tế bào thần kinh để đáp ứng với ET-1. Các phát hiện tiền lâm sàng của chúng tôi tạo tiền đề cho một thử nghiệm lâm sàng trong tương lai để đánh giá khả năng giảm đau của macitentan ở bệnh nhân ung thư. Đau do ung thư vẫn được điều trị kém, với opioid là thuốc giảm đau hiệu quả duy nhất, khiến bệnh nhân ung thư có nguy cơ phụ thuộc vào opioid. Nhu cầu cấp bách về các loại thuốc giảm đau thay thế, đặc biệt là với đại dịch opioid hiện nay và tác động tàn phá của nó đối với bệnh nhân và hệ thống chăm sóc sức khỏe. Điều trị giảm đau do ung thư không hiệu quả không chỉ làm giảm chất lượng cuộc sống mà còn làm giảm khả năng sống sót ở bệnh nhân ung thư 20. Bệnh nhân ung thư miệng nói riêng có nguy cơ cao trong việc kiểm soát cơn đau kém và phụ thuộc vào opioid 21 , 22 .
Liên kết số của ET A R và ET B R và liên kết ràng buộc của ET A R và ET B R đối với ET-1
ET A R và ET B R liên kết với tư cách là dị nhân thông qua liên kết với phối tử ET-1 hóa trị hai. Một chất đối kháng ET A R phá vỡ heterodimer và giải phóng ET B R để liên kết ET-1 với ái lực lớn hơn chín lần so với ET A R hoặc AB dimer 23 . Do đó, một chất đối kháng ET A R thích hợp có thể giải phóng ET BR để liên kết ET-1 trong môi trường vi sinh ung thư, dẫn đến tiết opioid nội sinh — một cách tiếp cận tiềm năng để kiểm soát cơn đau do ung thư tại gốc. Các chất đối kháng thụ thể endothelin được phát triển trước đây bao gồm atrasentan và bosentan. Macitentan, không giống như bosentan và ambrisentan, là một chất đối kháng không thể vượt qua với tỷ lệ phân ly thụ thể thấp trên một loạt các nồng độ ET-1 24 . Ngoài ái lực cao với ET A R, macitentan có ái lực thấp với ET B R, dược lý học rất quan trọng đối với việc kích hoạt ET B R bởi ET-1. Macitentan có thể được dùng bằng đường uống và đã được sử dụng trong các thử nghiệm lâm sàng để điều trị tăng huyết áp động mạch phổi 25. Ngoài việc thiết lập tác dụng chống ung thư của macitentan đối với SCC đường uống, chúng tôi xác định vai trò mới của macitentan như một loại thuốc giảm đau để điều trị đau do ung thư. Chiến lược điều trị của chúng tôi liên quan đến macitentan với EDNRBliệu pháp gen ức chế di căn và đau SCC qua đường miệng hiệu quả hơn so với macitentan đơn thuần. Mặc dù trực tiếp chuyển chiến lược điều trị này sang các thử nghiệm lâm sàng là một nhiệm vụ phức tạp, nhưng tiềm năng chuyển đổi của nghiên cứu của chúng tôi nằm ở việc chứng minh một phương pháp y học chính xác để điều trị di căn và đau ung thư miệng. Chúng tôi xác định một con đường bị rối loạn điều hòa trong các mô ung thư của bệnh nhân ung thư miệng, thiết kế liệu pháp để điều chỉnh sự rối loạn điều hòa của các gen thành phần trong con đường bằng cách sử dụng một loại thuốc và liệu pháp gen sẵn có, đồng thời điều trị hiệu quả di căn và đau trong một mô hình tiền lâm sàng. Hơn nữa, chúng tôi nhấn mạnh tầm quan trọng của việc tận dụng các vai trò phân đôi của ET A R và ET BCác thụ thể R, phần lớn đã bị bỏ qua trong các nghiên cứu tiền lâm sàng và lâm sàng trên các phân nhóm ung thư khác nhau 16 . Phát hiện của chúng tôi nhấn mạnh trục endothelin như một mục tiêu quan trọng không chỉ đối với di căn ung thư mà còn đối với đau do ung thư, một vấn đề vẫn được điều trị kém mặc dù có những tiến bộ trong điều trị ung thư giúp cải thiện khả năng sống sót.
Phương pháp
Nuôi cấy tế bào
Tế bào ung thư: Các dòng tế bào ung thư biểu mô vảy ở miệng ở người, HSC-3 và Hela-O3, được nuôi cấy trong Dulbecco’s Modification of Eagle’s Medium (DMEM) với 4,5 g / L glucose, L -glutamine và natri pyruvate, được bổ sung với 10% bào thai. huyết thanh bò (FBS), và được nuôi cấy ở 37 ° C trong 5% CO 2 . HSC-3 được mua từ ATCC và được sử dụng chưa đầy 6 tháng sau khi hồi sức. Hela-O3 được lấy từ Tiến sĩ Roberto Weigert tại Viện Ung thư Quốc gia và được kiểm tra Mycoplasma bằng PCR (ATCC) trước khi sử dụng.
Tế bào thần kinh: Các hạch sinh ba của chuột được thu hoạch và nuôi cấy như đã mô tả trước đây 26 . Các hạch sinh ba được phân lập, chuyển vào Dung dịch muối cân bằng Hank (HBSS) và được tiêu hóa bằng enzym bằng cách ủ với papain (Worthington), collagenase loại II (Worthington), và loại II (MB). Các tế bào thần kinh phân ly được mạ trên các tấm bìa thủy tinh phủ poly-d-lysine và laminin và duy trì ở 37 ° C với 5% CO 2 /95% không khí trong môi trường F12 (Life Technologies) với 5% FBS.
Truyền luciferase
Dòng tế bào Hela-O3 được truyền plasmid mã hóa gen luciferase để cho phép tạo hình khối u động vật sống. DNA plasmid, mã hóa cho luciferase (gWIZ luciferase) dưới sự kiểm soát của chất khởi động / tăng cường cytomegalovirus được lấy từ Genlantics (San Diego, CA). Chúng tôi đã sử dụng kỹ thuật chuyển nạp đã sửa đổi với vectơ lai không virus, chuỗi peptit HIV-1 Tat được sửa đổi với các gốc histidine và cysteine kết hợp với một lipid cation 27 .
Sự tải nạp của EDNRB
CDNA của người EDNRB có chứa thẻ GFP ở đầu C (OriGene) được nhân dòng thành plasmid con thoi. Quá trình tách dòng và tinh chế hạt virus đã được hoàn thành thông qua Viraquest. Tế bào SCC trong miệng (HSC-3 hoặc Hela-O3) được chuyển nạp với adenovirus tái tổ hợp (Ad-EDNRB hoặc Ad-GFP) với số lần lây nhiễm ngày càng tăng (MOI) để xác định hiệu quả tải nạp. Quá trình chuyển nạp được thực hiện trong DMEM với 2% huyết thanh bò thai (FBS) và các chất bổ sung đã nói ở trên 1 .
Thử nghiệm di cư và xâm nhập in vitro
Xét nghiệm xâm lấn BD Biosciences được sử dụng theo khuyến nghị của nhà sản xuất. Thử nghiệm bao gồm một miếng chèn buồng xâm lấn phía trên phù hợp với đĩa nuôi cấy tế bào 24 giếng. Buồng xâm lấn phía trên được phủ bằng ma trận BD Matrigel để cho phép đánh giá khả năng xâm lấn. Đối với mỗi lần điều trị, các khoang xâm lấn không phủ được sử dụng làm đối chứng. Số lượng bằng nhau của tế bào Hela-O3 (2 × 10 5 ) trong DMEM được bổ sung 0,4% FBS đã được thêm vào mỗi buồng trên. Các tế bào đã được chuyển nạp bằng GFP hoặc EDNRB 1 .Macitentan đã bị giải thể trong DMEM. Các giếng đáy trong đĩa nuôi cấy 24 giếng được lấp đầy bằng DMEM được bổ sung 5% FBS, đóng vai trò như một chất hóa trị. Các khoang xâm lấn phía trên được đặt vào đĩa nuôi cấy tế bào và ủ ở 37 ° C trong 16 giờ. Vào cuối thời kỳ ủ, các tế bào từ bề mặt trên của bộ lọc được lau sạch bằng tăm bông. Bề mặt dưới của bộ lọc được nhuộm bằng DiffQuik (Dade Behring, Thụy Sĩ). Số lượng tế bào di chuyển đến đáy buồng được đếm trong kính hiển vi ánh sáng trên mười trường được chọn ngẫu nhiên ở độ phóng đại 10 lần. Việc đếm được thực hiện bởi một điều tra viên bị mù đối với các nhóm điều trị. Số lượng ô trung bình được tính cho mỗi trường. Ba bộ thí nghiệm đã được thực hiện, mỗi bộ làm bốn.
Thử nghiệm RTCA
Máy phân tích tế bào thời gian thực xCELLigence (ACEA) được sử dụng để định lượng sự thay đổi trong trở kháng và chỉ số tăng sinh tế bào. 10 3 Tế bào Hela-O3, được chuyển nạp bằng Ad-GFP hoặc Ad-EDNRB, được nuôi cấy qua đêm trong DMEM được bổ sung 5% FBS để thu được đường cơ sở. Sau khi có được đường cơ sở, macitentan hoặc điều khiển phương tiện được thêm vào mỗi giếng. Các tế bào được theo dõi liên tục sau mỗi 15 giây trong 72 giờ. Sự thay đổi về trở kháng so với mức cơ bản đã được phần mềm Phân tích tế bào thời gian thực tính toán và chuyển đổi thành chỉ số tế bào.
Thử nghiệm MTS
Xét nghiệm MTS được sử dụng để định lượng hiệu quả của điều trị macitentan và sự tái biểu hiện EDNRB đối với sự tăng sinh Hela-O3. 2 × 10 4 tế bào Hela-O3 được chuyển nạp bằng GFP hoặc EDNRB (ở 12 MOI) được gieo vào mỗi giếng trong đĩa 96 giếng. Tế bào được gieo hạt bằng macitentan 4,5 µM hoặc phương tiện (DMSO) trong DMEM bổ sung 5% FBS. Mỗi nhóm xử lý được gieo vào 16 giếng. Tế bào được ủ ở 37ºC trong 24 giờ. 20 μl MTS (Promega BioSciences, San Luis Obispo, CA) được thêm vào mỗi giếng và ủ ở 37 ° C trong 2 giờ. Độ hấp thụ của mỗi giếng được đọc ở bước sóng 450 nm. Giá trị độ hấp thụ được tính trung bình cho mỗi nhóm trong số bốn nhóm xử lý.
Hình ảnh canxi
Các tế bào thần kinh phân ly được cấy vào các tấm phủ thủy tinh, được nạp 1 µM thuốc nhuộm nhạy cảm với canxi có thể thẩm thấu qua tế bào, Fura 2AM (Đầu dò phân tử) trong 30 phút và rửa sạch bằng HBSS trước khi sử dụng. Các tấm bìa có chứa các tế bào được đặt trong một buồng có truyền HBSS liên tục ở nhiệt độ phòng. Hiện tượng huỳnh quang được phát hiện bởi kính hiển vi Nikon Eclipse TI ở bước sóng kích thích 340 và 380 và được phân tích bằng Phần mềm Phần tử TI (Nikon). Các tế bào HSC-3 được tính là đáp ứng với truyền 10 µM [D-Ala 2 , N-MePhe 4 , Gly-ol] -enkephalin (DAMGO) và các tế bào thần kinh được tính là đáp ứng với truyền dịch nổi ung thư nếu tỷ lệ 340/380 là ≥ 0,2 từ đường cơ sở 28 .
Mô hình ung thư chuột
Tất cả các thí nghiệm trên chuột đã được Ủy ban chăm sóc và sử dụng động vật có tổ chức (IACUC) tại Đại học New York chấp thuận và được thực hiện theo quy định của IACUC. Mô hình giảm đau do ung thư bàn chân chuột được tạo ra bằng cách cấy HSC-3, một dòng tế bào ung thư biểu mô vảy ở miệng, vào chân sau bên phải của BALB / c thể thao như đã mô tả 7 trước đó . 24 giờ trước khi cấy, tế bào ung thư được chuyển nạp bằng Ad-EDNRB hoặc Ad-GFP. Những con chuột được chia thành hai nhóm và được cấy vào chân sau bên phải với các loại tế bào tương ứng: (1) Ad-EDNRB và (2) Ad-GFP. Các phép đo thể tích chân được thực hiện bằng máy đo độ màng phổi (IITC Life Sciences) như mô tả 1và được sử dụng như một chỉ số về sự phát triển của ung thư. Một mô hình ung thư lưỡi chuột được tạo ra bằng cách cấy vi khuẩn Hela-O3 vào lưỡi bên phải của chuột BALB / c khỏe mạnh. Dòng tế bào Hela-O3 (trước đây là OSCC3) di căn đến các nút cổ tử cung khi được tiêm vào khoang miệng của những con chuột khỏe mạnh 3 .
Điều trị Macitentan
Macitentan, một chất đối kháng thụ thể endothelin (ET) loại A và loại B kép, được cung cấp bởi Actelion, được hòa tan trong dung dịch nước chứa 0,5% methylcellulose và 0,05% Tween 80. Dung dịch được sử dụng theo trọng lượng cơ thể ở mức 15 mg / kg, 30 mg / kg hoặc 45 mg / kg đối với các thí nghiệm định lượng và ở mức 45 mg / kg đối với tất cả các thí nghiệm khác. Đối với các thí nghiệm in vitro, macitentan được hòa tan trực tiếp vào môi trường tế bào.
Phép đo allodynia cơ học
Chúng tôi xác định chứng dị ứng cơ học bằng cách sử dụng hai mô hình đau ung thư riêng biệt, một mô hình ung thư lưỡi và một mô hình ung thư bàn chân. Chúng tôi định lượng tình trạng dị ứng trên khuôn mặt bằng cách sử dụng một loạt các sợi von Frey được phân loại 29 . Thử nghiệm được thực hiện vào ngày 0 trước khi cấy và hai lần một tuần sau khi cấy. Xét nghiệm von Frey được phân loại là một xét nghiệm hợp lệ để định lượng chứng dị ứng trên mô hình chuột mắc bệnh ung thư xương hàm 30. Chúng tôi đã định lượng ngưỡng rút chân bằng cách sử dụng máy đo gây mê von Frey điện tử như chúng tôi đã mô tả 1 . Thử nghiệm được thực hiện vào ngày 0 trước khi cấy và sau đó hai lần một tuần sau khi cấy.
Đo nhiệt độ hyperalgesia
Chúng tôi xác định chứng tăng nhiệt do nhiệt bằng cách sử dụng mô hình ung thư mặt và mô hình ung thư chân. Sự tăng nhiệt độ tăng nhiệt được đánh giá như đã mô tả trước đây 31 bằng cách sử dụng bóng đèn chiếu hội tụ để cung cấp kích thích nhiệt đến phần râu bên phải hoặc bàn phím chân phải của mỗi con chuột với thời gian cắt 20 s. Sự rút mặt hoặc rút chân về nhiệt được tính là giá trị trung bình của sáu phép đo. Thử nghiệm được thực hiện vào ngày 0 trước khi cấy và sau đó hai lần một tuần sau khi cấy, cùng ngày với thử nghiệm dị ứng cơ học.
Hình ảnh phát quang sinh học
Hình ảnh phát quang sinh học thu được bằng máy phân tích sinh học Xenogen IVIS Lumina II. Hai mươi phút trước khi chụp ảnh, những con chuột được tiêm 200 μl d-luciferin (Khoa học Đời sống Caliper). Sau đó, họ được gây mê bằng khí isoflurane và được gây mê bằng isoflurane 2%. Sau đó, chuột được đặt ở tư thế nằm sấp trong hệ thống hình ảnh IVIS và quét toàn bộ cơ thể. Phát xạ ánh sáng được thu thập và cường độ được biểu thị bằng số photon / cm 2 trong vùng quan tâm (ROI). Biểu hiện Luciferase được định lượng bằng Phần mềm Hình ảnh Sống phiên bản 4.0. Đối với chuột trong tất cả các nhóm thử nghiệm, ROI được chọn làm vùng mặt, để định lượng mức độ phát triển của ung thư ở lưỡi.
Thu hoạch mô
Các mô chuột được thu hoạch vào cuối thí nghiệm. Đối với mô hình ung thư lưỡi chuột, lưỡi và các hạch bạch huyết ở cổ được thu hoạch, cố định trong 4% paraformaldehyde và nhúng vào parafin. Khối lượng ung thư của lưỡi được tính toán sau khi thu hoạch mô bằng cách đo chiều dài, chiều rộng và chiều sâu của khối ung thư. Ba đoạn 5 µm được cắt để nhuộm hematoxylin và eosin. Các phần hạch bạch huyết đã được phân tích để tìm bằng chứng về sự di căn của ung thư bởi một nhà nghiên cứu bệnh học răng miệng được chứng nhận bởi hội đồng quản trị (Tiến sĩ King Chong Chan), người bị mù trong các nhóm điều trị. Di căn nút cổ tử cung được đánh dấu là không có nếu cả ba phần không chứng minh được sự hiện diện của tế bào ung thư. Di căn cổ tử cung được đánh dấu là hiện tại nếu ít nhất một trong ba phần chứng tỏ có tế bào ung thư.
Phân tích mảng mô bệnh nhân
Nghiên cứu đã được phê duyệt bởi Hội đồng Đánh giá Thể chế tại Đại học New York và được thực hiện theo các hướng dẫn và quy định liên quan. Tất cả bệnh nhân đều nhận được sự đồng ý đã được thông báo, với những bệnh nhân đủ điều kiện bao gồm cả những người từ 18 tuổi trở lên bị ung thư biểu mô tế bào vảy trong khoang miệng đã được chứng minh bằng sinh thiết và không có tiền sử điều trị ung thư đầu và cổ. Chụp mô đông lạnh của ung thư và mô bình thường bên cạnh được lấy tại thời điểm phẫu thuật cắt bỏ 22 bệnh nhân ung thư miệng. Các phần phụ của bệnh bao gồm lưỡi, nướu răng hàm trên và hàm dưới, và sàn miệng. RNA và DNA được tách chiết theo giao thức Qiagen AllPrep (Qiagen). RNA và DNA đã được xử lý để chuẩn bị cho Mảng Methyl hóa Illumina 450K và Mảng Biểu hiện Gen.ECE1, ECE2, EDN1, EDNRA, EDNRB ) chúng tôi đã tạo ra một ma trận tương quan của biểu hiện gen và sự methyl hóa DNA. Sau đó, chúng tôi phù hợp với một mô hình hồi quy tuyến tính cho mỗi vị trí CpG và mỗi bản sao của một gen nhất định.
Phân tích thống kê
Kết quả được phân tích bằng Sigma Plot phiên bản 13.0 hoặc GraphPad Prism phiên bản 7.01.
Người giới thiệu
- 1.Việt, CT và cộng sự. Sự tái biểu hiện của gen EDNRB đã được methyl hóa trong ung thư biểu mô tế bào vảy ở miệng làm giảm cơn đau do ung thư. Pain 152 (10), 2323–2332 (2011).CAS PubMed PubMed Central Bài báo Google Scholar
- 2.Cooper, JS và cộng sự. Xạ trị đồng thời sau phẫu thuật và hóa trị cho ung thư biểu mô tế bào vảy nguy cơ cao ở đầu và cổ. N. Engl. J. Med. 350 (19), 1937–1944 (2004).PubMed Bài báo Google Scholar
- 3.Amornphimoltham, P. và cộng sự. Rab25 điều chỉnh sự xâm lấn và di căn trong ung thư đầu cổ. Clin. Cancer Res 19 (6), 1375–1388 (2013).CAS PubMed PubMed Central Bài báo Google Scholar
- 4.Kim, SJ và cộng sự. Macitentan, một chất đối kháng thụ thể endothelin kép, kết hợp với temozolomide dẫn đến thoái triển u nguyên bào thần kinh đệm và tồn tại lâu dài ở chuột. Clin. Ung thư Res. 21 (20), 4630–4641 (2015).CAS PubMed PubMed Central Bài báo Google Scholar
- 5.Kim, SJ và cộng sự. Macitentan (ACT-064992), một chất đối kháng thụ thể endothelin nhắm mục tiêu vào mô, nâng cao hiệu quả điều trị của paclitaxel bằng cách điều chỉnh các con đường sống sót trong các mô hình trực tiếp của ung thư buồng trứng di căn ở người. Neoplasia 13 (2), 167–179 (2011).CAS PubMed PubMed Central Bài báo Google Scholar
- 6.Lee, HJ và cộng sự. Điều trị thực nghiệm ung thư vú ở người và ung thư phổi di căn não ở chuột bằng macitentan, một chất đối kháng kép của thụ thể endothelin, kết hợp với paclitaxel. Oncol thần kinh. 18 (4), 486–496 (2016).CAS PubMed PubMed Central Bài báo Google Scholar
- 7.Pickering, V., Jay Gupta, R., Quang, P., Jordan, RC & Schmidt, BL Ảnh hưởng của nồng độ endothelin-1 ngoại vi lên cơn đau do ung thư biểu mô ở chuột. Eur. J. Pain 12 (3), 293–300 (2008).CAS PubMed Bài báo Google Scholar
- số 8.Ono, K. và cộng sự. Sắc tố da điều chỉnh độ nhạy cảm của da thông qua tín hiệu dopaminergic phụ thuộc tyrosinase. Khoa học. Rep. 7 (1), 9181 (2017).QUẢNG CÁO PubMed PubMed Central Bài báo Google Scholar
- 9.Việt, CT và cộng sự. Thuốc khử methyl như thuốc giảm đau mới cho cơn đau do ung thư. Clin. Ung thư Res. 20 (18), 4882–4893 (2014).CAS PubMed PubMed Central Bài báo Google Scholar
- 10.Yamamoto, T. và cộng sự. Đáp ứng qua trung gian thụ thể endothelin trong tế bào thần kinh hạch sinh ba. J. Dent Res. 92 (4), 335–339 (2013).CAS PubMed Bài báo Google Scholar
- 11.Bagnato, A., Loizidou, M., Pflug, BR, Curwen, J. & Growcott, J. Vai trò của trục endothelin và các chất đối kháng của nó trong điều trị ung thư. Br. J. Pharmacol. 163 (2), 220–233 (2011).CAS PubMed PubMed Central Bài báo Google Scholar
- 12.Spinella, F. và cộng sự. Endothelin-1 và endothelin-3 thúc đẩy hành vi xâm lấn thông qua yếu tố 1alpha gây giảm oxy trong tế bào u ác tính ở người. Có thể. Res. 67 (4), 1725–1734 (2007).CAS Bài báo Google Scholar
- 13.Bagnato, A. & Rosano, L. Chuyển tiếp biểu mô-trung mô trong tiến triển ung thư buồng trứng: Một vai trò quan trọng đối với trục endothelin. Tế bào Mô cơ quan 185 (1–3), 85–94 (2007).CAS PubMed Bài báo Google Scholar
- 14.Hinsley, EE, Hunt, S., Hunter, KD, Whawell, SA & Lambert, DW Endothelin-1 kích thích nhu động của tế bào ung thư biểu mô vảy ở đầu và cổ bằng cách thúc đẩy tương tác mô đệm-biểu mô. J. Int. Ung thư 130 (1), 40–47 (2012).CAS Bài báo Google Scholar
- 15.Mai, HQ et al. Nhắm mục tiêu điều trị của endothelin, một thụ thể trong ung thư biểu mô vòm họng ở người. Khoa học ung thư. 97 (12), 1388–1395 (2006).CAS PubMed Bài báo Google Scholar
- 16.Enevoldsen, FC và cộng sự. Thuốc đối kháng thụ thể endothelin: Hiện trạng và viễn cảnh tương lai cho liệu pháp nhắm mục tiêu. J. Clin. Med. 9 (3), 824 (năm 2020).CAS PubMed Central Bài báo Google Scholar
- 17.D’Cruz, AK và cộng sự. Bóc tách cổ tự chọn so với điều trị trong ung thư miệng âm tính với nút. N Engl J Med 373 (6), 521–529 (2015).CAS PubMed Bài báo Google Scholar
- 18.Hans, G., Deseure, K., Robert, D. & De Hert, S. Những thay đổi về tế bào thần kinh trong mô hình người về cơn đau do endothelin-1 gây ra: Một nghiên cứu về hành vi. Tế bào thần kinh. Lett. 418 (2), 117–121 (2007).CAS PubMed Bài báo Google Scholar
- 19.Khodorova, A., Montmayeur, JP & Strichartz, G. Các thụ thể endothelin và cảm giác đau. J. Pain 10 (1), 4–28 (2009).CAS PubMed PubMed Central Bài báo Google Scholar
- 20.Temel, JS và cộng sự. Chăm sóc giảm nhẹ sớm cho bệnh nhân ung thư phổi không phải tế bào nhỏ di căn. N. Engl. J. Med. 363 (8), 733–742 (2010).CAS PubMed Bài báo Google Scholar
- 21.van den Beuken-van Everdingen, MH và cộng sự. Tỷ lệ đau cao ở bệnh nhân ung thư trong một nghiên cứu dựa trên dân số lớn ở Hà Lan. Pain 132 (3), 312–320 (2007).PubMed Bài báo Google Scholar
- 22.Viet, CT & Schmidt, BL Cơ chế sinh học của đau do ung thư miệng và ý nghĩa đối với điều trị lâm sàng. J Dent Res 91 (5), 447–453 (2012).CAS PubMed PubMed Central Bài báo Google Scholar
- 23.Harada, N., Himeno, A., Shigematsu, K., Sumikawa, K. & Niwa, M. Liên kết endothelin-1 với các thụ thể endothelin trong tuyến yên trước của chuột: Có thể hình thành dị nhân thụ thể ETA-ETB. Ô Mol. Neurobiol. 22 (2), 207–226 (2002).CAS PubMed Bài báo Google Scholar
- 24.Gatfield, J., Mueller, GC, Sasse, T., Clozel, M. & Nayler, O. Động học phân ly thụ thể chậm phân biệt macitentan với các chất đối kháng thụ thể endothelin khác trong tế bào cơ trơn động mạch phổi. PLoS ONE 7 (10), e47662 (2012).QUẢNG CÁO CAS PubMed PubMed Central Bài báo Google Scholar
- 25.Channick, RN và cộng sự. Ảnh hưởng của macitentan khi nhập viện: Kết quả từ thử nghiệm SERAPHIN. JACC Suy tim 3 (1), 1–8 (2015).PubMed Bài báo Google Scholar
- 26.Malin, SA, Davis, BM & Molliver, DC Sản xuất các nuôi cấy nơ-ron cảm giác phân ly và xem xét việc sử dụng chúng trong nghiên cứu chức năng và độ dẻo của tế bào thần kinh. Nat. Protoc. 2 (1), 152–160 (2007).CAS PubMed Bài báo Google Scholar
- 27.Yamano, S. và cộng sự. Sự phân phối gen không virus ex vivo của thụ thể mu-opioid để làm giảm cơn đau do ung thư gây ra. Pain 158 (2), 240–251 (2017).CAS PubMed PubMed Central Bài báo Google Scholar
- 28.Samoshkin, A. và cộng sự. Tương tác về cấu trúc và chức năng giữa thụ thể mu-opioid sáu xuyên màng và thụ thể beta2-adrenorenorenoreceptor điều chỉnh tín hiệu opioid. Khoa học. Rep. 5 , 18198 (2015).QUẢNG CÁO CAS PubMed PubMed Central Bài báo Google Scholar
- 29.Vos, BP, Strassman, AM & Maciewicz, RJ Bằng chứng hành vi về chứng đau thần kinh sinh ba sau chấn thương co thắt mãn tính đối với dây thần kinh dưới ổ mắt của chuột. J. Tế bào thần kinh. 14 (5 Pt 1), 2708–2723 (1994).CAS PubMed PubMed Central Bài báo Google Scholar
- 30.Ye, Y., Ung thư biểu mô tế bào vảy ở miệng gây ra sự thay đổi khác biệt về độ nhạy cảm cơ học và nhiệt toàn cầu ở chuột, Hiệp hội Quốc tế về Nghiên cứu Đau (Milan, Ý 2012).
- 31.Hargreaves, K., Dubner, R., Brown, F., Flores, C. & Joris, J. Một phương pháp mới và nhạy để đo cảm giác nhiệt trong tăng trương lực da. Pain 32 (1), 77–88 (1988).CAS PubMed Bài báo Google Scholar
Tải xuống tài liệu tham khảo
Kinh phí
Tổ chức Phẫu thuật Răng miệng và Răng hàm mặt.
Thông tin tác giả
Chi nhánh
- Khoa phẫu thuật răng hàm mặt, Đại học New York, New York, NY, Hoa KỳDongmin Dang, Yi Ye & Bradley E. Aouizerat
- Trung tâm nghiên cứu lâm sàng Bluestone, Đại học New York, New York, NY, Hoa KỳDongmin Dang, Yi Ye, Bradley E. Aouizerat, Yogin K. Patel & Dan T. Viet
- Rory Meyers Cao đẳng Điều dưỡng, Đại học New York, New York, NY, Hoa KỳBradley E. Aouizerat và Gary Yu
- Phòng X quang Răng Hàm Mặt, Khoa Nha khoa Bệnh viện, Trung tâm Y tế Irving Đại học Columbia, New York, NY, Hoa KỳKing Chong Chan
- Khoa Sinh lý, Đại học Nha khoa Kyushu, Kitakyushu, Nhật BảnKentaro Ono
- Khoa Phẫu thuật Răng Hàm Mặt, Trường Nha khoa Đại học Loma Linda, Loma Linda, CA, Hoa KỳColeen Doan & Chi T. Viet
- Khoa Khoa học Cơ bản, Trung tâm Chênh lệch Sức khỏe và Y học Phân tử, Trường Y Đại học Loma Linda, Loma Linda, CA, Hoa KỳJohnny D. Figueroa
Đóng góp
CTV thiết kế tất cả các thí nghiệm in vitro và in vivo. DD, YY, YKP, DTV, KO, CD và CTV thực hiện các thí nghiệm. Kết quả mảng diễn giải BEA và GY, KCC xác định tình trạng di căn cổ ở các nhóm thí nghiệm theo kiểu mù. CTV diễn giải kết quả và thực hiện phân tích dữ liệu. JDF đã tư vấn thiết kế thử nghiệm và sửa đổi bản thảo. CTV đã chuẩn bị bản thảo và số liệu, cùng tất cả các tác giả xem lại bản thảo.
Đồng tác giả
Thư từ Chi T. Việt .