Nhắm mục tiêu miễn dịch qua trung gian axit hạt nhân trong các liệu pháp ức chế điểm kiểm soát miễn dịch ung thư
- Miaoqin Chen ,
- Shiman Hu ,
- Yiling Li ,
- Ting Ting Jiang ,
- Hongchuan Jin &
- Lifeng Feng
Theo NATURE
- trừu tượng
Liệu pháp miễn dịch ung thư đặc biệt là ức chế trạm kiểm soát miễn dịch đã đạt được những thành công chưa từng có trong điều trị ung thư. Tuy nhiên, có nhiều bệnh nhân đã không đạt được lợi ích từ các liệu pháp này, cho thấy sự cần thiết phải kết hợp mới để tăng hiệu quả lâm sàng của các chất ức chế điểm kiểm tra miễn dịch. Trong bài tổng quan này, chúng tôi tóm tắt những khám phá mới nhất về sự kết hợp giữa miễn dịch cảm ứng axit nucleic và chất ức chế điểm kiểm tra miễn dịch trong liệu pháp miễn dịch ung thư. Với vai trò quan trọng của miễn dịch qua trung gian axit hạt nhân trong việc duy trì hoạt hóa chức năng tế bào T, có vẻ như việc khai thác miễn dịch qua trung gian axit hạt nhân mở ra các chiến lược mới để tăng cường tác dụng của các chất ức chế điểm kiểm soát miễn dịch trong việc kiểm soát khối u.
Giới thiệu
Liệu pháp miễn dịch ung thư, khai thác để kích hoạt hệ thống miễn dịch chống lại các khối u ác tính, đã trở thành một chiến lược lớn trong một thời gian dài. Đầu năm 1891, Willam Cooley đã cố gắng điều trị bệnh sarcoma bằng cách tiêm Streptococcus pyogenes và Serratia marcescens vào khoang miệng để kích hoạt khả năng miễn dịch. 1 Hiện tại, chiến lược được sử dụng phổ biến nhất là ức chế các điểm kiểm tra miễn dịch, đặc biệt nhắm mục tiêu vào thụ thể chết tế bào được lập trình-1 (PD-1) và phối tử của nó, phối tử tế bào chết được lập trình-1 (PD-L1) và tế bào lympho T gây độc tế bào- protein liên kết 4 (CTLA4). 2Nivolumab, pembrolizumab và camrelizumab là những chất ngăn chặn PD-1 đã được phê duyệt, trong khi atezolizumab, avelumab và durvalumab là những kháng thể ngăn chặn PD-L1 đã được phê duyệt. Một cách rộng rãi, các tác nhân này đã được áp dụng để điều trị nhiều loại khối u tiên tiến, bao gồm khối u ác tính di căn, ung thư phổi không tế bào nhỏ, ung thư biểu mô dạ dày, ung thư biểu mô tế bào gan, ung thư biểu mô tế bào thận, v.v. 3 , 4 , 5 , 6 , 7
Mặc dù đáp ứng điều trị mạnh mẽ, các tác nhân này chỉ cung cấp các đáp ứng lâm sàng bền vững ở gần 20% bệnh nhân ung thư dưới dạng đơn trị liệu. 8 Và có nhiều cơ chế phức tạp của sự đề kháng nguyên phát hoặc mắc phải đối với phong tỏa điểm kiểm soát miễn dịch. Vì trung tâm của các chất ức chế điểm kiểm tra miễn dịch (ICI) là kích hoạt lại các tế bào T tác động, sự kháng thuốc chủ yếu là do sự xâm nhập không đủ hoặc suy giảm chức năng của các tế bào T trong vi môi trường khối u. 9
Là tuyến phòng thủ đầu tiên, các phản ứng miễn dịch bẩm sinh rất quan trọng trong việc khởi phát và duy trì các phản ứng của tế bào T, bao gồm cả miễn dịch khối u lấy tế bào T làm trung tâm. 10 Một cách ngắn gọn, các tế bào trình diện kháng nguyên (APC) hấp thu và trình bày kháng nguyên khối u thông qua phức hợp tương thích mô chính I (MHC-I), và do đó gây ra sự mở rộng tế bào T CD8 + đặc hiệu của khối u . Ngoài ra, một số APC như cDC1 (một tập hợp con của các tế bào đuôi gai thông thường) cũng có thể tạo ra chemokine bao gồm CXCL9 và CXCL10 để tuyển dụng các tế bào T vào vi môi trường khối u. 11 Tế bào tiêu diệt tự nhiên (tế bào NK), một lớp tế bào miễn dịch bẩm sinh quan trọng khác, có thể tiêu diệt các tế bào khối u mục tiêu, tiết ra các cytokine chống khối u, và cũng góp phần vào sự xâm nhập của cDC1 vào khối u. 12
Các tín hiệu quan trọng để tạo ra các phản ứng miễn dịch bao gồm các độc tố có nguồn gốc từ mầm bệnh như LPS và các vật liệu di truyền ngoài tử cung như axit hạt nhân ngoại sinh hoặc tế bào. Trong khi đó, cái gọi là các thụ thể nhận dạng mẫu (PRR) là các protein tham gia vào việc phát hiện các mẫu phân tử liên quan đến mầm bệnh và truyền tín hiệu loại trừ các tác nhân lây nhiễm. Quan trọng hơn, sinh vật kích hoạt hệ thống miễn dịch bẩm sinh dựa vào tín hiệu qua trung gian PRRs. 13Cảm biến axit nucleic, có thể phát hiện DNA hoặc RNA ngoại bào hoặc nội bào như các tín hiệu mô hình phân tử liên quan đến tổn thương, là phần thiết yếu của PRR. Khi kích hoạt, cảm biến axit nucleic có thể tạo ra các interferon loại I (IFN). IFN loại I được biết đến với vai trò quan trọng trong các phản ứng miễn dịch kháng vi rút. IFN loại I được tiết ra sẽ hoạt động trên các tế bào sản xuất và lân cận thông qua IFNα / βreceptor 1 (IFNAR1, ái lực đặc biệt cao với IFNβ) hoặc IFNAR1-IFNAR2 heterodimer. 14IFN loại I hỗ trợ tế bào lympho T gây độc tế bào (CTL) thông qua một số cơ chế. Thứ nhất, chúng thúc đẩy kích thích sự trưởng thành của các DC để cải thiện khả năng bắt mồi chéo với tế bào T; thứ hai, chúng làm tăng sự biểu hiện của perforin 1 và granzyme B để tăng cường chức năng của các tế bào T hiệu ứng; thứ ba, chúng có thể vô hiệu hóa chức năng ức chế của tế bào T (Treg) điều hòa; Cuối cùng, IFN loại I có thể ngăn chặn tế bào NK loại bỏ các CD8 + CTL được kích hoạt bởi kháng nguyên, và cảm ứng đại thực bào giải phóng các cytokine gây viêm (như IL-1β và IL-18). 15
Khi các chiến lược tổ hợp được yêu cầu và nâng cao, sự kết hợp của việc giải phóng nhiều phanh trên tế bào T thông qua ICI và giải phóng khả năng miễn dịch bẩm sinh để kích hoạt các chức năng của tế bào T là một chiến lược đầy hứa hẹn để kiểm soát sự phát triển của khối u. Ở đây, chúng tôi xem xét vai trò của cảm biến axit nucleic trong khả năng miễn dịch bẩm sinh hoặc thích ứng, và các cơ chế có thể ảnh hưởng đến độ nhạy và hiệu quả của ICI trong việc chống khối u. Cuộc thảo luận của chúng tôi tập trung vào những khám phá mới nhất về sức mạnh tổng hợp của khả năng miễn dịch bẩm sinh qua trung gian cảm biến axit nucleic và ICI là tín hiệu đầy hứa hẹn trong liệu pháp miễn dịch ung thư.
Cảm biến axit nucleic
Retinoic acid cảm ứng gen-I (RIG-I) giống như thụ thể
Các thụ thể RIG-I thích (RLR), bao gồm RIG-I, protein liên quan đến biệt hóa hắc tố 5 (MDA5) và phòng thí nghiệm về di truyền và sinh lý học 2 (LGP2), được biểu hiện trong bào tương của hầu hết các tế bào miễn dịch và không miễn dịch, bao gồm các tế bào ung thư. 16 RLR phổ biến trong việc chia sẻ miền DExD / H-box helicase và miền đầu C (CTD), những thứ cần thiết cho việc nhận biết các axit nhân ngoại sinh như RNA của virus. Ngoài ra, RIG-I và MDA5 chứa hai miền tuyển dụng và kích hoạt caspase song song đầu cuối N (CARD), chịu trách nhiệm tuyển dụng trong các thành phần tín hiệu hạ lưu và dẫn đến việc kích hoạt miễn dịch. Tuy nhiên, LGP2 thiếu CARD, dẫn đến các chức năng của LGP2 khác với RIG-I và MAD5 (Hình 1 ). 17
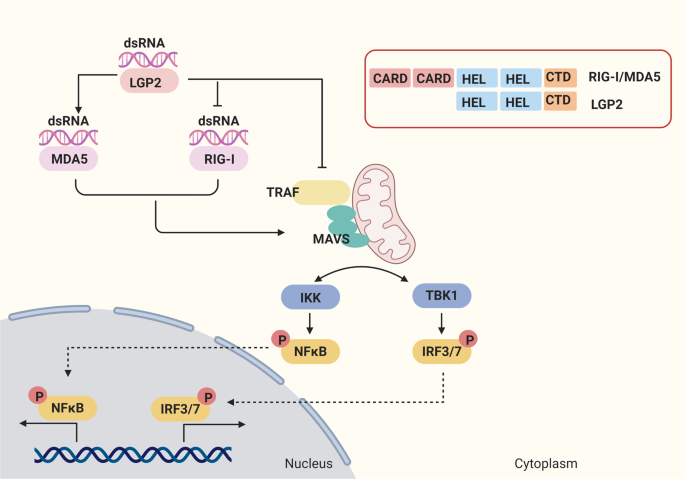
Con đường dẫn truyền tín hiệu qua trung gian RIG-I-like receptor (RLRs). Các thụ thể giống RIG-I (RLRs) đã được xác định là cảm biến RNA tế bào chất quan trọng, bao gồm RIG-I, MDA5 và LGP2. RLR phổ biến trong việc chia sẻ miền helicase DExD / H-box và miền đầu cuối C (CTD) và RIG-I và MDA5 chứa hai miền tuyển dụng và kích hoạt caspase N-terminal (CARD), trong khi LGP2 thiếu CARD. RIG-I phát hiện dsRNA ngắn của virus trong tế bào chất có chứa gốc 5′-triphosphate hoặc 5′-diphosphate, trong khi cấu trúc dsRNA dài được MDA5 công nhận. LGP2 có thể liên kết các phối tử RNA của RIG-I, can thiệp vào việc tuyển IKK vào MAVS thông qua tương tác protein hoặc liên kết với RIG-I thông qua miền ức chế trực tiếp, để ức chế sự hoạt hóa của RIG-I. LGP2 có thể làm tăng khả năng MDA5 hình thành các sợi ổn định trên dsRNA để thúc đẩy con đường trung gian MDA5. LGP2 tương tác với TRAF và làm gián đoạn hoạt động của nó, dẫn đến sự gián đoạn của IRF và kích hoạt NFκB. RIG-I và MDA5 được kích hoạt tạo ra sự tiếp nhận và trùng hợp của bộ tiếp hợp MAVS trên màng ty thể. Sau đó, MAVS kích hoạt TBK1 cũng như phức hợp IKK, kích hoạt IRF3 và IRF7, và NF-κB. Và sự biểu hiện gen của IFN, cytokine tiền viêm và chemokine được tạo ra để bảo vệ virus và điều chỉnh khả năng miễn dịch
RIG-I ban đầu được công nhận là một cảm biến kháng vi rút. 18 Ngược lại với siRNA tổng hợp, axit polyinosine-polycytidylic ngoại sinh (poly I: C, RNA tổng hợp) đã được chứng minh là kích hoạt RIG-I để tạo ra các phản ứng kháng vi-rút bẩm sinh bao gồm sản xuất IFN. RIG-I nhận biết RNA theo cách phụ thuộc vào trình tự, với dsRNA chủ yếu kết thúc bằng 5 ′ triphosphate (5’ppp). 19 Mặc dù MDA5 có sự tương đồng về trình tự cao với RIG-I, nó cảm nhận được các nhóm RNA virus khác nhau theo cách phụ thuộc vào độ dài. Một số nghiên cứu sinh hóa và cấu trúc cho thấy rằng dsRNA dài hơn có ái lực mạnh hơn với MDA5, có thể giữ ổn định hơn trong quá trình động học tạo mầm của MDA5 và cung cấp nền tảng cho MDA5 tương tác với các phân tử truyền tín hiệu xuôi dòng. 20 , 21
Sau khi nhận biết dsRNA thông qua CTD của RLRs, sự sắp xếp lại cấu trúc cho phép CARDs cảm ứng việc tuyển chọn và trùng hợp tín hiệu kháng virus ty thể tiếp hợp (MAVS) trên màng ty thể, đóng vai trò như một giá đỡ cho việc kích hoạt yếu tố liên quan đến thụ thể TNF (TRAF) họ (TRAF2,3,5,6). 22 Bên cạnh đó, TRAF truyền tín hiệu tuần tự từ MAVS đến kinase liên kết TANK 1 (TBK1) và IκB kinase (IKK), và kích hoạt các yếu tố phiên mã interferon yếu tố điều hòa 3 (IRF3) và yếu tố hạt nhân–B (NFκB) để kích thích phiên mã các IFN loại I và các cytokine gây viêm kháng khuẩn, tương ứng (Hình 1 ). 17Một thành viên khác của RLRs LGP2 ban đầu được coi là chất ức chế RIG-I cảm nhận tín hiệu IFN thông qua các phối tử RNA liên kết của RIG-I, can thiệp vào việc tuyển dụng IKK vào MAVS thông qua tương tác protein hoặc liên kết với RIG-I thông qua miền bộ kìm hãm trực tiếp. 17 , 23 , 24 , 25 Tuy nhiên, chuột trống LGP2 hiển thị phản ứng giảm đối với một số vi rút RNA được MDA5 phát hiện. 24 Kích hoạt thủy phân ATP cơ bản cao của LGP2 giúp tăng cường khả năng nhận dạng và đa dạng RNA của nó, làm tăng khả năng MDA5 hình thành các sợi ổn định trên dsRNA và hiệp đồng với MDA5 để tăng phản ứng kháng virus. 26LGP2 có thể tương tác với TRAF và làm gián đoạn hoạt động của nó, dẫn đến việc kích hoạt IRF3 và NFκB bị gián đoạn. 27 Do đó, chức năng của LGP2 có thể phụ thuộc vào ngữ cảnh.
RLRs biểu hiện trong các tế bào không miễn dịch bao gồm một số tế bào ung thư và sự kích thích RLRs thông qua phối tử của chúng bắt chước sự lây nhiễm vi-rút có thể gây ra quá trình apoptosis thông qua sự điều chỉnh của gen pro-apoptotic TRAIL và điều hòa giảm các gen chống apoptotic BCL2, BIRC3 và PRKCE qua IRF3 và IRF7. 28 , 29 Trong khi đó, kích hoạt RLR có thể kích thích các phản ứng miễn dịch bẩm sinh và thích ứng. Một mặt, các phối tử RLR có thể bắt chước sự lây nhiễm virus để kích hoạt trực tiếp các tế bào đuôi gai (DC). Mặt khác, việc kích hoạt RIG-I trong tế bào ung thư có thể tạo ra các tế bào tiền viêm như CXCL10, IL-6, IFNβ và điều chỉnh biểu hiện MHC-I trong tế bào ung thư, có thể kích thích các DC và sau đó kích hoạt độc tế bào Tế bào T. 30 ,31 , 32 , 33 Ngoài ra, RIG-I đã được kích hoạt có thể tuyển dụng bộ điều hợp ASC gây bệnh, kích hoạt caspase-1. Caspase-1 được kích hoạt có thể tạo ra sự trưởng thành của IL-1β, IL-18 và Gasdermin-D. Gasdermin-D được kích hoạt chuyển vào màng sinh chất và liên kết với nhau, tạo thành các lỗ và bắt đầu quá trình trương nở và ly giải tế bào giảm trương lực. 34 , 35
Các thụ thể giống như điện thoại di động
Một loại PRR khác là các thụ thể giống Toll (TLR), bao gồm ít nhất 11 thành viên, đóng vai trò quan trọng trong việc tạo ra các phản ứng miễn dịch bẩm sinh và thích ứng với kháng sinh. 36 , 37 Trong số các thành viên này, TLR3, TLR7, TLR8, TLR9 được phát hiện là đóng một vai trò thiết yếu trong việc cảm nhận axit nucleic (Hình 2 ). 36 Nói chung, TLR bao gồm miền ngoại bào tận cùng N (ECD), miền xuyên màng (TM) và miền thụ thể Toll / IL-1 tế bào chất ở đầu C (TIR). Miền ECD chịu trách nhiệm liên kết các mẫu phân tử liên quan đến mầm bệnh (PAMP) và các tầng tín hiệu được tiến hành thông qua miền TIR, miền này tuyển dụng protein bộ điều hợp chứa miền TIR bao gồm IFN-β (TRIF) hoặc Myd88 làm bộ điều hợp, để kích hoạt NFκB và IRF.38 Ví dụ, TLR3 được biểu hiện trên cả màng tế bào và màng trong của hầu hết các tế bào miễn dịch bẩm sinh. Sau khi nhận ra dsRNA 39 , 40 có nguồn gốc từ vi rútvà các cấu trúc gốc không hoàn chỉnh chứa RNA ssRNA sợi đơn trongcác ống nội tạng, 41 TLR3 sắp xếp và thu nạp TICAM-1, và sau đó kích hoạt IRF3 và NFκB, để tăng cường sản xuất IFN loại I như IFNβand các cytokine tiền viêm như TNF-α và IL-6. 42 TLR7 và TLR8 đều là TLR được bản địa hóa của endosome. Họ nhận ra ssRNA của virus, các hợp chất imidazoquinoline và các chất tương tự guanosine, đồng thời tuyển dụng MyD88 để kích hoạt NFκB và IRF7. 43 , 44 TLR7 được kích hoạt bởi các RNA can thiệp nhỏ tổng hợp (siRNA), 45lncRNA FMR1-AS1 exosomal, các ssRNA như microRNA let-7, 46 ssRNA có nguồn gốc từ tế bào chết, 47 và guanosine cũng như các dẫn xuất của nó. 48 Ngược lại, TLR8 cảm nhận được uridine, oligonucleotide và các sản phẩm thoái hóa của ssRNA. 49 Mặc dù có độ tương đồng cao, TLR7 được biểu hiện trong các tế bào DC plasmacytoid (pDCs) và tế bào B trong khi TLR8 chủ yếu biểu hiện trong các đại thực bào, bạch cầu đơn nhân và cDC. 41 Kích hoạt TLR7 / 8 thông qua chất chủ vận nội cơ trong mô hình ung thư hắc tố gây ra sự sản sinh CCL2 để tạo điều kiện thuận lợi cho sự xâm nhập của đại thực bào M1, tế bào T CD8 +, tế bào B. 50
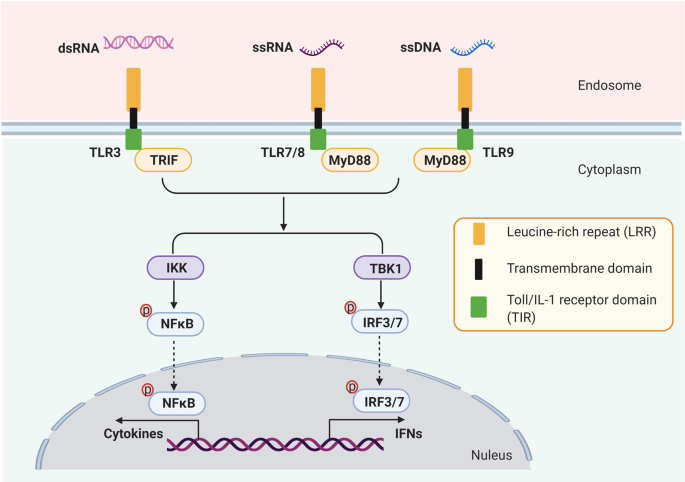
Con đường dẫn truyền tín hiệu qua trung gian thụ thể Toll-like (TLRs). Các thụ thể giống như điện thoại di động (TLR) bao gồm ít nhất 11 thành viên. Trong số 11 thành viên, TLR3, TLR7, TLR8, TLR9 được tìm thấy khu trú trên màng nội tiết và đóng một vai trò thiết yếu trong việc cảm nhận axit nucleic. TLR3 có thể phát hiện dsRNA và ssRNA được TLR7 và TLR8 công nhận. Và mô típ CpG chưa được methyl hóa của ssDNA có thể kích hoạt TLR9. TLR bao gồm miền ngoại bào tận cùng N (ECD), miền xuyên màng (TM) và miền thụ thể Toll / IL-1 tế bào chất ở đầu C (TIR). Miền ECD chịu trách nhiệm liên kết các mẫu phân tử liên quan đến mầm bệnh (PAMP) và các tầng tín hiệu được thực hiện thông qua miền TIR, miền này tuyển TRIF hoặc Myd88 làm bộ điều hợp, để kích hoạt NFκB và IRFs
TLR9 được biểu hiện chủ yếu ở các tế bào pDC và tế bào B, và mô-típ CpG không được methyl hóa của ssDNA là không thể thiếu để kích thích TLR9. 51 Bằng cách xử lý DNA sợi đôi (dsDNA, chẳng hạn như DNA nhiễm sắc thể và ty thể) thành ssDNA ngắn, DNase là yếu tố cần thiết để kích hoạt TLR9. 52 Khi bị nhiễm trùng, TLR9 rất quan trọng để bắt đầu đáp ứng miễn dịch bẩm sinh bằng cách tăng các tế bào tiền viêm và kích hoạt các tế bào NK gây độc tế bào và tế bào T CD8 +. 53
con đường cGAS-STING
Chuỗi tổng hợp GMP-AMP chu kỳ (cGAS) lần đầu tiên được xác định là cảm biến DNA sợi kép tế bào (dsDNA) vào năm 2013. 54 Sau khi liên kết trực tiếp với DNA, cGAS có thể che giấu GTP và ATP thành GMP-AMP theo chu kỳ (cGAMP) để tạo thành chất truyền tin thứ hai 2′3′-cGAMP để kích hoạt bộ kích thích của gen interferon (STING). 55 Sau khi bị ràng buộc bởi 2’3′-cGAMP, STING chuyển vị trí từ ER sang Golgi để tạo thành một phức hợp với TBK1 hoặc IKK. TBK1 được kích hoạt STING có thể phosphoryl hóa IRF3, thúc đẩy quá trình dime hóa IRF3 và chuyển vị vào nhân nơi nó gây ra sự phiên mã của nhiều gen viêm, đặc biệt là IFNβ. Mặt khác, IKK được STING kích hoạt có thể phosphoryl hóa IκBα, dẫn đến sự chuyển vị của NFκB đến nhân, và sau đó kích hoạt phiên mã của các cytokine tiền viêm (Hình.3 ). 56
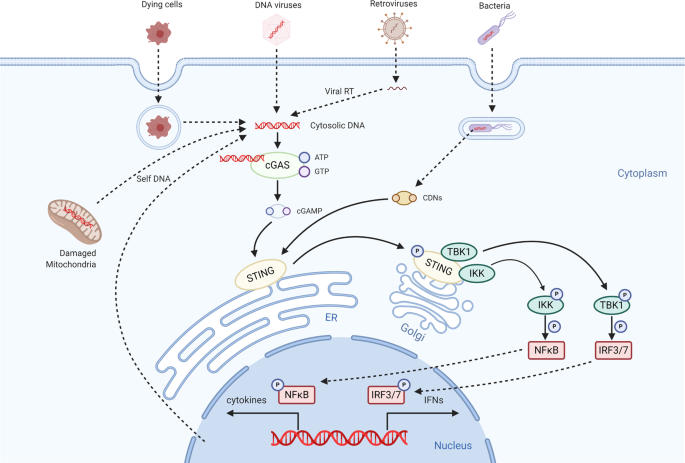
cGAS / STING- con đường dẫn truyền tín hiệu qua trung gian. Là bộ cảm biến DNA của tế bào, cGAS nhận dạng dsDNA từ virus DNA hoặc dsDNA được tạo ra bởi retrovirus. Sau khi phát hiện DNA, cGAS tổng hợp cGAMP thông tin thứ hai, sau đó liên kết và kích hoạt STING trên lưới nội chất (ER). Ngoài ra, STNG có thể cảm nhận các CDN. STING được kích hoạt chuyển vị trí từ ER đến Golgi để tạo thành phức hợp với TBK1 hoặc IKK. Sự kích hoạt TBK1 hoặc IKK gây ra sự biểu hiện của gen IFN loại I và các cytokine gây viêm khác thông qua trục TBK1-IRF3 / 7 và NF-κB
Mặc dù DNA ngoại lai hoặc DNA tự thân có thể kích hoạt cGAS theo cách phụ thuộc vào độ dài, nhưng 57 tế bào khỏe mạnh có thể tiêu hóa chính xác dsDNA của vật chủ thông qua DNase hoặc ngăn cách DNA trong nhân hoặc ty thể để ngăn chặn sự kích hoạt sai lệch của con đường cGAS-STING. 56 Tương ứng, đột biến DNase hoặc STING, sự tích tụ DNA tự gây ra do tổn thương DNA, mất ổn định nhiễm sắc thể, rối loạn chức năng ti thể, v.v., có thể kích hoạt con đường cGAS-STING không ổn định, do đó dẫn đến các bệnh viêm khác nhau, bao gồm cả ung thư.
Ảnh hưởng
Inflammasomes là những phức hợp đa protein lớn để làm trung gian cho sự trưởng thành và bài tiết của các cytokine, và quá trình pyroptosis. Có ba thành phần trong một đèn chiếu sáng điển hình: cảm biến, bộ chuyển đổi và bộ tạo hiệu ứng. Và các cảm biến viêm nhiễm thường được chia thành ba loại: (1) Không có melanoma 2 pyrin và biểu hiện tạo máu, cảm ứng interferon, khu trú hạt nhân và miền 200 axit amin đặc trưng (HIN200) chứa họ protein (PYHIN), (2) vùng liên kết nucleotide và vùng lặp lại giàu leucine (NLR) chứa họ protein, (3) thành viên họ TRIM, Pyrin. Cảm biến Inflammasome có thể phát hiện sự hiện diện của phân tử có nguồn gốc từ mầm bệnh, bao gồm axit nucleic, chất chuyển hóa, v.v. Các protein tiếp hợp cung cấp tín hiệu từ các cảm biến đến các hiệu ứng thông qua tương tác protein-protein. 58Và tác động thúc đẩy sự phân cắt các cytokine tiền viêm (pro-IL-1β và pro-IL-18) và Gasdermin D, dẫn đến việc tiết interleukin-1β trưởng thành (IL-1β) và IL-18 và pyroptosis ( Hình 4 ). 59 IL-18 đã được chứng minh là tạo ra IFNγ, tăng hoạt động của tế bào NK và tăng sinh tế bào T. 60 , 61 IL-1 có thể thúc đẩy sự phân cực Th17 để tiết ra IL-17 cùng với IFNγ. 62 Hơn nữa, IL-1 có thể thúc đẩy tăng sinh tế bào T, và ngăn chặn tế bào T điều hòa và sản xuất IL-10 của tế bào T. Paracrine của IL-1 có thể đóng góp vào các DC trưởng thành, thúc đẩy phản ứng của tế bào T CD8 +. 63
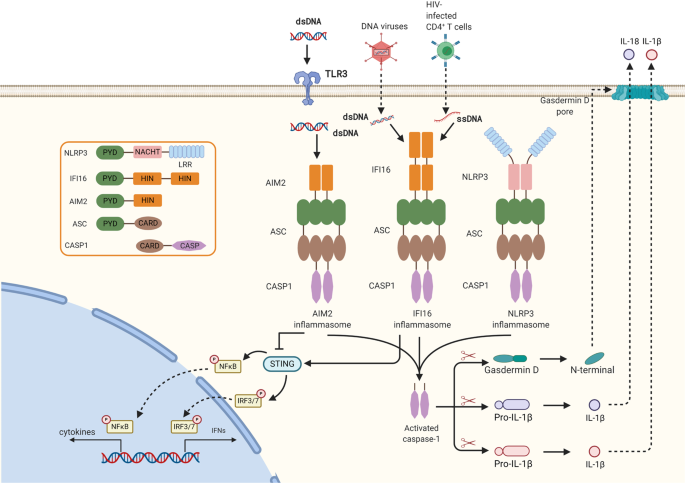
Con đường dẫn truyền tín hiệu qua trung gian ảnh hưởng. Cảm biến DNA AIM2 và IFI16 bao gồm miền pyrin đầu cuối N và miền HIN-200 đầu cuối C. DNA của tế bào sinh ra kích hoạt AIM2 hoặc IFI16. Miền HIN-200 tương tác với DNA, trong khi miền pyrin liên kết với miền pyrin của ASC. CARD của ASC liên kết CARD của pro-caspase-1, kích hoạt caspase-1. Các ổ caspase-1 được kích hoạt phân tách pro-IL-1β, pro-IL-18 và Gasdermin D. Ngoài ra, IFI16 được kích hoạt có thể tuyển dụng STING để kích hoạt IRF3 và NFκB để tạo ra interferon loại I
Trong số ba loại cảm biến, các thành viên gia đình PYHIN vắng mặt trong khối u ác tính 2 (AIM2) và protein interferon-γinducible 16 (IFI16) được coi là cảm biến DNA. 64 AIM2 bao gồm miền pyrin đầu cuối N (PYD) và miền HIN-200 đầu cuối C. dsDNA liên kết với miền HIN của AIM2 để giải phóng miền PYD của AIM2. Và miền PYD miễn phí tương tác với protein tiếp hợp gen viêm nhiễm có chứa PYD-CARD có chứa protein dạng đốm liên quan đến apoptosis có chứa CARD tận cùng carboxy (ASC) thành các sợi xoắn, dẫn đến việc kích hoạt caspase-1 của effector. 65 IFI16 chứa PYD và hai miền HIN, là DNA cảm nhận protein chứa PYD đầu tiên làm trung gian cho cảm ứng IFNβ. 66IFI16 nhận dạng dsDNA từ vi rút DNA xâm nhập, ssDNA từ tế bào T CD4 + bị nhiễm HIV và DNA bị hư hỏng nhân từ các tế bào sừng được xử lý bằng etoposide. 67 , 68 , 69 Ngoài việc kích hoạt thể viêm phụ thuộc ASC-caspase 1 để tạo ra IL-1β, 69 IFI16 được kích hoạt có thể tuyển dụng STING để kích hoạt IRF3 và NFκB để tạo ra IFN loại I. 68 Một nghiên cứu khác cho thấy STING có thể tương tác trực tiếp với IFI16 và tạo điều kiện thuận lợi cho IFI16 phổ biến trên lysine3 / 4/6 và phân hủy thông qua con đường ubiquitin-proteasome bằng cách tuyển dụng ubiquitin E3 ligase TRIM21. 70 Ngoài ra, trong quá trình Mycobacterianhiễm trùng, các viêm nhiễm qua trung gian AIM2 hoạt hóa có thể tương tác với STING và ngăn chặn sự hoạt hóa của TBK1 và IRF3, do đó ức chế cảm ứng IFN-β. 71
NLR chứa protein 3 (NLRP3) đã được đặc trưng rõ ràng để đóng những vai trò quan trọng trong việc lây nhiễm virus và cảm nhận axit nucleic của virus. 64 Tuy nhiên, vẫn chưa rõ liệu NLRP3 có cảm nhận trực tiếp DNA hay RNA của virus hay không.
Các cảm biến axit hạt nhân khác
Protein liên kết Z-DNA 1 (ZBP1) có thể liên kết trực tiếp dsDNA và kích hoạt phản ứng bẩm sinh thông qua việc kích hoạt IRF3 và NFκB. 72 Ngoài ra, nó có thể cảm nhận RNA để kích hoạt quá trình hoại tử thông qua việc tuyển dụng RIPK3 để phosphoryl hóa và kích hoạt MLKL, dẫn đến cái chết của tế bào bị nhiễm virus. 73 LRRFIP1 đã được báo cáo là nhận ra cả RNA và DNA từ virus hoặc vi khuẩn, điều này có thể dẫn đến sự tích tụ và chuyển vị sau đó vào nhân của β-catenin để tăng cường sự chuyển hóa của IRF3. 74 Helicase hộp DEAD 41 (DDX41) có thể cảm nhận dsDNA hoặc c-di-GMP để tạo ra miễn dịch bẩm sinh thông qua liên kết và kích hoạt STING trực tiếp để kích hoạt các yếu tố phiên mã IRF3 và NFκB. 75Protein kinase được kích hoạt bằng RNA (PKR) có thể nhận ra dsRNA dài của virus trong quá trình nhiễm HCV, sau đó trải qua quá trình dime hóa và autophosphoryl hóa. PKR được phosphoryl hóa có thể chặn bắt đầu dịch mã thông qua phosphoryl hóa eIF2 trên Ser51 để gây chết tế bào, 76 và kích hoạt NFκB thông qua phosphoryl hóa IKKB để tạo ra miễn dịch bẩm sinh. 77 Một nhóm xoắn RNA khác không phải RLR cũng có thể cảm nhận RNA và làm trung gian cho bệnh viêm, hoặc tăng cường tín hiệu RLR để tăng cường phản ứng IFN và tác dụng ức chế nhiễm virus. 78 Một nghiên cứu báo cáo rằng, khi liên kết với dsDNA, miền CARD của họ thụ thể giống NOD chứa 3 (NLRC3) có thể giải phóng STING khỏi sự cô lập của nó, gây ra kích hoạt miễn dịch qua trung gian STING. 79
Sự kết hợp của miễn dịch cảm ứng axit hạt nhân với ICI như một chiến lược đầy hứa hẹn trong liệu pháp miễn dịch ung thư
Với vai trò chính của các đáp ứng miễn dịch cảm ứng axit nhân trong việc kích hoạt các chức năng của tế bào T, có nhiều nghiên cứu khác nhau chỉ ra những ưu điểm của việc kích hoạt miễn dịch cảm ứng axit nhân để tăng cường tác dụng của ICI trong liệu pháp miễn dịch ung thư (tóm tắt trong Bảng 1 ).
Việc sử dụng chất chủ vận cảm biến
RIG-Tôi thích các phối tử thụ cảm
Các phối tử thụ thể giống RIG-I đã được chứng minh là có triển vọng trong điều trị các khối u ác tính như ung thư vú, u ác tính, ung thư tuyến tụy và bệnh bạch cầu dòng tủy cấp tính (AML) trong các mô hình tiền lâm sàng. 31 , 80 , 81 , 82 Kích hoạt RIG-I thông qua loại bỏ khối u ngắn 5’ppp-RNA gây ra và hình thành bộ nhớ miễn dịch trong mô hình bệnh bạch cầu cấp dòng tủy (AML) do cảm ứng IFN loại I để tăng mức CXCL10 để kích hoạt Tế bào T CD4 + và CD8 + . 82 Theo đó, xử lý 5’ppp-RNA có thể nhạy cảm với điều trị ICIs in vivo. 82 , 83 , 84Trong các mô u ác tính nguyên phát ở người, sự biểu hiện cao của RIG-I có liên quan đến việc kích hoạt thụ thể tế bào T và con đường trình bày kháng nguyên, kéo dài thời gian sống thêm của bệnh nhân và đáp ứng lâm sàng lâu dài với phong tỏa điểm kiểm soát chống CTLA-4. 85 Do đó, sự biểu hiện cao của RIG-I trong tế bào ung thư có thể cho thấy phản ứng tốt hơn với phong tỏa điểm kiểm tra miễn dịch mà vẫn cần được nghiên cứu thêm.
Kích hoạt MDA5 thông qua poly I: C trong các tế bào ung thư tuyến tụy, gây ra quá trình chết rụng và sản xuất IFN loại I và các cytokine tiền viêm, dẫn đến việc kích hoạt các DC. Và các CD8α + DC được kích hoạt đã nhấn chìm vật liệu khối u apoptotic và trình bày chéo kháng nguyên liên kết với khối u vào các tế bào T CD8 + chưa từng biết , gây ra sự ly giải qua trung gian tế bào lympho T gây độc tế bào (CTL). 86
Theo đó, nghiên cứu lâm sàng giai đoạn I / II đã được thực hiện để đánh giá tính an toàn, khả năng dung nạp và hoạt động chống khối u của việc tiêm thuốc trong khoang miệng (IT) / tiêm trong miệng (IL) chất chủ vận của RIG-I, MK-4621 (RGT100), dưới dạng đơn trị liệu hoặc kết hợp với pembrolizumab ở những người tham gia có khối u rắn tiến triển (NCT03065023 và NCT03739138, được tóm tắt trong Bảng 2 ).
Chất chủ vận TLRs
Với vai trò quan trọng của TLR trong việc kích hoạt khả năng miễn dịch bẩm sinh, nhiều tác nhân khác nhau đã được tìm thấy để điều chỉnh khả năng miễn dịch chống lại khối u. 87 , 88
Một phối tử nhân tạo với TLR3, một phân tử lai DNA-dsRNA tổng hợp (ARNAX) có thể kích hoạt các tế bào đuôi gai trình diện kháng nguyên để tạo ra sự tăng sinh tế bào lympho T gây độc tế bào thông qua con đường TLR3-TICAM-1-IRF3-IFNβ. 89Mặt khác, nó có thể thiết lập một vi môi trường ức chế khối u thông qua việc gây ra sự biểu hiện của các gen liên quan đến tuyển dụng DCs bao gồm CCL4, CCL5 và CCL27. Ngoài ra, điều trị ARNAX với kháng nguyên liên kết khối u có thể gây ra biểu hiện mRNA của các gen liên quan đến độc tính tế bào (IFNγ, Gzmb và Prf1) và các chemokine tuyển dụng các CTL (Cxcl9 và Cxcl10) trong các khối u, gây ra sự xâm nhập CTL của tác nhân và tạo điều kiện cho Th1- loại miễn dịch chống khối u trên mô hình chuột. Tuy nhiên, sự kết hợp của kháng thể kháng PD-L1 với chất bổ trợ đặc hiệu TLR3 (ARNAX + Kháng nguyên khối u) gây ra phản ứng hồi quy khối u hiệu quả hơn trong mô hình chuột. 90Và sự gia tăng được đánh giá của CTL đặc hiệu kháng nguyên của tế bào đơn nhân máu ngoại vi của người (PBMC) đã được quan sát thấy thông qua điều trị ARNAX kết hợp với TAA. Tuy nhiên, ARNAX vẫn chưa được phát triển lâm sàng.
Poly-ICLC (Hiltonol) là một Poly-IC tổng hợp có thể tạo ra các tế bào NK cụ thể của khối u, CTLs và các phản ứng miễn dịch qua trung gian tế bào NK-T thông qua việc kích hoạt TLR3 và MDA5. 91 , 92 Ngoài ra, poly-ICLC được chứng minh là chất bổ trợ hiệu quả cho các tế bào T CD8 + đặc hiệu với kháng nguyên nguyên tố và kéo dài thời gian sống sót Trong các mô hình u thần kinh đệm và u hắc tố ở chuột. 93 Và các nghiên cứu lâm sàng khác nhau đã tiết lộ sự đóng góp của Poly-ICLC cùng với các kháng nguyên đặc hiệu cho khối u để cải thiện các phản ứng miễn dịch. 91 , 92 , 94
BO-112 là một dạng phức hợp nano của Poly I: C, có thể kích hoạt các cảm biến như TLR3 và MDA5. Điều trị BO-112 trong khoang miệng dẫn đến sự thoái triển đáng kể của khối u phụ thuộc vào IFN loại I và gamma-interferon trên các mô hình chuột. 89 Hơn nữa, các tế bào lympho T CD8 + phong phú hơn và các tế bào lympho T gây độc tế bào đặc hiệu với kháng nguyên của khối u đã được tìm thấy sau khi điều trị BO-112 trong khoang. Và việc sử dụng BO-112 trong khoang miệng cho thấy hiệu quả đơn phương đối với song phương ở chuột mang khối u kết hợp với kháng thể đơn dòng kháng PD-L1 toàn thân. 89
Chất chủ vận của TLR7, Imiquimod (còn được gọi là R-837) là một chất điều chỉnh phản ứng miễn dịch và đã được Cơ quan Quản lý Thực phẩm và Dược phẩm Hoa Kỳ (FDA) phê duyệt để điều trị ung thư biểu mô tế bào đáy bề mặt, mụn cóc sinh dục và dày sừng quang hóa. 95 Trong mô hình ung thư vú, Imiquimod kết hợp với chiếu tia laser có thể kích hoạt tế bào NK, đại thực bào và tế bào lympho B thông qua các cytokine cảm ứng TLR-7 (IFN-α, IL-6 và TNF-α) để tăng cường hơn nữa sự hoạt hóa của đáp ứng miễn dịch. Và nó có thể tạo ra nhiều tế bào T CD8 + , CD3 + , CD4 + và PD-1 + trong các khối u ở xa. Do đó, Imiquimod kết hợp với chiếu xạ có thể làm tăng đáp ứng với kháng thể kháng PD-1. 96Hơn nữa, người ta đã mô tả rằng một số trường hợp bệnh nhân u ác tính được điều trị thành công với sự kết hợp của ipilimumab và Imiquimod. 97 , 98
Chất Resiquimod chủ vận TLR7 / 8 (R848) được tiết lộ để kích hoạt pDCs và cDCs in vivo, giúp tăng cường tế bào T mồi trong các hạch bạch huyết khu vực. Và kết hợp điều trị kháng thể PD-L1 với resiquimod rất hữu ích để giảm sự phát triển của khối u trong hai mô hình khối u kháng phong tỏa PD-L1. 99 Tuy nhiên, một số nghiên cứu lâm sàng cho thấy rằng resiquimod làm chất bổ trợ cho vắc-xin ung thư hắc tố không đủ để tạo ra các đáp ứng nhất quán của tế bào T CD8 + đặc hiệu với kháng nguyên . 100 , 101 3M-025 là một chất chủ vận TLR7 / 8 khác, có thể gây tăng mức độ chemokine CCL2, thâm nhập vào các đại thực bào đã chuyển kiểu hình M1, các tế bào T gây độc tế bào trong mô hình chuột u ác tính. 50Trong khi đó, các hạt nano được nạp chất chủ vận TLR7 / 8 với ái lực của đại thực bào liên quan đến khối u (TAM) có thể đảo ngược sự phân cực của TAM từ kiểu hình giống M2 (chống viêm) sang kiểu hình giống M1 (chống viêm) và ức chế sự phát triển của khối u trong cách thức phụ thuộc vào tế bào T CD8 + trong cơ thể sống. 102 Theo đó, sự kết hợp của TLR7 / 8 với anti-PD-1 và anti-CTLA-4 dẫn đến sự kết hợp của sự thoái triển khối u. 50
Motolimod (VTX-2337) là một chất chủ vận TLR8 đặc hiệu, kích hoạt tế bào NK và tăng cường độc tính tế bào phụ thuộc vào kháng thể (ADCC). 103 Ngoài ra, motolimod có thể tạo điều kiện kích hoạt tế bào NK và tế bào đuôi gai bắt mồi chéo tế bào T CD8 + đặc hiệu của khối u trong ung thư đầu và cổ. 104
IMO-2125, chất chủ vận của TLR9, được tiết lộ là dẫn đến việc sản xuất các cytokine và chemokine loại Th1. 105 Điều trị IMO-2125 trực tiếp vào một khối u dẫn đến sự thoái lui khối u mạnh mẽ của các khối u ở xa được tiêm và không được tiêm thông qua phản ứng Th1 hướng tế bào CD8 + với bộ nhớ đặc hiệu khối u dài hạn trong mô hình chuột ung thư biểu mô ruột kết. 106 Và các thử nghiệm lâm sàng giai đoạn I / II đã chỉ ra rằng sự kết hợp của IMO-2125 và Ipilimumab được dung nạp tốt và tích cực thúc đẩy các phản ứng miễn dịch chống khối u trong khối u ác tính. Việc điều trị gây ra đáp ứng ngay cả ở các khối u ở xa không được điều trị bằng IMO-2125 (NCT02644967). 107
Điều trị nội nhãn bằng chất chủ vận TLR9, SD-101, kích thích TLR9 của pDC, có thể khiến pDC giải phóng IFN và trưởng thành, do đó có thể gây ra sự xâm nhập và mở rộng của tế bào T CD8 + . Và theo đó, phương pháp điều trị SD-101 có thể vượt qua khả năng kháng thuốc phong tỏa PD-1 trên mô hình chuột ung thư biểu mô ruột kết. 108 CMP-001, một chất chủ vận khác của TLR9 cũng có thể tạo điều kiện thuận lợi cho phản ứng miễn dịch chống khối u bao gồm sự gia tăng biểu hiện của chemokine, cytokine tiền viêm và sự thâm nhập của tế bào CD8 + T và NK, giúp cải thiện sự sống sót trong ung thư biểu mô ruột kết và tuyến tụy ung thư. 109Hơn nữa, có cảm hứng rằng các chất chủ vận của TLR9, CMP-001 và SD-101, có thể kích thích TLR9 và khiến pDC tiết ra IFN loại I và các chemokine gây viêm, đồng thời tạo điều kiện cho tế bào T gây độc tế bào thâm nhập để có khả năng vượt qua sự kháng thuốc phong tỏa PD-1 ở bệnh nhân u ác tính di căn. 110 , 111 , 112
Dựa trên những bằng chứng hứa hẹn này trong các nghiên cứu tiền lâm sàng, một số thử nghiệm lâm sàng đã được tiến hành với chất chủ vận TLR kết hợp với ICI để đánh giá hiệu quả lâm sàng tiềm năng (tóm tắt trong Bảng 2 ).
Chất chủ vận STING
Vì STING được biểu hiện rộng rãi trong các loại tế bào khác nhau trong các mô khối u, các chất chủ vận STING tổng hợp như dinucleotide chu kỳ (CDN) hoặc chu kỳ di-GMP (CDG), có thể kích thích con đường STING trong DC, đại thực bào, tế bào B và các bạch cầu khác để tạo ra sản xuất IFN loại I. IFN, theo cách tự nội tiết hoặc nội tiết, có thể tạo điều kiện thuận lợi cho việc trình bày kháng nguyên tới các tế bào T CD4 + và CD8 + của DC, và tạo mồi cho các tế bào NK, giúp tăng cường phản ứng kháng u. 113 Nhiều nỗ lực tập trung vào sự phát triển của CDN đã được sửa đổi hoặc các phân tử nhỏ khác. 114Các chất chủ vận STING đã cho thấy lợi ích điều trị đáng kể thông qua việc tăng khả năng thâm nhập CD8 + TIL qua trung gian DCs vào vi môi trường khối u trong các mô hình chuột bị ung thư tế bào hắc tố, bệnh bạch cầu cấp dòng tủy, ung thư vú và đại trực tràng. Điều trị bằng vắc xin ung thư công thức chủ vận 115 , 116 , 117 STING (STINGVAX) có thể làm tăng khối u xâm nhập vào tế bào T CD8 + IFNγ + với cơ chế điều hòa PD-L1 rõ rệt trong mô hình chuột u ác tính, có thể nhạy cảm với phong tỏa PD-1. 115 Chất chủ vận STING gây ra các cytokine tiền viêm toàn thân, xử lý và trình bày kháng nguyên trong DC cũng như tăng PD-1 + CD8 +Tỷ lệ tế bào T ở chuột bị ung thư biểu mô buồng trứng dạng huyết thanh cao. Sự kết hợp của carboplatin với chất chủ vận STING và phong tỏa PD-1 đã kéo dài đáng kể thời gian sống sót của những con chuột này. 118 Tương tự, các chất chủ vận STING như ADU-S100 (còn được gọi là MIW815 hoặc ML RR-S2 CDA), 2′3′-c-di-AM (PS) 2 (Rp, Rp) và di-GMP tuần hoàn có thể tăng cường hiệu quả điều trị của liệu pháp miễn dịch kháng PD-1 / PD-L1 trong ung thư ruột kết, ung thư miệng do HPV + , ung thư tuyến tụy, ung thư tuyến tiền liệt, v.v. 119 , 120 , 121
Do đó, sự kết hợp của chất chủ vận STING với ICI được hứa hẹn sẽ tăng cường tác dụng của ICI trong liệu pháp chống khối u bằng cách kích hoạt miễn dịch bẩm sinh và thích ứng. Kết quả là, có một số thử nghiệm lâm sàng đang được thực hiện (tóm tắt trong Bảng 2).
Cảm ứng RNA tế bào chất
Ngoài ra, có những chiến lược khác để kích thích cảm biến axit hạt nhân như cảm ứng RNA hoặc DNA tế bào chất từ vật chủ để bắt chước sự lây nhiễm của vi sinh vật. Ví dụ, sự ức chế histone H3K4 demethylase LSD1 trong các tế bào khối u làm tăng các phiên mã trình tự retrovirus nội sinh (ERVs), cho phép hình thành dsRNA. Và LSD1 có thể tạo ra sự ổn định protein của AGO2 thông qua việc tăng cường quá trình methyl hóa AGO2. AGO2 là thành phần quan trọng của phức hợp tạo ra sự im lặng do RNA (RISC) tạo ra, làm trung gian cho sự im lặng của RNA. Do đó, sự ức chế LSD1 làm tăng sự tích tụ của dsRNA, được cảm nhận bởi MDA5 và TLR3, sau đó kích hoạt sự biểu hiện của IFNs và biểu hiện MHC-I trong các tế bào khối u. Ngoài ra,122 , 123 Hơn nữa, LSD1 biểu hiện quá mức trong các khối u so với các mô bình thường trong nhiều loại ung thư, điều này cho thấy LSD1 là một mục tiêu đầy hứa hẹn để tăng cường tác dụng của ICI. 122
Bên cạnh đó, việc xử lý chất khử methyl DNA 5-AZA-CdR trong tế bào khối u có thể gây ra sự phiên mã của các ERV cụ thể và làm tăng các dsRNA của tế bào chất. Và sự gia tăng của dsRNA được phát hiện thông qua MDA5, điều này tiếp tục gây ra phản ứng IFN để chống lại khối u. 124 , 125 Ngoài ra, điều trị 5-AZA-CdR có thể tăng cường hiệu quả chống khối u của kháng thể chống CTLA-4 trên mô hình chuột ung thư vú, có thể liên quan đến khả năng phòng vệ virus cao. 126
Các nghiên cứu gần đây cho thấy các đột biến tăng chức năng của MDA5 (GOF MDA5) dẫn đến sự kích hoạt sai lệch tín hiệu của nó, dẫn đến một loạt các rối loạn miễn dịch, chẳng hạn như hội chứng Aicardi-Goutières (AGS) và lupus ban đỏ hệ thống (SLE). 127 , 128 , 129 Nghiên cứu sâu hơn chỉ ra rằng con lai Alu: Alu được hình thành từ sự lặp lại ngược (IRs) có nhiều trong tế bào, là phối tử chính của GOF MDA5, trong khi loại hoang dã MDA5 có khả năng nhận ra con lai Alu: Alu rất hạn chế. Điều thú vị là dưới sự thiếu hụt ADAR1 (một trình biên tập RNA từ A đến I), các cây lai Alu: Alu không biến đổi có thể kích hoạt MDA5 kiểu hoang dã một cách đáng kể, 130điều này dẫn đến việc sản xuất IFN loại I đáng kể. Mặt khác, khi đáp ứng IFNs, việc xóa ADAR1 có thể kích hoạt một cảm biến dsRNA khác, PKR để tạo ra quá trình apoptosis ở một số dòng tế bào ung thư. 131 Hơn nữa, mất ADAR1 có thể khắc phục khả năng kháng phong tỏa điểm kiểm soát PD-1 do sự gia tăng đáng kể trong sản xuất IFNs và các tế bào miễn dịch, bao gồm tế bào T CD4 + , tế bào T CD8 + , tế bào NK và giảm dòng tủy loại M2 ô trong mô hình chuột. 132
Chất ức chế kinase 4 và 6 (CDK4 / 6) phụ thuộc cyclin đã cho thấy hoạt động đáng kể trong việc ức chế chất ức chế khối u nguyên bào võng mạc phosphoryl hóa (RB), và sau đó gây ra sự ngừng chu kỳ tế bào G1 trong các tế bào khối u. 133 Ngoài việc gây ra sự bắt giữ chu kỳ tế bào, chất ức chế CDK4 / 6 có thể làm giảm hoạt động của DNA methyltransferase 1 (DNMT1) trong tế bào ung thư vú, làm giảm sự methyl hóa DNA ở trình tự ERV và tăng mức dsRNA trong tế bào khối u. Mức độ cao của dsRNA kích hoạt các thụ thể nhận dạng RNA như RIG-I, LGP2 và MDA5, do đó kích thích sản xuất IFN loại I và do đó tăng cường trình bày kháng nguyên khối u. Ngoài ra, chất ức chế CDK4 / 6 ngăn chặn sự gia tăng của Tregs và thúc đẩy sự thanh thải qua trung gian tế bào T của tế bào khối u. 134Các nghiên cứu in vitro và in vivo cho thấy ức chế CDK4 / 6 dẫn đến tăng hoạt động chống khối u và nhạy cảm với phong tỏa PD-1. 135
Do đó, các nghiên cứu trên chỉ ra rằng cảm ứng RNA tế bào chất để tạo ra miễn dịch bẩm sinh trong khối u thông qua xóa LSD1 hoặc ADAR1, hoặc điều trị chất khử methyl DNA hoặc chất ức chế CDK4 / 6, cho thấy hiệu quả đầy hứa hẹn khi kết hợp với ICI để chống khối u. Tuy nhiên, các nghiên cứu sâu hơn có lẽ sẽ tập trung vào dịch lâm sàng như phát minh chất ức chế LSD1 và ADAR1.
Cảm ứng DNA tế bào chất
Kể từ khi một số nghiên cứu quan trọng tiết lộ việc giám sát các vi nhân bằng cGAS, người ta đã chú ý nhiều đến sức mạnh tổng hợp giữa tổn thương DNA và ICI. 136 , 137 Tích lũy DNA tế bào chất trong vi nhân của tế bào khối u, được gây ra bởi các tác nhân bức xạ hoặc hóa trị (như cisplatin và etoposide), tắc nghẽn sửa chữa tổn thương DNA (như ức chế PARP và thiếu BRCA1) và ức chế CHK1 để ngăn chặn chu kỳ tế bào bắt giữ trong quá trình sửa chữa tổn thương DNA, có thể kích hoạt con đường cGAS-STING để tạo ra khả năng miễn dịch bẩm sinh. 138 , 139 , 140 , 141
Tuy nhiên, có những cơ chế khác nhau. Ví dụ, xạ trị có thể làm nhạy cảm các ICI, có thể được trung gian thông qua các tế bào T đa dòng thường trú và xâm nhập, sự đa dạng của các thụ thể tế bào T (TCR) của tế bào T trong khoang sau bức xạ. 142 , 143Ataxia Telangiectasia Mutated (ATM) là một thành phần quan trọng trong phản ứng tổn thương DNA (DDR) và đóng một vai trò quan trọng trong việc đáp ứng với điều trị bức xạ gây ra đứt gãy sợi kép DNA. Trong ung thư tuyến tụy, việc ức chế ATM đơn lẻ hoặc kết hợp với bức xạ có thể làm tăng quá trình phosphoryl hóa tyrosine kinase Src và sự phosphoryl hóa tiếp theo của TBK1, điều này sẽ làm tăng phiên mã IFNs loại I và kích hoạt miễn dịch bẩm sinh. Kết quả là, sự ức chế ATM làm nhạy cảm tế bào ung thư với ICI. 144
Chất ức chế CHK1 hoặc chất ức chế PARP gây ra phiên mã CXCL10 phụ thuộc STING từ các dòng tế bào ung thư phổi tế bào nhỏ in vitro . Vì CXCL10 là một chemokine quan trọng để tuyển dụng các tế bào miễn dịch, việc tăng sản xuất của nó sẽ làm nhạy cảm các tế bào ung thư với điều trị ICI. Thật vậy, trong mô hình chuột ung thư phổi tế bào nhỏ, sự ức chế PARP hoặc CHK1 làm tăng đáng kể tác dụng chống khối u của phong tỏa PD-L1 thông qua kích hoạt IRF3 qua trung gian STING, do đó gây ra sản xuất IFN loại I và kích hoạt miễn dịch bẩm sinh. 139
BRCA1 và BRCA2 là thành phần quan trọng trong việc sửa chữa tổn thương DNA thông qua tái tổ hợp tương đồng (HR). 145 Tổn thương DNA do thiếu BRCA1 gây ra có thể làm tăng giải phóng vi nhân vào tế bào chất của tế bào ung thư vú. Các vi nhân được cảm nhận bởi cGAS / STING và tạo ra CXCL10 và CXCL5, làm tăng sự thâm nhập của tế bào T CD4 + và CD8 + . Và sự biểu hiện của PD-L1 trong các tế bào khối u được điều chỉnh phụ thuộc vào sự kích hoạt STING. 146 Và sự thiếu hụt HR và ức chế PARP đã được chứng minh là tạo ra khả năng gây chết tổng hợp. Sự ức chế PARP trong mô hình chuột TNBC thiếu BRCA1, có thể tạo điều kiện cho CD8 +Sự thâm nhập tế bào T và hiệu quả chống khối u thông qua việc kích hoạt con đường cGAS / STING trong tế bào khối u do đó kích hoạt nội tiết của tế bào đuôi gai. 147 , 148 Ngoài ra, sự kết hợp giữa chất ức chế PARP1 / 2 và kháng thể kháng PD-1 đã chứng minh các hoạt động hiệp đồng kháng u ở mô hình chuột TNBC thiếu BRCA1. 147 Bên cạnh đó, ở các tế bào ung thư buồng trứng thiếu BRCA1, việc điều trị chất ức chế PARP kết hợp với chất ức chế điểm kiểm soát miễn dịch khác, kháng thể CTLA-4, có thể làm tăng quá trình tuyển dụng và kích hoạt tế bào T, sản xuất cytokine và miễn dịch tế bào T có tác dụng toàn thân / trí nhớ lâu dài cuối cùng mang lại sức mạnh tổng hợp điều trị. 149
Hơn nữa, một nghiên cứu tiết lộ rằng các khiếm khuyết trong protein sửa chữa đứt gãy sợi đôi (DSB) như phức hợp Ku70 / 80 hoặc BRCA2 dẫn đến kích hoạt ATR / CHK1 và sự gia tăng phosphoryl hóa STAT1 / STAT3 và biểu hiện IRF1 sau đó gây ra phiên mã PD-L1. 150 Bên cạnh đó, ức chế ATM và CHK1 có thể làm tăng tự nội tiết và nội tiết IFNs, làm tăng quá trình phosphoryl hóa STAT1 / STAT3 thông qua các thụ thể IFN. Và sự phosphoryl hóa STAT1 / STAT3 làm tăng biểu hiện IRF1, gây ra biểu hiện PD-L1 trên các tế bào khối u. Và sự điều chỉnh biểu hiện PD-L1 có thể cung cấp cơ sở lý thuyết cho liệu pháp kết hợp với ICI theo một cách khác. 144 , 150 , 151
Virus oncolytic (OV)
Trong những thập kỷ qua, virus gây ung thư (OV) đã được tạo ra từ cả virus DNA và virus RNA. 152 , 153 Có rất nhiều ưu điểm của OV như là tác nhân điều trị ung thư. OV tiêu diệt trực tiếp và chọn lọc các tế bào khối u thông qua quá trình chết tế bào sinh miễn dịch. Ngoài ra, các phần tử virus (như DNA và RNA) có thể liên kết với các thụ thể nucleic-acid (chẳng hạn như TLR, cGAS-STING, MDA5, RIG-I, v.v.), kích hoạt giải phóng IFN loại I và chemokine. 154 , 155 , 156Hơn nữa, sự chết của các tế bào khối u dẫn đến việc giải phóng các kháng nguyên hòa tan liên quan đến khối u, các mẫu phân tử liên quan đến mầm bệnh do vi rút (PAMP) và các mẫu phân tử liên quan đến tổn thương tế bào (DAMP). PAMP và DAMP có thể tuyển dụng và kích hoạt các APC để nhấn chìm các kháng nguyên khối u hòa tan và di chuyển đến các hạch bạch huyết trong khu vực để tạo ra phản ứng tế bào T thích ứng chính chống lại khối u. Mặt khác, nhiễm vi rút có thể gây ra sự biểu hiện của MHC lớp I và tuyển dụng các tế bào T CD8 + đặc hiệu cho khối u . 157 Hơn nữa, việc sản xuất quá nhiều interferon có thể gây ra môi trường ức chế miễn dịch thông qua việc tăng sự biểu hiện của các phân tử điểm kiểm soát, chẳng hạn như PD1, PD-L1 và CTLA-4. 155 , 158 , 159
Các thử nghiệm lâm sàng ban đầu về OV đã cho thấy tính an toàn và đáp ứng đầy hứa hẹn của nó trong nhiều loại khối u. 160 Và theo đó, nó hứa hẹn sẽ kết hợp OV với ICI để đẩy nhanh phản ứng miễn dịch chống khối u và loại bỏ các rào cản tiêu diệt khối u qua trung gian tế bào T. Thật vậy, các thí nghiệm tiền lâm sàng cho thấy OV có thể làm tăng độ nhạy của khối u với ICI thông qua việc kích hoạt hoạt động của tế bào T. 161 , 162 , 163 , 164 Cùng với các nghiên cứu tiền lâm sàng này, có nhiều thử nghiệm lâm sàng được áp dụng để điều tra sự kết hợp của liệu pháp virothelytic với ICI trong điều trị ung thư (tóm tắt trong Bảng 3 ). 164Ví dụ, một thử nghiệm lâm sàng giai đoạn Ib cho thấy liệu pháp virothelytic oncolytic có thể cải thiện hiệu quả của liệu pháp kháng PD-1 với tỷ lệ đáp ứng tổng thể cao hơn và đáp ứng hoàn toàn trong khối u ác tính di căn thông qua việc tăng cường sự xâm nhập CD8 + , biểu hiện PD-L1, cũng như Biểu thức IFN-γ. 165 Và một thử nghiệm lâm sàng Giai đoạn III đang diễn ra hiện đang được tiến hành để đánh giá tốt hơn hiệu quả của liệu pháp phối hợp này ở những bệnh nhân bị u ác tính giai đoạn IIIB-IV (NCT02263508). Do đó, liệu pháp virothelytic oncolytic cho thấy mối quan tâm hấp dẫn trong điều trị ung thư, đặc biệt là sự kết hợp của ICI.
Kết luận
Con đường cảm ứng axit nucleic đóng vai trò quan trọng trong việc kích hoạt các chức năng của tế bào T trong nhiễm trùng mầm bệnh cũng như ung thư. Nói chung, các biểu hiện cao hoặc đột biến tăng chức năng của cảm biến axit nucleic, phương pháp điều trị với phối tử mở rộng hoặc chất chủ vận của các thụ thể trong khối u hoặc cảm ứng axit nucleic có thể bắt chước nhiễm trùng mầm bệnh để kích hoạt tín hiệu cảm nhận axit nucleic. Và sự kích thích của các tín hiệu cảm nhận axit nucleic gây ra sự phiên mã của IFN loại I và các cytokine khác, những tế bào này rất quan trọng để tái cấu trúc vi môi trường khối u. Kết quả là, nhiều tế bào miễn dịch hơn sẽ được tuyển dụng và nhiều tế bào ung thư hơn được tạo ra quá trình apoptosis. Quan trọng hơn, biểu hiện PD-L1 trong tế bào ung thư tăng lên, cho thấy ICIs sẽ hiệu quả hơn. Vì vậy,5 ).
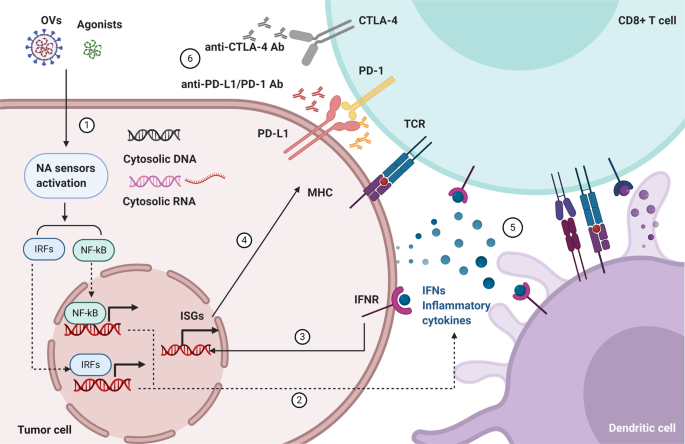
Nhắm mục tiêu miễn dịch cảm ứng axit nucleic để nhạy cảm với các chất ức chế điểm kiểm soát miễn dịch (ICI) trong liệu pháp điều trị ung thư. Mô hình hoạt động của việc nhắm mục tiêu miễn dịch cảm ứng axit nucleic để nhạy cảm ICI trong điều trị ung thư. 1. Sự cảm ứng của DNA tế bào chất, RNA, các chất chủ vận của cảm biến axit nucleic, và vi rút oncolytic (OV) có thể kích thích cảm biến axit nucleic. 2. Cảm biến được kích hoạt làm trung gian sản xuất và tiết IFN và cytokine trong tế bào khối u và DC. 3. IFN loại I được tiết ra sẽ hoạt động trên các tế bào sản xuất và lân cận thông qua IFNR. 4. IFN loại I gây ra sự biểu hiện của PD-L1 và MHC-I trong tế bào ung thư. 5. Việc sản xuất IFN có thể thúc đẩy sự trưởng thành của các DC để cải thiện khả năng bắt mồi chéo với các tế bào T và kích hoạt các tế bào NK để tiêu diệt các tế bào khối u mục tiêu. 6.
Tuy nhiên, khi xem xét sự kết hợp của các chất chủ vận cảm biến, biểu hiện và mức độ liên quan của các cảm biến có thể khác nhau trong các bệnh ung thư khác nhau. Ví dụ, biểu hiện cao của RIG-I trong ung thư buồng trứng có tương quan với mức độ khối u cao hơn và kết quả kém, cũng như sự biểu hiện cao hơn của PD-L1 và yếu tố phiên mã đặc hiệu tế bào T điều hòa FoxP3. 166 Ngược lại, biểu hiện thấp của RIG-I ở bệnh nhân ung thư biểu mô tế bào gan có tương quan thuận với thời gian sống thêm ngắn. 167 Vì vậy, biểu hiện và mức độ liên quan của các cảm biến trong các loại khối u khác nhau nên được xem xét khi kết hợp các chất chủ vận cảm biến này với ICI.
Bằng chứng nổi bật cho thấy các thụ thể axit nucleic cảm nhận được RNA hoặc DNA tế bào chất được tạo ra bởi hóa trị, xạ trị hoặc tổn thương DNA. Ví dụ, AIM2 có thể cảm nhận được tổn thương DNA do bức xạ ion hóa gây ra trong nhân, để kích hoạt quá trình chết tế bào qua trung gian caspase-1 trong tế bào biểu mô ruột và tế bào tủy xương. 168 Tuy nhiên, sự thiếu hụt AIM2 có thể làm tăng quá trình phosphoryl hóa AKT tại Ser473 để làm tăng sự phát triển của tế bào ung thư ruột kết của chuột không phụ thuộc vào quá trình viêm qua trung gian AIM2. 169 cGAS có thể nhận ra DNA tế bào chất hoặc vi nhân được tạo ra bởi hóa trị, xạ trị hoặc tổn thương DNA để kích hoạt miễn dịch bẩm sinh. 136 , 137Tuy nhiên, tổn thương DNA có thể gây ra sự chuyển vị hạt nhân của cGAS, có thể cảm nhận được sự đứt gãy sợi kép DNA và thu nhận PARP1 để ức chế sự tái tổ hợp tương đồng DNA (HR) và thúc đẩy sự hình thành khối u ở một số loại ung thư. 170 tín hiệu TLR3 cũng có thể tham gia vào các phản ứng tiền viêm góp phần tạo ra khối u. 171 Tổng hợp lại, khi xem xét các chiến lược kích hoạt khả năng miễn dịch qua trung gian axit nucleic đối với các ICI nhạy cảm, các nhà nghiên cứu nên lưu ý rằng các con đường tín hiệu khác có thể dẫn đến tác dụng chống khối u hoặc chống khối u cần phải được xem xét cẩn thận. Điều thú vị là sự ức chế ATR làm mất ổn định PD-L1, có thể khiến các tế bào khối u nhạy cảm với việc giết chết qua trung gian tế bào T. 172 Do đó, ảnh hưởng của sự kết hợp giữa ức chế ATR và ICI trong liệu pháp miễn dịch ung thư cần được nghiên cứu thêm.
Tuy nhiên, việc giải phóng khả năng miễn dịch bẩm sinh qua trung gian cảm nhận axit nucleic sẽ thúc đẩy các máy gia tốc của tế bào T và ICI giải phóng nhiều hệ thống phanh trên tế bào T. Theo đó, nó hứa hẹn sẽ kết hợp khai thác phản ứng miễn dịch qua trung gian axit nucleic với ICI trong liệu pháp miễn dịch ung thư. Tuy nhiên, các nghiên cứu sâu hơn nên chú ý nhiều hơn đến sự cân bằng nội môi của môi trường vi mô miễn dịch của khối u, và các nghiên cứu dịch chuyển lâm sàng mới nổi vẫn cần thiết cho chiến lược tổng hợp này.
Người giới thiệu
- 1.Coley, WB Điều trị sarcoma không thể phẫu thuật bằng độc tố vi khuẩn (độc tố hỗn hợp của Streptococcus erysipelas và Bacillus prodigiosus ). Proc. R. Soc. Med. 3 , 1–48 (1910).
CAS PubMed PubMed Central Google Scholar
- 2.Pardoll, DM Việc phong tỏa các trạm kiểm soát miễn dịch trong liệu pháp miễn dịch ung thư. Nat. Rev. Cancer 12 , 252–264 (2012).
CAS PubMed PubMed Central Bài báo Google Scholar
- 3.Topalian, SL và cộng sự. Khả năng sống sót, sự thuyên giảm khối u lâu dài và an toàn lâu dài ở những bệnh nhân bị u ác tính giai đoạn nặng được điều trị bằng nivolumab. J. Clin. Oncol. 32 , 1020–1030 (2014).
CAS PubMed PubMed Central Bài báo Google Scholar
- 4.Garon, EB và cộng sự. Pembrolizumab để điều trị ung thư phổi không tế bào nhỏ. N. Engl. J. Med. 372 , 2018–2028 (2015).
PubMed Bài báo PubMed Central Google Scholar
- 5.Inarrairaegui, M., Melero, I. & Sangro, B. Liệu pháp miễn dịch ung thư biểu mô tế bào gan: sự thật và hy vọng. Clin. Ung thư Res. 24 , 1518–1524 (2018).
CAS PubMed Bài báo PubMed Central Google Scholar
- 6.Muro, K. và cộng sự. Pembrolizumab cho bệnh nhân ung thư dạ dày tiến triển dương tính với PD-L1 (KEYNOTE-012): một thử nghiệm đa trung tâm, nhãn mở, giai đoạn 1b. Lancet Oncol. 17 , 717–726 (2016).
CAS PubMed Bài báo PubMed Central Google Scholar
- 7.Motzer, RJ và cộng sự. Nivolumab so với everolimus trong ung thư biểu mô tế bào thận tiến triển. N. Engl. J. Med 373 , 1803–1813 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- số 8.Ott, PA, Hodi, FS, Kaufman, HL, Wigginton, JM & Wolchok, JD Liệu pháp miễn dịch kết hợp: một bản đồ đường đi. J. Miễn dịch. Ung thư 5 , 16 (2017).
PubMed PubMed Central Bài báo Google Scholar
- 9.Nowicki, TS, Hu-Lieskovan, S. & Ribas, A. Cơ chế kháng PD-1 và phong tỏa PD-L1. Cancer J. 24 , 47–53 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 10.Demaria, O. và cộng sự. Khai thác khả năng miễn dịch bẩm sinh trong điều trị ung thư. Nature 574 , 45–56 (2019).
CAS PubMed Bài báo Google Scholar
- 11.Spranger, S., Dai, D., Horton, B. & Gajewski, TF Tế bào đuôi gai Batf3 cư trú trong khối u được yêu cầu để buôn bán tế bào T tác động và liệu pháp tế bào T được áp dụng. Tế bào ung thư 31 , 711–723 e714 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 12.Barry, KC và cộng sự. Trục tế bào đuôi gai tự nhiên xác định môi trường khối u đáp ứng với liệu pháp điểm kiểm tra. Nat. Med. 24 , 1178–1191 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 13.Takeuchi, O. & Akira, S. Các thụ thể nhận dạng mẫu và viêm. Tế bào 140 , 805-820 (2010).
CAS PubMed Bài báo Google Scholar
- 14.McNab, F., Mayer-Barber, K., Sher, A., Wack, A. & O’Garra, A. Interferon loại I trong bệnh truyền nhiễm. Nat. Rev. Immunol. 15 , 87–103 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- 15.Zitvogel, L., Galluzzi, L., Kepp, O., Smyth, MJ & Kroemer, G. Interferon loại I trong miễn dịch chống ung thư. Nat. Rev. Immunol. 15 , 405–414 (2015).
CAS PubMed Bài báo Google Scholar
- 16.Kato, H., Takahasi, K. & Fujita, T. Các thụ thể giống RIG-I: cảm biến tế bào chất cho RNA không tự. Immunol. Rev. 243 , 91–98 (2011).
PubMed Bài báo Google Scholar
- 17.Reikine, S., Nguyen, JB & Modis, Y. Cơ chế nhận dạng và báo hiệu mẫu của RIG-I và MDA5. Trước mặt. Immunol. 5 , 342 (2014).
PubMed PubMed Central Bài báo CAS Google Scholar
- 18.Yoneyama, M. và cộng sự. RNA helicase RIG-I có một chức năng thiết yếu trong các phản ứng kháng vi rút bẩm sinh do RNA sợi đôi tạo ra. Nat. Immunol. 5 , 730–737 (2004).
CAS PubMed Bài báo Google Scholar
- 19.Hornung, V. và cộng sự. RNA 5′-triphosphate là phối tử cho RIG-I. Khoa học 314 , 994–997 (2006).
PubMed Bài báo Google Scholar
- 20.Peisley, A. và cộng sự. Hợp tác lắp ráp và tháo rời động các sợi MDA5 để nhận dạng dsRNA của virus. Proc. Natl Acad. Khoa học. Hoa Kỳ 108 , 21010–21015 (2011).
CAS PubMed Bài báo Google Scholar
- 21.Jo, MH và cộng sự. Cơ chế động học để phân biệt độ dài DSRNA của virus bằng các sợi MDA5. Lý sinh. J. 104 , 420a – 420a (2013).
Google Scholar
- 22.Liu, S. và cộng sự. MAVS tuyển dụng nhiều ligase ubiquitin E3 để kích hoạt các tầng tín hiệu kháng virus. Elife 2 , e00785 (2013).
PubMed PubMed Central Bài báo Google Scholar
- 23.Venkataraman, T. và cộng sự. Mất hộp DExD / H RNA helicase LGP2 biểu hiện các phản ứng kháng virus khác nhau. J. Immunol. 178 , 6444–6455 (2007).
CAS PubMed Bài báo Google Scholar
- 24.Yoneyama, M. và cộng sự. Các chức năng được chia sẻ và duy nhất của hộp DExD / H-box xoắn RIG-I, MDA5 và LGP2 trong khả năng miễn dịch bẩm sinh kháng vi rút. J. Immunol. 175 , 2851–2858 (2005).
CAS PubMed Bài báo Google Scholar
- 25.Saito, T. và cộng sự. Quy định phòng thủ chống vi-rút bẩm sinh thông qua miền ức chế được chia sẻ trong RIG-I và LGP2. Proc. Natl Acad. Khoa học. Hoa Kỳ 104 , 582–587 (2007).
CAS PubMed Bài báo Google Scholar
- 26.Bruns, AM và cộng sự. Sự thủy phân ATP giúp tăng cường khả năng nhận biết RNA và truyền tín hiệu kháng virus bằng cảm biến miễn dịch bẩm sinh, phòng thí nghiệm di truyền và sinh lý học 2 (LGP2). J. Biol. Chèm. 288 , 938–946 (2013).
CAS PubMed Bài báo Google Scholar
- 27.Parisien, JP và cộng sự. Cảm biến RNA LGP2 ức chế TRAF ubiquitin ligase để điều chỉnh tiêu cực tín hiệu miễn dịch bẩm sinh. Đại diện EMBO 19 , https://doi.org/10.15252/embr.201745176 (2018).
- 28.Wu, YB, Wu, XQ, Wu, LH, Wang, XC & Liu, ZP Chức năng chống ung thư của các thụ thể giống RIG-I, RIG-I và MDA5, và các ứng dụng của chúng trong điều trị ung thư. Bản dịch. Res. 190 , 51–60 (2017).
CAS PubMed Bài báo Google Scholar
- 29.Kumar, S. và cộng sự. IPS-1 gây ra một cách khác biệt TRAIL, BCL2, BIRC3 và PRKCE trong hoạt động chống ung thư phụ thuộc và phụ thuộc vào interferon loại I. Cell Death Dis. 6 , e1758 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- 30.Duewell, P. và cộng sự. Các vi khuẩn Helicase giống RIG-I gây ra sự chết tế bào sinh miễn dịch của các tế bào ung thư tuyến tụy và làm cho các khối u nhạy cảm với hướng tiêu diệt bởi các tế bào T CD8 (+) . Cell Death Differ. 21 , 1984–1984 (2014).
Google Scholar
- 31.Ellermeier, J. và cộng sự. Hiệu quả điều trị của siRNA chức năng kết hợp TGF-beta1 im lặng với kích hoạt RIG-I trong ung thư tuyến tụy. Ung thư Res. 73 , 1709–1720 (2013).
CAS PubMed Bài báo Google Scholar
- 32.Kubler, K. và cộng sự. Sự kích hoạt có mục tiêu của RNA helicase retinoic gen-I cảm ứng axit gây ra quá trình apoptosis proimmunogenic của các tế bào ung thư buồng trứng ở người. Ung thư Res. 70 , 5293–5304 (2010).
PubMed Bài báo CAS Google Scholar
- 33.Glas, M. và cộng sự. Nhắm mục tiêu các thụ thể miễn dịch bẩm sinh tế bào RIG-I và MDA5 chống lại sự không đồng nhất của tế bào ung thư trong u nguyên bào thần kinh đệm một cách hiệu quả. Tế bào gốc 31 , 1064–1074 (2013).
CAS PubMed Bài báo Google Scholar
- 34.Rintahaka, J., Wiik, D., Kovanen, PE, Alenius, H. & Matikainen, S. Con đường nhận biết RNA kháng vi rút Cytosolic kích hoạt caspases 1 và 3. J. Immunol. 180 , 1749–1757 (2008).
CAS PubMed Bài báo Google Scholar
- 35.Poeck, H. và cộng sự. Sự nhận biết virus RNA bằng RIG-I dẫn đến việc kích hoạt CARD9 và tín hiệu viêm nhiễm để tạo ra interleukin 1 beta. Nat. Immunol. 11 , 63–69 (2010).
CAS PubMed Bài báo Google Scholar
- 36.Aderem, A. & Ulevitch, RJ Các thụ thể giống như Toll trong việc cảm ứng phản ứng miễn dịch bẩm sinh. Nature 406 , 782–787 (2000).
CAS PubMed Bài báo Google Scholar
- 37.Akira, S., Takeda, K. & Kaisho, T. Các thụ thể giống như Toll: các protein quan trọng liên kết khả năng miễn dịch bẩm sinh và có được. Nat. Immunol. 2 , 675–680 (2001).
CAS PubMed Bài báo Google Scholar
- 38Werling, D., Jann, OC, Offord, V., Glass, EJ & Coffey, TJ Các vấn đề về biến thể: cấu trúc TLR và nhận dạng mầm bệnh cụ thể theo loài. Xu hướng Immunol. 30 , 124–130 (2009).
CAS PubMed Bài báo PubMed Central Google Scholar
- 39.Matsumoto, M., Kikkawa, S., Kohase, M., Miyake, K. & Seya, T. Thành lập kháng thể đơn dòng chống lại thụ thể giống Toll 3 ở người ngăn chặn tín hiệu qua trung gian RNA sợi đôi. Hóa sinh. Lý sinh. Res. Công ty 293 , 1364–1369 (2002).
CAS Bài báo Google Scholar
- 40.Alexopoulou, L., Holt, AC, Medzhitov, R. & Flavell, RA Nhận biết RNA sợi đôi và kích hoạt NF-kappaB bởi thụ thể giống Toll 3. Nature 413 , 732–738 (2001).
CAS PubMed Bài báo PubMed Central Google Scholar
- 41.Tatematsu, M., Nishikawa, F., Seya, T. & Matsumoto, M. Thụ thể giống Toll 3 nhận biết cấu trúc thân không hoàn chỉnh trong RNA virus sợi đơn. Nat. Commun. 4 , 1833 (2013).
PubMed Bài báo CAS PubMed Central Google Scholar
- 42.Oshiumi, H., Matsumoto, M., Funami, K., Akazawa, T. & Seya, T. TICAM-1, một phân tử tiếp hợp tham gia vào quá trình cảm ứng interferon-beta qua trung gian 3 thụ thể Toll. Nat. Immunol. 4 , 161–167 (2003).
CAS PubMed Bài báo PubMed Central Google Scholar
- 43.Diebold, SS, Kaisho, T., Hemmi, H., Akira, S. & Sousa, CRE Đáp ứng kháng vi-rút bẩm sinh bằng cách nhận biết RNA sợi đơn qua trung gian TLR7. Khoa học 303 , 1529–1531 (2004).
CAS PubMed Bài báo PubMed Central Google Scholar
- 44.Heil, F. et al. Nhận dạng đặc trưng của loài đối với RNA sợi đơn thông qua thụ thể giống số 7 và 8. Science 303 , 1526–1529 (2004).
CAS PubMed Bài báo Google Scholar
- 45.Hornung, V. và cộng sự. Cảm ứng mạnh mẽ theo trình tự của IFN-alpha bằng RNA can thiệp ngắn trong tế bào đuôi gai plasmacytoid thông qua TLR7. Nat. Med. 11 , 263–270 (2005).
CAS PubMed Bài báo Google Scholar
- 46.Lehmann, SM và cộng sự. Một vai trò khác thường đối với miRNA: let-7 kích hoạt thụ thể Toll-like 7 và gây ra sự thoái hóa thần kinh. Nat. Tế bào thần kinh. 15 , 827 – U844 (2012).
CAS PubMed Bài báo Google Scholar
- 47.Savarese. Phức hợp miễn dịch ribonucleoprotein hạt nhân nhỏ U1 tạo ra interferon loại I trong tế bào đuôi gai plasmacytoid thông qua TLR7. Máu 107 , 3831–3831 (2006).
CAS Bài báo Google Scholar
- 48.Zhang, ZK và cộng sự. Phân tích cấu trúc cho thấy rằng thụ thể giống số 7 là một thụ thể kép dành cho guanosine và RNA sợi đơn. Miễn dịch 45 , 737–748 (2016).
CAS PubMed Bài báo Google Scholar
- 49.Tanji, H. và cộng sự. Thụ thể giống Toll 8 cảm nhận các sản phẩm thoái hóa của RNA sợi đơn. Nat. Kết cấu. Mol Biol. 22 , 109–115 (2015).
CAS PubMed Bài báo Google Scholar
- 50.Singh, M. và cộng sự. Miễn dịch kháng biểu mô bẩm sinh và thích ứng hiệu quả thông qua kích hoạt TLR7 / 8 tại chỗ. J. Immunol. 193 , 4722–4731 (2014).
CAS PubMed PubMed Central Bài báo Google Scholar
- 51.Ohto, U. và cộng sự. Cơ sở cấu trúc của CpG và sự nhận biết DNA ức chế bởi thụ thể Toll-like 9. Nature 520 , 702 – U303 (2015).
CAS PubMed Bài báo PubMed Central Google Scholar
- 52.Chan, MP và cộng sự. Quá trình phân hủy DNA phụ thuộc DNase II là cần thiết để TLR9 cảm nhận DNA. Nat. Commun. 6 , https://doi.org/10.1038/ncomms6853 (2015).
- 53.Gowda, NM, Wu, XZ & Gowda, DC TLR9 và MyD88 rất quan trọng đối với sự phát triển của miễn dịch bảo vệ đối với bệnh sốt rét. J. Immunol. 188 , 5073–5085 (2012).
CAS PubMed PubMed Central Bài báo Google Scholar
- 54.Sun, LJ, Wu, JX, Du, FH, Chen, X. & Chen, ZJJ Cyclic GMP-AMP synthase là một cảm biến DNA tế bào kích hoạt con đường interferon loại I. Science 339 , 786–791 (2013).
CAS PubMed Bài báo PubMed Central Google Scholar
- 55.Wu, JX và cộng sự. GMP-AMP chu kỳ là một chất truyền tin thứ hai nội sinh trong quá trình truyền tín hiệu miễn dịch bẩm sinh bằng DNA tế bào. Khoa học 339 , 826–830 (2013).
CAS PubMed Bài báo PubMed Central Google Scholar
- 56.Motwani, M., Pesiridis, S. & Fitzgerald, KA cảm nhận DNA bằng con đường cGAS-STING trong sức khỏe và bệnh tật. Nat. Rev. Genet. 20 , 657–674 (2019).
CAS PubMed PubMed Central Bài báo Google Scholar
- 57.Luecke, S. và cộng sự. cGAS được kích hoạt bởi DNA theo cách phụ thuộc vào độ dài. EMBO Rep. 18 , 1707–1715 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 58.Lee, C. và cộng sự. Inflammasome như một mục tiêu điều trị đầy hứa hẹn cho bệnh ung thư. Khoa học đời sống. 231 , https://doi.org/10.1016/j.lfs.2019.116593 (2019).
- 59.Broz, P. & Dixit, VM Inflammasomes: cơ chế lắp ráp, điều hòa và truyền tín hiệu. Nat. Rev. Immunol. 16 , 407–420 (2016).
CAS PubMed Bài báo PubMed Central Google Scholar
- 60.Takeda, K. và cộng sự. Hoạt động tế bào NK bị khiếm khuyết và phản ứng Th1 ở chuột thiếu IL-18. Miễn dịch 8 , 383–390 (1998).
CAS PubMed Bài báo PubMed Central Google Scholar
- 61.Wong, JL, Berk, E., Edwards, RP & Kalinski, P. Tế bào NK có mồi IL-18 cộng tác với các tế bào đuôi gai để thúc đẩy việc tuyển dụng các tế bào T CD8 + tác động vào môi trường vi mô khối u. Ung thư Res. 73 , 4653–4662 (2013).
CAS PubMed PubMed Central Bài báo Google Scholar
- 62.Zielinski, CE và cộng sự. Tế bào TH17 của người do mầm bệnh tạo ra IFN-gamma hoặc IL-10 và được điều chỉnh bởi IL-1beta. Nature 484 , 514–518 (2012).
CAS PubMed Bài báo PubMed Central Google Scholar
- 63.Pang, IK, Ichinohe, T. & Iwasaki, A. Tín hiệu IL-1R trong tế bào đuôi gai thay thế các thụ thể nhận dạng mẫu trong việc thúc đẩy phản ứng của tế bào T CD8 (+) đối với vi rút cúm A. Nat. Immunol. 14 , 246–253 (2013).
CAS PubMed PubMed Central Bài báo Google Scholar
- 64.Chan, YK & Gack, MU Lẩn tránh vi-rút cảm nhận DNA và RNA nội bào. Nat. Rev. Microbiol. 14 , 360–373 (2016).
CAS PubMed PubMed Central Bài báo Google Scholar
- 65.Wang, B. & Yin, Q. Kích hoạt và điều tiết vi khuẩn AIM2: quan điểm cấu trúc. J. Kết cấu. Biol. 200 , 279–282 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 66.Unterholzner, L. và cộng sự. IFI16 là một cảm biến miễn dịch bẩm sinh cho DNA nội bào. Nat. Immunol. 11 , 997 – U942 (2010).
CAS PubMed PubMed Central Bài báo Google Scholar
- 67.Ansari, MA và cộng sự. Sự nhận biết bộ gen của Herpesvirus gây ra sự acetyl hóa IFI16 của hạt nhân là điều cần thiết cho sự chuyển vị tế bào chất, phản ứng viêm nhiễm và IFN-beta của nó. PLoS Pathog. 11 , https://doi.org/10.1371/journal.ppat.1005019 (2015).
- 68.Dunphy, G. và cộng sự. Kích hoạt không chuẩn của bộ điều hợp cảm biến DNA STING bằng ATM và IFI16 làm trung gian truyền tín hiệu NF-kappaB sau khi DNA hạt nhân bị hư hại. Mol Tế bào 71 , 745-760. e745 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 69.Kerur, N. và cộng sự. IFI16 hoạt động như một cảm biến mầm bệnh hạt nhân để gây ra bệnh viêm để phản ứng với nhiễm herpesvirus liên quan đến sarcoma Kaposi. Vi sinh vật chủ tế bào 9 , 363–375 (2011).
CAS PubMed PubMed Central Bài báo Google Scholar
- 70.Li, D. và cộng sự. Sự suy giảm IFI16 qua trung gian STING kiểm soát tiêu cực việc sản xuất interferon loại I. Đại diện ô 29 , 1249–1260 e1244 (2019).
CAS PubMed Bài báo PubMed Central Google Scholar
- 71.Yan, S. và cộng sự. Sự thiếu hụt tín hiệu AIM2-ASC phát hiện ra phản ứng quá kích do STING điều khiển của IFN loại I và sự suy giảm tương hỗ của miễn dịch IFN-gamma bảo vệ trong nhiễm trùng mycobacteria. J. Immunol. 200 , 1016–1026 (2018).
CAS PubMed Bài báo PubMed Central Google Scholar
- 72.Takaoka, A. và cộng sự. DAI (DLM-1 / ZBP1) là một cảm biến DNA tế bào và một chất kích hoạt phản ứng miễn dịch bẩm sinh. Nature 448 , 501 – U514 (2007).
CAS PubMed Bài báo PubMed Central Google Scholar
- 73.Maelfait, J. và cộng sự. Việc cảm nhận virus và RNA nội sinh của ZBP1 / DAI gây ra hiện tượng hoại tử. Embo J. 36 , 2529–2543 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 74.Yang, P. và cộng sự. Cảm biến axit nucleic trong tế bào LRRFIP1 làm trung gian sản xuất interferon loại I thông qua con đường phụ thuộc beta-catenin. Nat. Immunol. 11 , 487–494 (2010).
CAS PubMed Bài báo PubMed Central Google Scholar
- 75.Jiang, Y., Zhu, YP, Liu, ZJ & Ouyang, SY Các vai trò mới nổi của protein DDX41 trong khả năng miễn dịch và bệnh tật. Tế bào Protein 8 , 83–89 (2017).
CAS PubMed Bài báo PubMed Central Google Scholar
- 76.Meurs, EF và cộng sự. Sự biểu hiện thành phần của p68 kinase chuỗi kép được kích hoạt bằng RNA ở người trong tế bào chó làm trung gian cho quá trình phosphoryl hóa yếu tố khởi đầu 2 của sinh vật nhân chuẩn và khả năng chống lại một phần sự phát triển của virus viêm cơ tim. J. Virol. 66 , 5805–5814 (1992).
CAS PubMed PubMed Central Bài báo Google Scholar
- 77.Kumar, A. và cộng sự. Thiếu tín hiệu cytokine trong nguyên bào sợi của phôi chuột bị xóa mục tiêu trong gen PKR: vai trò của IRF-1 và NF-kappaB. EMBO J. 16 , 406–416 (1997).
CAS PubMed PubMed Central Bài báo Google Scholar
- 78.Chen, NH và cộng sự. Cảm biến RNA của hệ thống miễn dịch bẩm sinh và khả năng phát hiện mầm bệnh của chúng. Iubmb Life 69 , 297–304 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 79.Li, X. và cộng sự. Liên kết DNA của virus với NLRC3, một cảm biến axit nucleic ức chế, giải phóng STING, một thụ thể dinucleotide chu kỳ kích hoạt interferon loại I. Miễn dịch 50 , 591–599. e596 (2019).
CAS PubMed PubMed Central Bài báo Google Scholar
- 80.Elion, DL và cộng sự. Chất chủ vận RIG-I có hoạt tính điều trị gây ra tiêu diệt tế bào khối u gây miễn dịch trong ung thư vú. Ung thư Res. 78 , 6183–6195 (2018).
CAS PubMed Bài báo Google Scholar
- 81.Poeck, H. và cộng sự. 5′-Triphosphate-siRNA: biến gen im lặng và kích hoạt Rig-I chống lại khối u ác tính. Nat. Med. 14 , 1256–1263 (2008).
CAS PubMed Bài báo Google Scholar
- 82.Ruzicka, M. và cộng sự. Liệu pháp miễn dịch dựa trên RIG-I giúp tăng cường khả năng sống sót trong các mô hình AML tiền lâm sàng và làm nhạy cảm các tế bào AML để phong tỏa điểm kiểm soát. Bệnh bạch cầu 34 , 1017–1026 (2020).
CAS PubMed Bài báo Google Scholar
- 83.Jacobson, ME, Wang-Bishop, L., Becker, KW & Wilson, JT Cung cấp RNA 5′-triphosphate với các hạt nano nội phân tử kích hoạt mạnh RIG-I để cải thiện liệu pháp miễn dịch ung thư. Máy bơm sinh học. Khoa học. 7 , 547–559 (2019).
CAS PubMed Bài báo PubMed Central Google Scholar
- 84.Heidegger, S. và cộng sự. RIG-I kích hoạt RNA kích thích miễn dịch làm tăng hiệu quả của vắc-xin chống ung thư và hiệp đồng với phong tỏa điểm kiểm soát miễn dịch. EBioMedicine 41 , 146–155 (2019).
PubMed PubMed Central Bài báo Google Scholar
- 85.Heidegger, S. và cộng sự. Kích hoạt RIG-I rất quan trọng đối với khả năng đáp ứng đối với việc phong tỏa trạm kiểm soát. Khoa học. Immunol . 4 , 1–17 (2019).
Bài báo CAS Google Scholar
- 86.Duewell, P. và cộng sự. Các vi khuẩn Helicase giống RIG-I gây ra sự chết tế bào sinh miễn dịch của các tế bào ung thư tuyến tụy và làm cho các khối u nhạy cảm với hướng tiêu diệt bởi các tế bào T CD8 (+). Cell Death Differ. 21 , 1825–1837 (2014).
CAS PubMed PubMed Central Bài báo Google Scholar
- 87.Chi, H. và cộng sự. Hoạt động chống khối u của chất chủ vận thụ thể giống số 7. Trước mặt. Dược phẩm. 8 , 304 (2017).
Bài báo CAS Google Scholar
- 88.He, LZ, Weidlick, J., Sisson, C., Marsh, HC & Keler, T. Các chất chủ vận thụ thể giống Toll định hình các phản ứng miễn dịch đối với vắc xin ung thư nhắm mục tiêu vào thụ thể mannose. Ô. Mol Immunol. 12 , 719–728 (2015).
CAS PubMed Bài báo PubMed Central Google Scholar
- 89.Aznar, MA và cộng sự. Tác dụng điều trị miễn dịch của poly I: C được nano hóa trong khoang miệng. J. Miễn dịch. Cự Giải 7 , 116 (2019).
PubMed PubMed Central Bài báo Google Scholar
- 90.Takeda, Y. và cộng sự. Chất bổ trợ đặc hiệu TLR3 làm giảm khả năng kháng thuốc phong tỏa PD-L1 bẩm sinh mà không có độc tính cytokine trong liệu pháp miễn dịch vắc xin khối u. Đại diện Ô 19 , 1874–1887 (2017).
CAS PubMed Bài báo Google Scholar
- 91.Sabbatini, P. và cộng sự. Thử nghiệm giai đoạn I về các peptide dài chồng chéo lên nhau từ kháng nguyên tự thân của khối u và poly-ICLC cho thấy sự cảm ứng nhanh chóng của phản ứng miễn dịch tích hợp ở bệnh nhân ung thư buồng trứng. Clin. Ung thư Res. 18 , 6497–6508 (2012).
CAS PubMed Bài báo Google Scholar
- 92.Tsuji, T. và cộng sự. Tác dụng của Montanide và tá dược poly-ICLC lên tế bào T CD4 + đặc hiệu với kháng nguyên khối u ở người trong giai đoạn I thử nghiệm vắc xin peptide dài chồng chéo lên nhau. Immunol ung thư. Res. 1 , 340–350 (2013).
CAS PubMed Bài báo Google Scholar
- 93.Zhu, X. và cộng sự. Toll like receptor-3 ligand poly-ICLC thúc đẩy hiệu quả của việc tiêm chủng ngoại vi với các biểu mô peptide có nguồn gốc từ kháng nguyên khối u trong các mô hình khối u thần kinh trung ương ở chuột. J. Dịch. Med. 5 , 10 (2007).
PubMed PubMed Central Bài báo CAS Google Scholar
- 94.Pavlick, A. và cộng sự. Tiêm vắc xin kết hợp với NY-ESO-1 protein, poly-ICLC và montanide giúp cải thiện các phản ứng miễn dịch dịch thể và tế bào ở những bệnh nhân bị u ác tính nguy cơ cao. Immunol ung thư. Res. 8 , 70–80 (2020).
CAS PubMed Bài báo Google Scholar
- 95.Hanna, E., Abadi, R. & Abbas, O. Imiquimod trong da liễu: tổng quan. Int J. Dermatol. 55 , 831–844 (2016).
CAS PubMed Bài báo Google Scholar
- 96.Zhang, L. và cộng sự. Dạng tấm nano quang học miễn dịch độc đáo chống lại ung thư miệng xenograft chỉnh hình và ung thư vú tổng hợp di căn. Nano Lett. 18 , 7092–7103 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 97.Joseph, RW và cộng sự. Điều trị khối u ác tính chuyển tiếp và di căn ở hai bệnh nhân được điều trị bằng ipilimumab và imiquimod tại chỗ. Ung thư hắc tố Res. 26 , 409–412 (2016).
PubMed Bài báo Google Scholar
- 98.Fujimura, T. và cộng sự. Điều trị thành công khối u đa u ác tính chuyển tiếp kháng nivolumab với ipilimumab và imiquimod tại chỗ. Đại diện Vụ án Oncol. 11 , 1–5 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 99.Nishii, N. và cộng sự. Sử dụng toàn thân chất chủ vận TLR7 làm suy giảm tế bào T điều hòa bằng cách biến đổi tế bào đuôi gai và khắc phục tình trạng kháng trị liệu phong tỏa PD-L1. Eur. J. Immunol. 48 , 71–72 (2018).
Google Scholar
- 100.Sabado, RL và cộng sự. Resiquimod như một chất bổ trợ miễn dịch cho việc chủng ngừa protein NY-ESO-1 ở những bệnh nhân bị u ác tính nguy cơ cao. Immunol ung thư. Res. 3 , 278–287 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- 101.Block, MS và cộng sự. Một thử nghiệm lâm sàng thí điểm thử nghiệm resiquimod tại chỗ và một xenopeptide làm chất bổ trợ miễn dịch cho vắc-xin ung thư hắc tố nhắm mục tiêu MART-1. Ung thư hắc tố Res. 29 , 420–427 (2019).
CAS PubMed Bài báo Google Scholar
- 102.Rodell, CB và cộng sự. Các hạt nano được nạp chất chủ vận TLR7 / 8 thúc đẩy sự phân cực của các đại thực bào liên quan đến khối u để tăng cường liệu pháp miễn dịch ung thư. Nat. Sinh học. Anh 2 , 578 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 103.Lu, HL và cộng sự. VTX-2337 là một chất chủ vận TLR8 mới kích hoạt các tế bào NK và tăng cường ADCC. Clin. Ung thư Res. 18 , 499–509 (2012).
CAS PubMed Bài báo Google Scholar
- 104.Stephenson, RM và cộng sự. Kích thích TLR8 giúp tăng cường ly giải tế bào tiêu diệt tự nhiên qua trung gian cetuximab đối với tế bào ung thư đầu và cổ và bắt mồi chéo tế bào đuôi gai của tế bào T CD8 + đặc hiệu EGFR. Immunol ung thư. Miễn dịch khác. 62 , 1347–1357 (2013).
CAS PubMed PubMed Central Bài báo Google Scholar
- 105.Yu, D. và cộng sự. ‘Immunomers’-tiểu thuyết 3 ‘-3’-liên kết CpG oligodeoxyribonucleotide làm tác nhân điều hòa miễn dịch mạnh. Axit nucleic Res. 30 , 4460–4469 (2002).
CAS PubMed PubMed Central Bài báo Google Scholar
- 106.Wang, DQ, Jiang, WN, Zhu, FG, Mao, XZ & Agrawal, S. Điều chế vi môi trường khối u bằng cách sử dụng IMO-2125, một chất chủ vận TLR9 mới, trong điều trị miễn dịch ung thư. Int. J. Oncol. 53 , 1193–1203 (2018).
CAS PubMed Google Scholar
- 107.Diab, A. và cộng sự. Một thử nghiệm giai đoạn 1/2 của IMO-2125 (IMO) trong khoang miệng kết hợp với chất ức chế điểm kiểm soát (CPI) trong u hắc tố chịu lửa 1-PD- (L). Ann. Oncol. 28 (2017).
- 108.Wang, S. và cộng sự. Tiêm vào trong khoang miệng một oligonucleotide CpG sẽ phục hồi khả năng kháng thuốc phong tỏa PD-1 bằng cách mở rộng các tế bào T CD8 + đa chức năng . Proc. Natl Acad. Khoa học. Hoa Kỳ 113 , E7240 – E7249 (2016).
CAS PubMed Bài báo Google Scholar
- 109.Miller, AM và cộng sự. Intraperitoneal CMP-001: một liệu pháp miễn dịch mới để điều trị ung thư biểu mô phúc mạc của ung thư đường tiêu hóa và tuyến tụy. Ann. Phẫu thuật. Oncol. , https://doi.org/10.1245/s10434-020-08591-7 (2020).
- 110.Poh, A. Làm ấm khối u ác tính “Lạnh” bằng thuốc chủ vận TLR9. Khám phá ung thư. 8 , 670–670 (2018).
Bài báo Google Scholar
- 111.Milhem, M. và cộng sự. Chất chủ vận giống thụ thể 9 (TLR9) trong khoang miệng, CMP-001, kết hợp với pembrolizumab có thể đảo ngược khả năng kháng lại sự ức chế PD-1 trong thử nghiệm giai đoạn Ib ở những đối tượng bị u ác tính tiến triển. Ung thư Res. 78 , https://doi.org/10.1158/1538-7445.Am2018-Ct144 (2018).
- 112.Ribas, A. và cộng sự. SD-101 kết hợp với pembrolizumab trong u ác tính tiến triển: kết quả của nghiên cứu đa trung tâm pha Ib. Khám phá ung thư. 8 , 1250–1257 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 113.Corrales, L. và cộng sự. Kích hoạt trực tiếp STING trong vi môi trường khối u dẫn đến sự thoái lui và miễn dịch khối u toàn thân và mạnh mẽ. Đại diện Ô 11 , 1018–1030 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- 114.Ramanjulu, JM và cộng sự. Thiết kế chất chủ vận thụ thể amidobenzimidazole STING có hoạt tính toàn thân. Bản chất 564 , 439 (2018).
CAS PubMed Bài báo PubMed Central Google Scholar
- 115.Fu, J. và cộng sự. Vắc xin ung thư công thức chủ vận STING có thể chữa khỏi các khối u đã được hình thành kháng với phong tỏa PD-1. Khoa học. Bản dịch. Med. 7 , https://doi.org/10.1126/scitranslmed.aaa4306 (2015).
- 116.Curran, E. và cộng sự. Sự kích hoạt con đường STING kích thích khả năng miễn dịch mạnh chống lại bệnh bạch cầu cấp dòng tủy. Đại diện Ô 15 , 2357–2366 (2016).
CAS PubMed PubMed Central Bài báo Google Scholar
- 117.Glickman, LH và cộng sự. Kích hoạt trực tiếp STING trong vi môi trường khối u dẫn đến sự thoái lui và miễn dịch của khối u toàn thân và mạnh mẽ. Ung thư Res. 76 , https://doi.org/10.1158/1538-7445.Am2016-Sy39-02 (2016).
- 118.Ghaffari, A. và cộng sự. Liệu pháp chủ vận STING kết hợp với phong tỏa điểm kiểm tra miễn dịch PD-1 giúp tăng cường đáp ứng với hóa trị liệu carboplatin trong ung thư buồng trứng dạng huyết thanh cao. Br. J. Cancer 119 , 440–449 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 119.Kim, C., Kim, W., Hang, Y., Kim, J. & Chon, H. Liệu pháp miễn dịch ung thư với chất chủ vận STING và chất ức chế điểm kiểm tra miễn dịch PD-1 ngăn chặn hiệu quả ung thư biểu mô phúc mạc của ung thư ruột kết. Ann. Oncol. 30 (2019).
- 120.Dorta-Estremera, S. và cộng sự. Nhắm mục tiêu tín hiệu interferon và CTLA-4 nâng cao hiệu quả điều trị của liệu pháp miễn dịch kháng PD-1 trong mô hình tiền lâm sàng của ung thư miệng do HPV (+). J. Miễn dịch. Cự Giải 7 , 252 (2019).
PubMed PubMed Central Bài báo Google Scholar
- 121.Ager, CR và cộng sự. Kích hoạt STING trong khoang miệng với điều biến điểm kiểm tra tế bào T tạo ra khả năng miễn dịch kháng u toàn thân. Immunol ung thư. Res. 5 , 676–684 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 122.Sheng, W. và cộng sự. Cắt bỏ LSD1 kích thích miễn dịch chống khối u và cho phép phong tỏa trạm kiểm soát. Tế bào 174 , 549-563. e519 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 123.Qin, Y. và cộng sự. Sự ức chế demethylase 1 đặc hiệu của histone lysine tạo ra khả năng miễn dịch khối u vú và tăng cường hiệu quả chống khối u của phong tỏa điểm kiểm soát miễn dịch. Oncogene 38 , 390–405 (2019).
CAS PubMed Bài báo PubMed Central Google Scholar
- 124.Chiappinelli, KB và cộng sự. Ức chế sự methyl hóa DNA gây ra phản ứng interferon trong ung thư thông qua dsRNA bao gồm các retrovirus nội sinh. Tế bào 169 , 362-362 (2017).
Bài báo CAS Google Scholar
- 125.Roulois, D. và cộng sự. Các tác nhân khử methyl DNA nhắm mục tiêu vào các tế bào ung thư đại trực tràng bằng cách gây ra sự bắt chước virus bằng các bản sao nội sinh. Tế bào 162 , 961-973 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- 126.Covre, A. và cộng sự. Hoạt động chống khối u của điều hòa miễn dịch biểu sinh kết hợp với phong tỏa CTLA-4 trong các mô hình chuột đồng loại. Oncoimmunology 4 , 1–9 (2015).
Bài báo CAS Google Scholar
- 127.Oda, H. và cộng sự. Hội chứng aicardi-goutieres do đột biến IFIH1 gây ra. Là. J. Hum. Genet. 95 , 121–125 (2014).
CAS PubMed PubMed Central Bài báo Google Scholar
- 128.Van Eyck, L. và cộng sự. Đột biến IFIH1 gây ra bệnh lupus ban đỏ hệ thống với sự thiếu hụt IgA chọn lọc. Viêm khớp Rheumatol. 67 , 1592–1597 (2015).
PubMed Bài báo CAS Google Scholar
- 129.Rice, GI và cộng sự. Đột biến tăng chức năng trong IFIH1 gây ra một loạt các kiểu hình bệnh tật ở người liên quan đến tín hiệu interferon loại I được điều chỉnh. Nat. Genet. 46 , 503–509 (2014).
CAS PubMed PubMed Central Bài báo Google Scholar
- 130.Ahmad, S. và cộng sự. Vi phạm khả năng tự dung nạp RNA kép Alu làm cơ sở cho tình trạng viêm qua trung gian MDA5. Tế bào 172 , 797-810. e713 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 131.Gannon, HS và cộng sự. Xác định sự phụ thuộc adenosine deaminase ADAR1 trong một tập hợp con các tế bào ung thư. Nat. Commun. 9 , 5450 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 132.Ishizuka, JJ và cộng sự. Mất ADAR1 trong các khối u vượt qua khả năng kháng phong tỏa trạm kiểm soát miễn dịch. Bản chất 565 , 43 (2019).
CAS Bài báo Google Scholar
- 133.Thuốc ức chế Sherr, CJ & Roberts, JM CDK: chất điều hòa tích cực và tiêu cực của sự tiến triển pha G1. Genes Dev. 13 , 1501–1512 (1999).
CAS PubMed Bài báo PubMed Central Google Scholar
- 134.Goel, S. và cộng sự. Sự ức chế CDK4 / 6 kích hoạt miễn dịch chống khối u. Bản chất 548 , 471 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 135.Deng, J. và cộng sự. Sự ức chế CDK4 / 6 làm tăng khả năng miễn dịch chống khối u bằng cách tăng cường hoạt hóa tế bào T. Khám phá ung thư. 8 , 216–233 (2018).
CAS PubMed Bài báo PubMed Central Google Scholar
- 136.Harding, SM và cộng sự. Quá trình phân bào sau khi DNA bị tổn thương cho phép nhận dạng mẫu trong các vi nhân. Bản chất 548 , 466 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 137.Mackenzie, KJ và cộng sự. cGAS giám sát vi nhân liên kết sự bất ổn định của bộ gen với khả năng miễn dịch bẩm sinh. Bản chất 548 , 461 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 138.Deng, LF và cộng sự. Cảm nhận DNA tế bào phụ thuộc STING thúc đẩy khả năng miễn dịch kháng khối u phụ thuộc vào interferon loại I do bức xạ gây ra trong các khối u sinh miễn dịch. Miễn dịch 41 , 843–852 (2014).
CAS PubMed PubMed Central Bài báo Google Scholar
- 139.Sen, T. và cộng sự. Nhắm mục tiêu phản ứng tổn thương DNA thúc đẩy miễn dịch chống khối u thông qua kích hoạt tế bào T qua trung gian STING trong ung thư phổi tế bào nhỏ. Đĩa ung thư. 9 , 646–661 (2019).
CAS Bài báo Google Scholar
- 140.Ding, LY và cộng sự. Sự ức chế PARP tạo ra khả năng miễn dịch kháng khối u phụ thuộc STING trong ung thư buồng trứng do thiếu Brca1. Đại diện ô 25 , 2972 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 141.Grabosch, S. và cộng sự. Điều biến miễn dịch do cisplatin gây ra trên mô hình chuột ung thư buồng trứng với các cấu trúc viêm khác biệt. Oncogene 38 , 2380–2393 (2019).
CAS PubMed Bài báo PubMed Central Google Scholar
- 142.Dovedi, SJ và cộng sự. Xạ trị phân đoạn kích thích miễn dịch chống khối u qua trung gian của cả quần thể tế bào T đa dòng nội trú và thâm nhiễm khi kết hợp với phong tỏa PD-1. Clin. Ung thư Res. 23 , 5514–5526 (2017).
CAS PubMed Bài báo PubMed Central Google Scholar
- 143.Twyman-Saint Victor, C. et al. Bức xạ và phong tỏa điểm kiểm tra kép kích hoạt cơ chế miễn dịch không dư thừa trong bệnh ung thư. Nature 520 , 373 (2015).
CAS PubMed Bài báo PubMed Central Google Scholar
- 144.Zhang, Q. và cộng sự. Sự ức chế ATM làm tăng tín hiệu interferon và làm nhạy cảm ung thư tuyến tụy với liệu pháp phong tỏa trạm kiểm soát miễn dịch. Ung thư Res . 79 , 3940–3951 (2019).
CAS PubMed PubMed Central Bài báo Google Scholar
- 145.Jasin, M. & Rothstein, R. Sửa chữa đứt sợi bằng cách tái tổ hợp tương đồng. Lạnh mùa xuân Harb. Sự tôn trọng. Biol. 5 , a012740 (2013).
PubMed PubMed Central Bài báo CAS Google Scholar
- 146.Parkes, EE et al. Kích hoạt tín hiệu miễn dịch bẩm sinh phụ thuộc STING bằng tổn thương DNA đặc hiệu pha S trong ung thư vú. J. Natl Cancer Inst. 109 , 1–10 (2017).
Bài báo CAS Google Scholar
- 147.Wang, Z. và cộng sự. Niraparib kích hoạt tín hiệu interferon và tăng cường hiệu quả của kháng thể kháng PD-1 trong các mô hình khối u. Khoa học. Rep. 9 , 1853 (2019).
PubMed PubMed Central Bài báo CAS Google Scholar
- 148.Pantelidou, C. và cộng sự. Hiệu quả của chất ức chế PARP phụ thuộc vào sự tuyển dụng tế bào T CD8 (+) thông qua kích hoạt con đường STING trong khoang trong các mô hình ba âm tính thiếu BRCA. Đĩa đệm ung thư vú. 9 , 722–737 (2019).
Bài báo Google Scholar
- 149.Higuchi, T. và cộng sự. Phong tỏa CTLA-4 hiệp đồng điều trị với ức chế PARP trong ung thư buồng trứng thiếu BRCA1. Immunol ung thư. Res . 3 , 1257–1268 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- 150.Sato, H. và cộng sự. Con đường sửa chữa đứt gãy sợi kép DNA điều chỉnh sự biểu hiện PD-L1 trong tế bào ung thư. Nat. Commun. 8 , 1751 (2017).
PubMed PubMed Central Bài báo CAS Google Scholar
- 151.Garcia-Diaz, A. và cộng sự. Con đường tín hiệu của thụ thể interferon điều chỉnh sự biểu hiện PD-L1 và PD-L2. Đại diện Ô 19 , 1189–1201 (2017).
CAS PubMed PubMed Central Bài báo Google Scholar
- 152.Lawler, SE, Speranza, MC, Cho, CF & Chiocca, EA Vi rút gây tê trong điều trị ung thư: đánh giá. JAMA Oncol. 3 , 841–849 (2017).
PubMed Bài báo PubMed Central Google Scholar
- 153.Shi, T., Song, X., Wang, Y., Liu, F. & Wei, J. Kết hợp virus gây ung thư với liệu pháp miễn dịch ung thư: thiết lập một thế hệ điều trị ung thư mới. Trước mặt. Immunol. 11 , 683 (năm 2020).
CAS PubMed PubMed Central Bài báo Google Scholar
- 154.Lee, J., Ghonime, MG, Wang, R. & Cassady, KA Bộ máy kháng virus: STING và hạn chế virus oncolytic. Mol Họ. Oncolytics 13 , 7–13 (2019).
CAS PubMed PubMed Central Bài báo Google Scholar
- 155.Dai, P. và cộng sự. Phân phối trong khoang miệng của virus Ankara (iMVA) đã được biến đổi bất hoạt gây ra miễn dịch chống khối u toàn thân thông qua các tế bào đuôi gai phụ thuộc STING và Batf3. Khoa học. Immunol. 2 , https://doi.org/10.1126/sciimmunol.aal1713 (2017).
- 156.Kell, AM & Gale, M. Jr. RIG-I trong nhận dạng virus RNA. Virology 479-480 , 110–121 (2015).
CAS PubMed Bài báo Google Scholar
- 157.Bommareddy, PK, Shettigar, M. & Kaufman, HL Tích hợp virus gây ung thư trong liệu pháp miễn dịch điều trị ung thư kết hợp. Nat. Rev. Immunol. 18 , 498–513 (2018).
CAS PubMed Bài báo Google Scholar
- 158.Uehara, J. và cộng sự. Tiêm IFN-beta vào trong khoang miệng gây ra sản xuất chemokine trong khối u ác tính và làm tăng hiệu quả điều trị của mAb kháng PD-L1. Hóa sinh. Lý sinh. Res. Commun. 490 , 521–527 (2017).
CAS PubMed Bài báo Google Scholar
- 159.Cheng, X. và cộng sự. Con đường PD-1 / PD-L được điều chỉnh trong quá trình ức chế EAE do IL-12 gây ra qua trung gian IFN-gamma. J. Neuroimmunol. 185 , 75–86 (2007).
CAS PubMed PubMed Central Bài báo Google Scholar
- 160.Fulci, G. & Chiocca, EA Vi-rút oncolytic để điều trị khối u não và các khối u ác tính thể rắn khác: một đánh giá. Trước mặt. Biosci. 8 , e346 – e360 (2003).
CAS PubMed Bài báo Google Scholar
- 161.Zamarin, D. và cộng sự. Liệu pháp virothelytic oncolytic khu trú khắc phục sự đề kháng của khối u toàn thân đối với liệu pháp miễn dịch phong tỏa điểm kiểm soát miễn dịch. Khoa học. Bản dịch. Med. 6 , 226ra232 (2014).
Bài báo CAS Google Scholar
- 162.Bourgeois-Daigneault, MC và cộng sự. Liệu pháp virothelytic bổ trợ bổ trợ trước khi phẫu thuật làm nhạy cảm ung thư vú ba âm tính với liệu pháp kiểm tra miễn dịch. Khoa học. Bản dịch. Med . 10 , https://doi.org/10.1126/scitranslmed.aao1641 (2018).
- 163.Marchand, JB và cộng sự. Vectơ hóa trong vi rút tiêm chủng oncolytic của một kháng thể, một Fab và một scFv chống lại sự chết của tế bào theo chương trình-1 (PD-1) cho phép phân phối nội tạng của chúng và cải thiện sự ức chế phát triển khối u. Ung thư Res. 76 , https://doi.org/10.1158/1538-7445.Am2016-2352 (2016).
- 164.Chen, CY, Hutzen, B., Wedekind, MF & Cripe, TP Oncolytic virus và liệu pháp kết hợp phong tỏa PD-1 / PD-L1. Oncolytic Virother 7 , 65–77 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 165.Ribas, A. và cộng sự. Liệu pháp virothelytic oncolytic thúc đẩy sự xâm nhập của tế bào T trong khoang miệng và cải thiện liệu pháp miễn dịch chống PD-1. Tế bào 174 , 1031-1032 (2018).
CAS PubMed Bài báo PubMed Central Google Scholar
- 166.Wolf, D. và cộng sự. Biểu hiện RIG-I cao trong ung thư buồng trứng liên quan đến dấu hiệu thoát khỏi miễn dịch và kết quả lâm sàng kém. Int. J. Cancer 146 , 2007–2018 (2020).
CAS PubMed Bài báo PubMed Central Google Scholar
- 167.Hou, J. và cộng sự. RIG-I gan dự đoán khả năng sống sót và đáp ứng điều trị interferon-alpha trong ung thư biểu mô tế bào gan. Tế bào ung thư 25 , 49–63 (2014).
CAS PubMed Bài báo PubMed Central Google Scholar
- 168.Hu, B. và cộng sự. Vi khuẩn AIM2 cảm ứng DNA kiểm soát quá trình chết tế bào và tổn thương mô do bức xạ gây ra. Khoa học 354 , 765–768 (2016).
CAS PubMed PubMed Central Bài báo Google Scholar
- 169.Man, SM và cộng sự. Vai trò quan trọng của cảm biến DNA AIM2 trong việc tăng sinh tế bào gốc và ung thư. Tế bào 162 , 45-58 (2015).
CAS PubMed PubMed Central Bài báo Google Scholar
- 170.Liu, H. và cộng sự. CGAS hạt nhân ngăn chặn quá trình sửa chữa DNA và thúc đẩy sự hình thành khối u. Nature 563 , 131–136 (2018).
CAS PubMed PubMed Central Bài báo Google Scholar
- 171.Conforti, R. và cộng sự. Tác động đối lập của tín hiệu thụ thể giống như thụ thể số (TLR3) trong các khối u có thể được tách ra khỏi phương pháp điều trị để tối ưu hóa hiệu quả chống ung thư của các phối tử TLR3. Ung thư Res. 70 , 490–500 (2010).
CAS PubMed Bài báo Google Scholar
- 172.Sun, LL và cộng sự. Sự ức chế ATR điều chỉnh giảm PD-L1 và làm nhạy cảm các tế bào khối u với quá trình giết chết qua trung gian tế bào T. Là. J. Ung thư Res. 8 , 1307–1316 (2018).
CAS PubMed PubMed Central Google Scholar
Tải xuống tài liệu tham khảo
Sự nhìn nhận
Công trình này được hỗ trợ bởi Quỹ Khoa học Tự nhiên tỉnh Chiết Giang (Số tài trợ LR19H160003), Dự án Khoa học Y tế và Công nghệ Y tế của tỉnh Chiết Giang (Số tài trợ 2020RC067) và Quỹ Khoa học Tự nhiên tỉnh Chiết Giang (Số tài trợ Q18H160015). Và tất cả các số liệu đã được tạo bằng BioRender.com.
Thông tin tác giả
Chi nhánh
- Phòng thí nghiệm Sinh học Ung thư, Phòng thí nghiệm chính về Liệu pháp Sinh học ở tỉnh Chiết Giang, Viện Ung thư của Đại học Chiết Giang, bệnh viện Sir Run Run Shaw, Trường Y, Đại học Chiết Giang, Hàng Châu, Chiết Giang, 310016, Trung Quốc
Miaoqin Chen, Shiman Hu, Yiling Li, Hongchuan Jin & Lifeng Feng
- Khoa Ung thư Bức xạ, Bệnh viện Sir Run Run Shaw, Trường Y Đại học Chiết Giang, Hàng Châu, 310016, Trung Quốc
Ting Ting Jiang
Đồng tác giả
Thư từ Lifeng Feng .